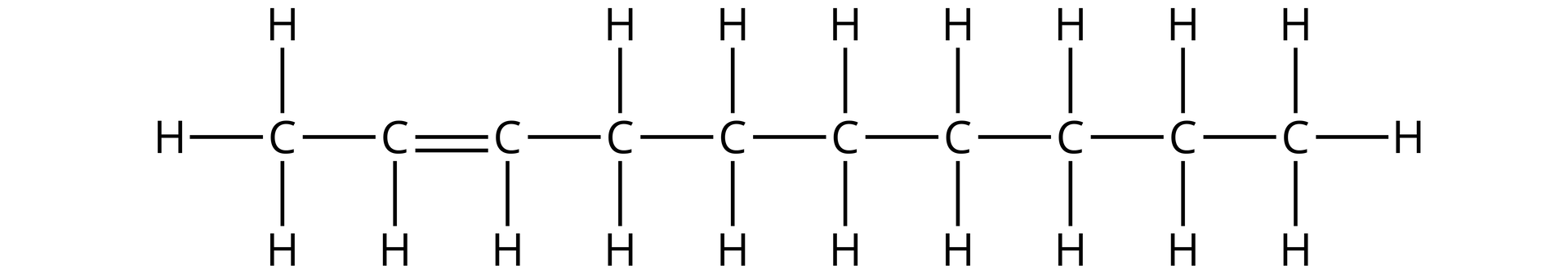
Alkeny - czym są i jak są zbudowane?
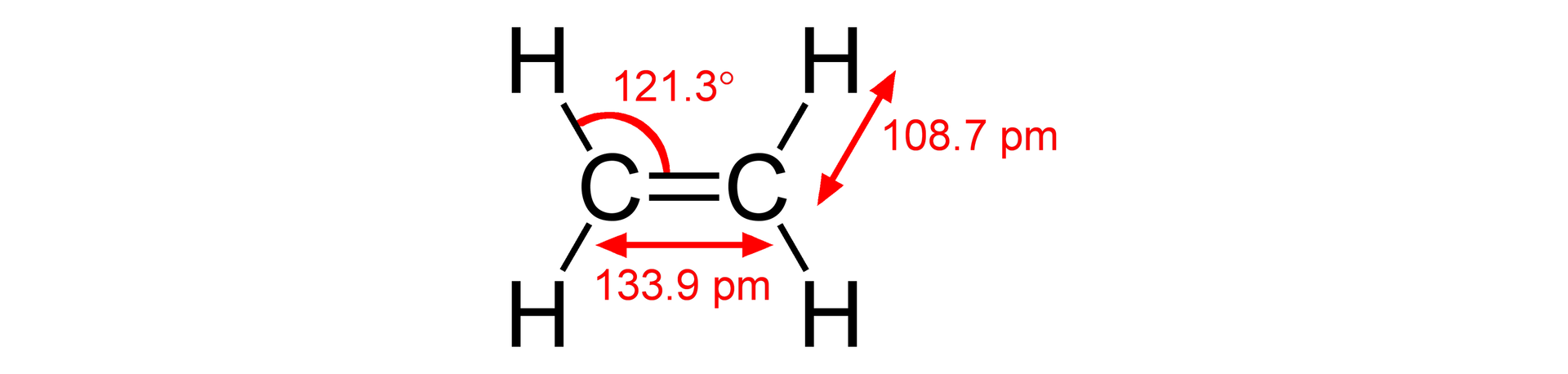
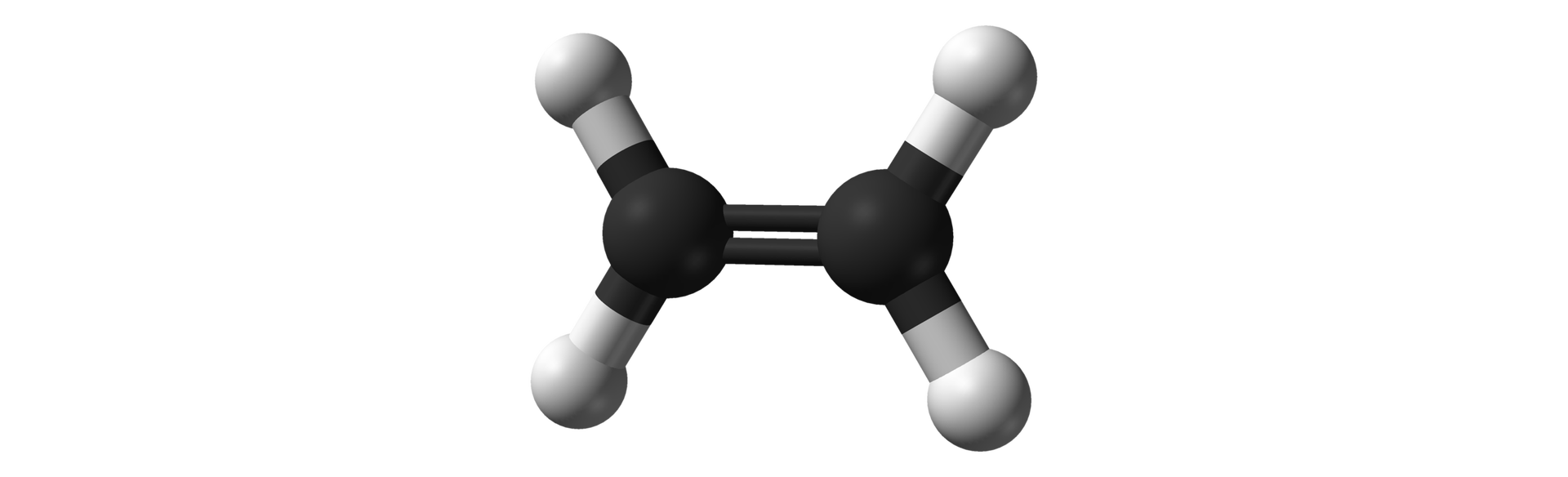
Budowa alkenów
Posiadasz już ogólne informacje na temat węglowodorów. Na ich podstawie zdobądź wiedzę szczegółową na temat jednej z rodzin węglowodorów, jaką są alkeny.
Na podstawie poniższej informacji o alkanach i parafinach oraz swoich dotychczasowych wiadomości o alkenach zastanów się, jak będą zbudowane poszczególne elementy szeregu homologicznego tych węglowodorów. Uzupełnij tabelę.
Informacja o alkanach:
Alkany zawierają w swojej budowie podstawowy szkielet węglowy i przyłączone do niego atomy wodoru. Atomy węgla scalone są ze sobą wyłącznie wiązaniami pojedynczymi (typu sigma). Alkany to związki chemiczne, które tworzą szereg homologiczny. Każdy kolejny węglowodór różni się od poprzedniego o jeden atom węgla oraz dwa atomy wodoru.
Dlaczego alkeny nie posiadają swojego odpowiednika metanu (alkan)?
Gra memory. Odkrywaj kwadraty i dopasuj wzór modelowy odpowiedniego alkenu do jego nazwy.
Nazewnictwo alkenów
Poniżej przedstawiono zestaw reguł (opracowany na podstawie zaleceń IUPAC), jakimi należy się kierować podczas konstruowania nazw alkenówalkenów.
Aby poprawnie sformułować nazwę alkenu, należy:
Przedrostek informuje o położeniu podstawnikówpodstawników, nazwa podstawowa o liczbie atomów węgla, a przyrostek jest końcówką oznaczającą grupę związków chemicznych.
Narysuj wzory strukturalne alkenów, których nazwy podano poniżej.
a) heks‑2-en
b) okt‑3-en
c) dec‑2-en
Podaj wzory grupowe alkenów, których nazwy podano poniżej.
a) heks‑2-en
b) okt‑3-en
c) dec‑2-en
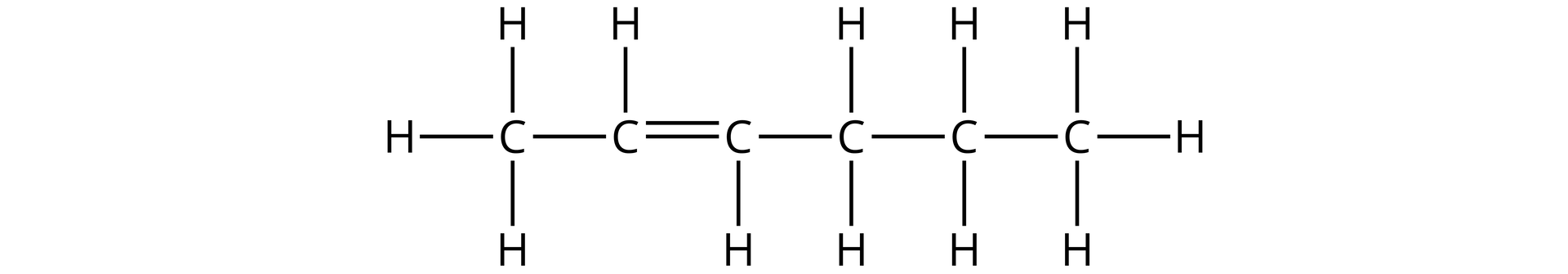
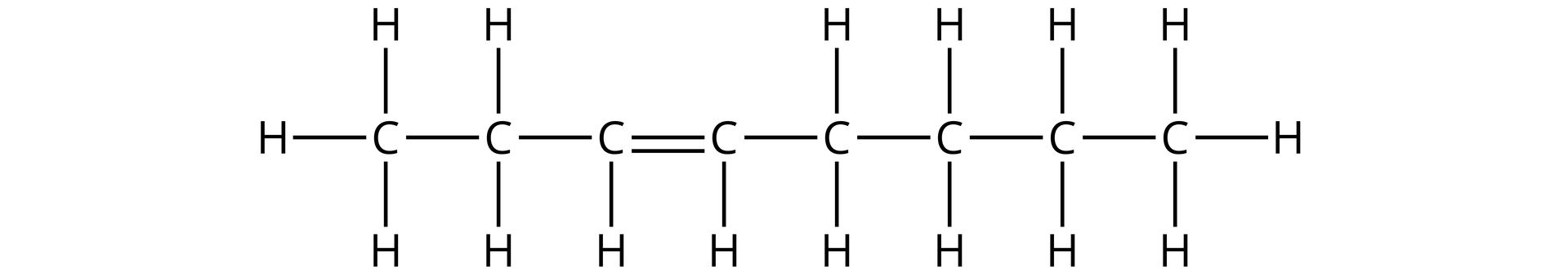
Podaj nazwy alkenów, których wzory półstrukturalne podano poniżej.
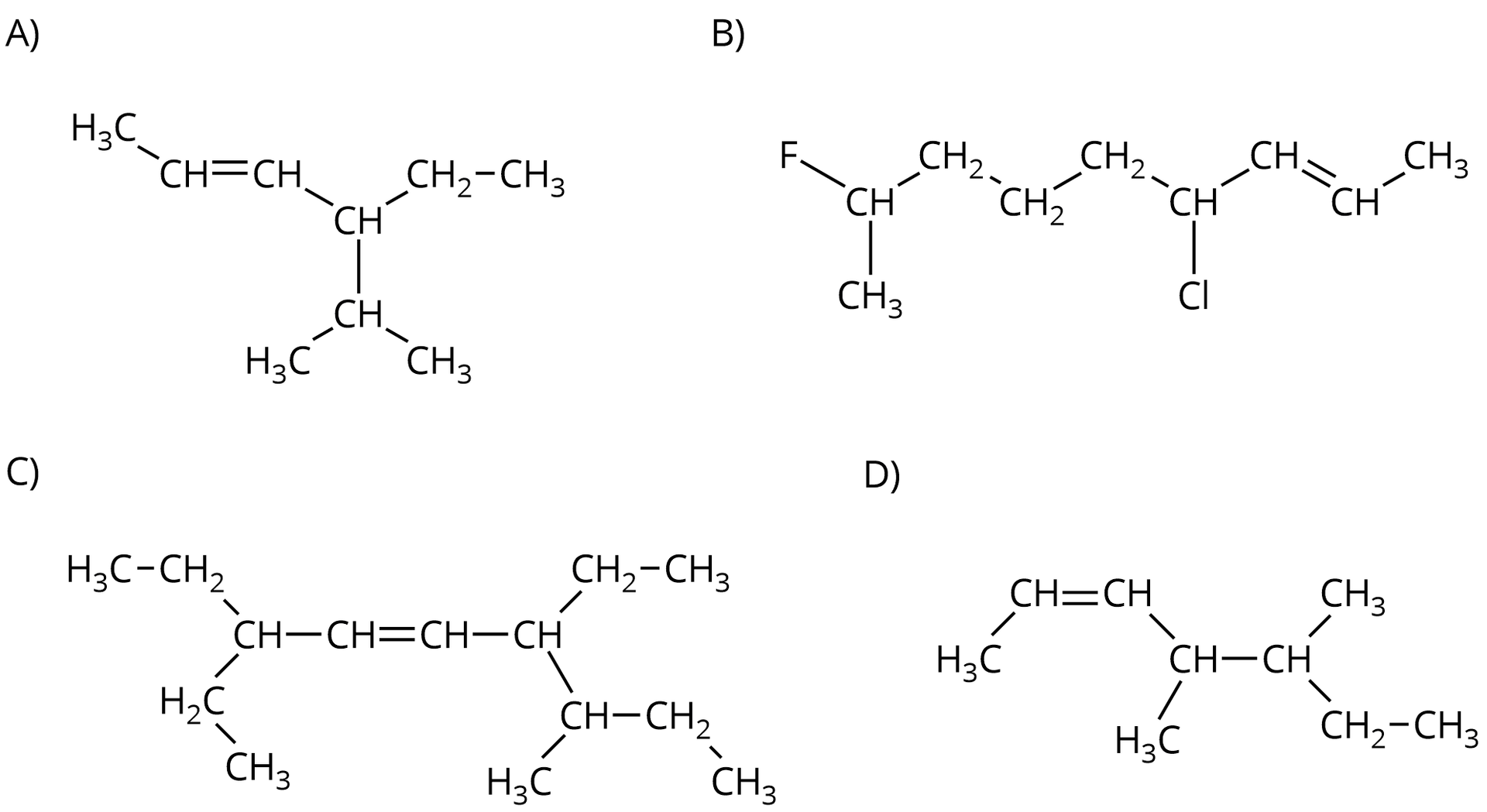
Otrzymywanie alkenów
Otrzymywanie alkenów z dihalogenopochodnych
W reakcjach eliminacji z dihalogenopochodnych alkanów istotne jest, aby atomy tego samego fluorowca były umieszczone na sąsiednich atomach węgla. O takich dihalogenopochodnych mówi się wówczas, że są to wicynalnewicynalne dihalogenowodory. Poniżej przedstawiono przykłady takich związków.
W wirtualnym laboratorium możesz przeprowadzić doświadczenie, które pozwoli na otrzymanie alkenów z dihalogenopochodnych. Wiesz, w jakich warunkach zachodzi taka reakcja? Potrafisz wymienić potrzebne odczynniki? Po wykonaniu doświadczenia uzupełnij formularz.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DFTSB7VRU
Otrzymywanie alkenów z alkoholi
Dehydratacja alkoholi jest jedną z reakcji eliminacji, w której pojedynczy substrat (alkohol) zostaje rozdzielony na dwa produkty. Innymi słowy alkohol przechodzi w alken, a produktem ubocznym reakcji dehydratacji jest woda. Poniżej przedstawiono mechanizm dehydratacji alkoholu.
Reakcja dehydratacji przebiega zgodnie z regułą Zajcewa, która mówi, że atom wodoru odrywa się od atomu węgla związanego z mniejszą liczbą atomów wodoru. Przykładowo:
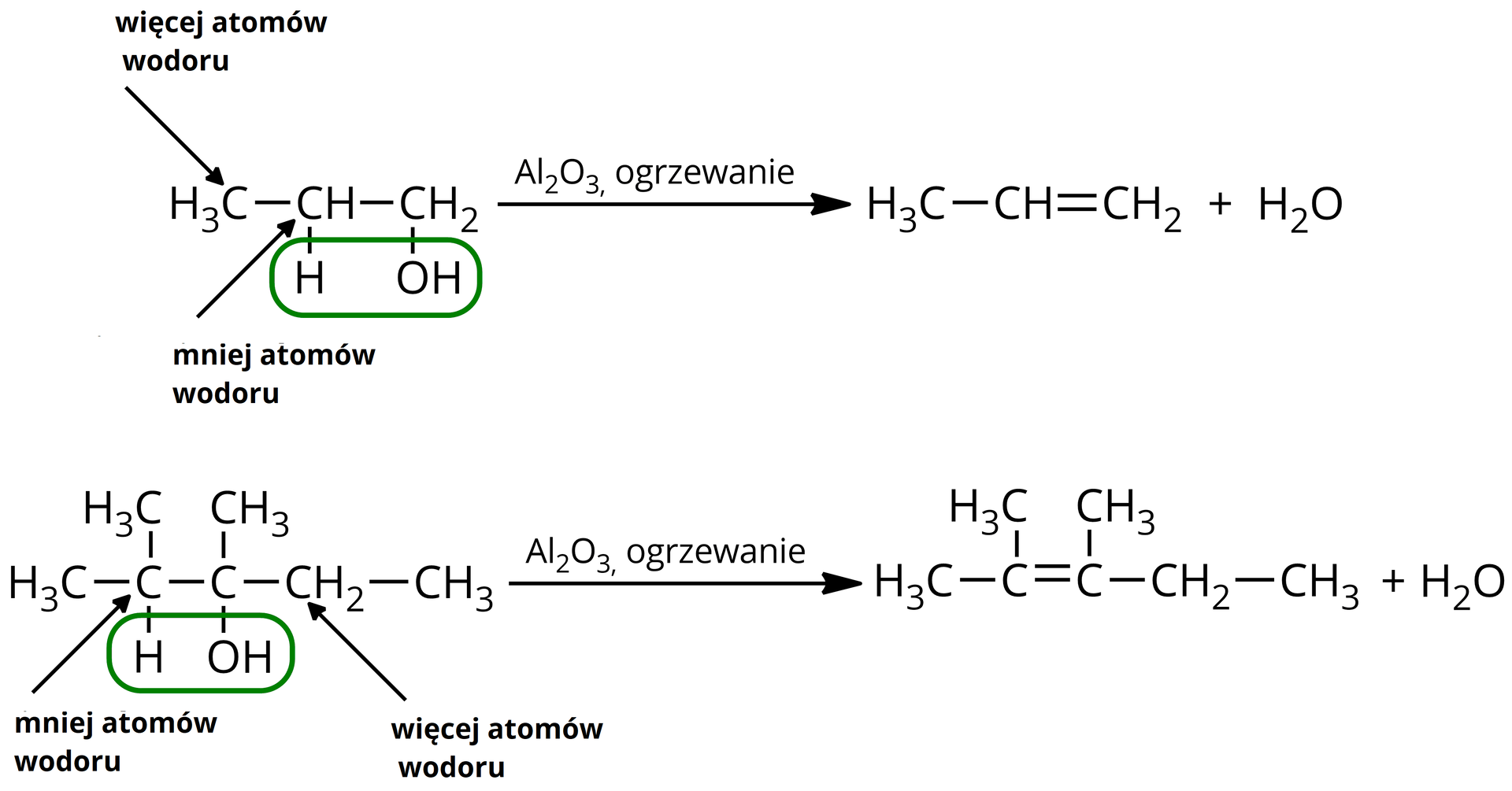
Zaznacz odpowiedź przedstawiającą produkty reakcji chemicznej przedstawionej poniżej:
Zaznacz odpowiedź przedstawiającą produkty opisanej reakcji chemicznej.

Otrzymywanie alkenów z chlorowcopochodnych
Jedną z głównych metod syntezy alkenów w warunkach laboratoryjnych jest reakcja eliminacji halogenków alkilowych, znana jako dehydrohalogenacja. W tym przypadku sąsiedztwo atomu chlorowca (chlor, brom, jod) ułatwia odłączanie się protonu od cząsteczki halogenoalkanu. Ostatecznie cząsteczka halogenopochodnej alkanu traci chlorowcowodór (), w efekcie czego powstaje alken. Chlorowcowodór z kationami, pochodzącymi od zasady, tworzy sól.

Przeanalizuj poniższą symulację interaktywną. Sprawdź, w jaki sposób z 1,2‑dichloroetanu otrzymać eten. W tym celu umieść w probówce kilka kropel wody bromowej. Następnie do kolby okrągłodennej dwuszyjnej dodaj za pomocą pęsety cynk. Do wkraplacza wprowadź kolejno 1,2‑dichloroetan oraz etanol. Połącz probówkę z kolbą za pomocą gumowego wężyka, po czym dodaj całą zawartość wkraplacza do kolby i uruchom płaszcz grzejny. Obserwuj, co się stanie i rozwiąż ćwiczenia sprawdzające.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DFTSB7VRU
Zapoznaj się z opisem symulacji interaktywnej, która dotyczy otrzymywania etenu z 1,2‑dichloroetanu, a następnie rozwiąż zadania sprawdzające.
Zadanie:
Synteza etenu z 1,2‑dichloroetanu.
Sprzęt laboratoryjny:
- probówka - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
- statyw - prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
- pipety Pasteura - wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
- dwuszyjna kolba okrągłodenna - szklane naczynie laboratoryjne z zaokrąglonym dnem;
- pęseta - narzędzie o sprężystych ramionach używane do chwytania przedmiotów, których mały rozmiar utrudnia lub uniemożliwia manipulację za pomocą rąk;
- wkraplacz - naczynie laboratoryjne służące do precyzyjnego dozowania ciekłych substancji, zazwyczaj substratów do prowadzonej w kolbie reakcji chemicznej;
- gumowy korek - niewielki element wykonany z gumy, służący do szczelnego zamykania probówek;
- gumowy wężyk - element sprzętu laboratoryjnego o kształcie miękkiej rurki, służący do łączenia różnych urządzeń i transportowania między nimi gazów i cieczy;
- płaszcz grzejny - sprzęt laboratoryjny umożliwiający podgrzewanie kolb okrągłodennych i ich zawartości. Posiada półokrągłe wgłębienie, w którym umieszcza się kolbę okrągłodenną poddawaną ogrzewaniu.
Odczynniki chemiczne:
- 1,2‑dichloroetan;
- woda bromowa;
- cynk;
- etanol.
Wykonanie:
1. Umieszczono w probówce kilka kropel wody bromowej.
2. Do kolby okrągłodennej dwuszyjnej dodano za pomocą pęsety cynk.
3. Do wkraplacza wprowadzono kolejno 1,2‑dichloroetan oraz etanol.
4. Połączono probówkę z kolbą za pomocą gumowego wężyka, po czym dodano całą zawartość wkraplacza do kolby.
5. Uruchomiono płaszcz grzejny.
Obserwacje:
Woda bromowa w probówce uległa odbarwieniu.
Stosując wzory półstrukturalne związków organicznych, zapisz równanie reakcji chemicznej, która zachodzi po wprowadzeniu zawartości wkraplacza do wnętrza kolby okragłodennej dwuszyjnej.