Badanie reaktywności żelaza i innych jego właściwości
Reakcja żelaza z tlenem
Żelazo jest metalem stabilnym na powietrzu. Jednak rozdrobnione ma właściwości piroforycznewłaściwości piroforyczne. Pod wpływem temperatury, zaczyna się utleniać, tworząc odpowiedni tlenek. W wyniku tej reakcji chemicznej powstaje tlenek żelaza() i magnetyt – tlenek żelaza(,).

Reakcje żelaza z fluorowcami
Żelazo reaguje z pierwiastkami grupy układu okresowego – fluorowcami. W wyniku reakcji chemicznej, pomiędzy żelazem a konkretnym fluorowcem powstają odpowiednie sole. W przypadku trzech pierwszych przedstawicieli grupy, żelazo w soli przyjmuje stopień utlenienia:
Gdzie .
Wyjaśnijmy to na przykładzie.
Zapisz w zeszycie równanie reakcji żelaza z fluorem, a współczynniki chemiczne dobierz, korzystając z metody bilansów elektronowego. Zapisz równania procesów utleniania i redukcji. Określ, które z indywiduów pełni funkcję utleniacza, a które reduktora.
Żelazo w odpowiednich warunkach reaguje również z jodem. W wyniku tej reakcji chemicznej, otrzymuje się jednak jodek żelaza().
Reakcje żelaza z kwasami
W zależności od użytego do reakcji chemicznej kwasu, otrzymujemy różne produkty:
kwasy o słabych właściwościach utleniających
Do kwasów o słabych właściwościach utleniających należą m.in.: kwas solny(chlorowodorowy) , kwas bromowodorowy , kwas fosforowy() , rozcieńczony kwas siarkowy() . W przypadku kwasów nieutleniających, w wyniku reakcji chemicznej metalu i kwasu, otrzymuje się sól żelaza() i wodór.
Jednak taka reakcja zachodzi tylko wtedy, gdy metal jest bardziej aktywny od wodoru. Aktywność chemiczną metali prezentuje tzw. szereg aktywności metali:
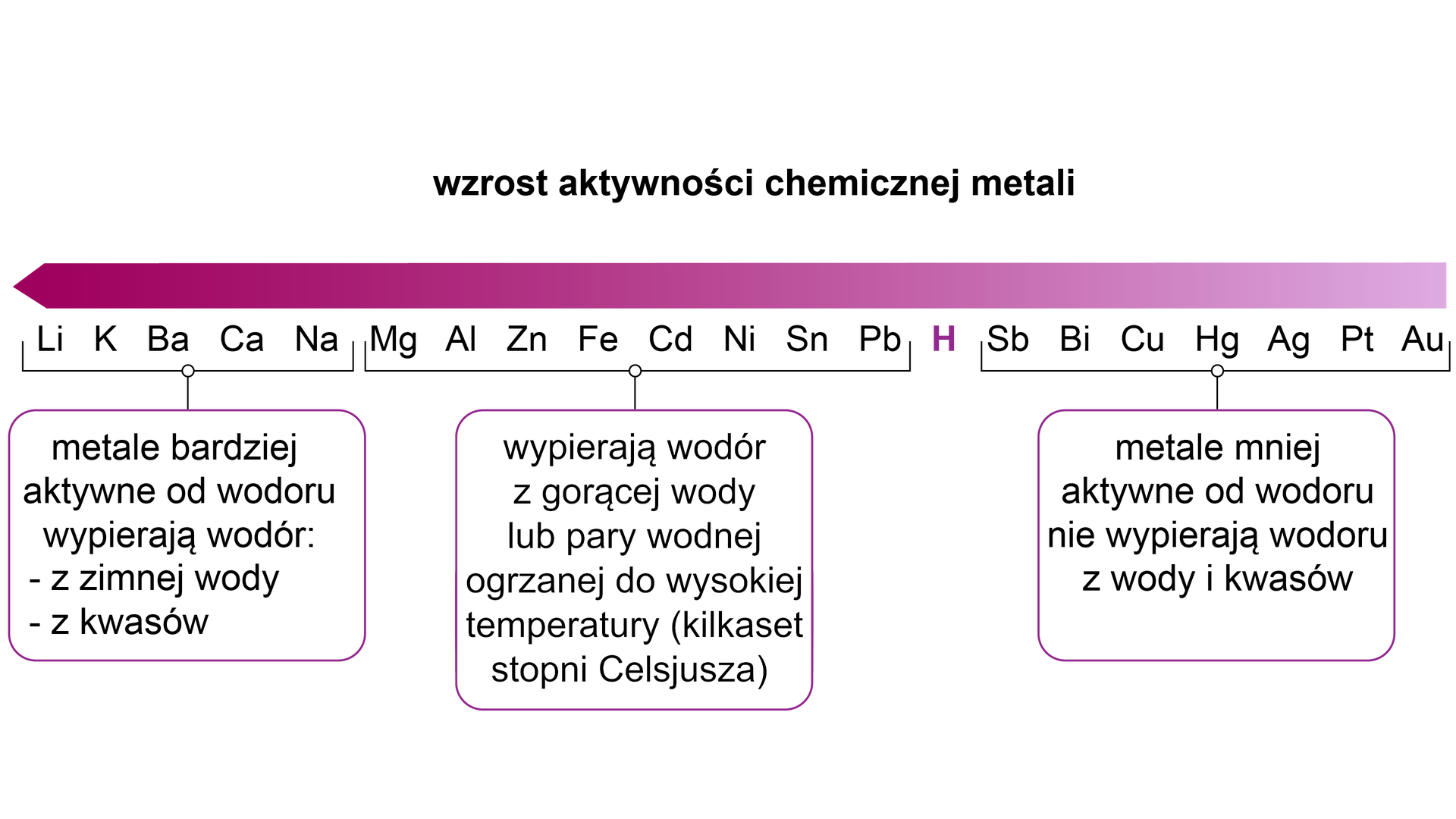
Jak łatwo zauważyć, żelazo znajduje się powyżej wodoru w szeregu aktywności metali. Dlatego też będzie będzie ono wypierać wodór z kwasów. W reakcji żelaza z kwasami nieutleniającymi powstają odpowiednie sole żelaza na stopniu utlenienia.
Wyjaśnijmy to na przykładzie.
Zapisz w zeszycie równanie reakcji żelaza z rozcieńczonym kwasem siarkowym(), a współczynniki chemiczne dobierz, korzystając z metody bilansu elektronowego. Zapisz równania procesów utleniania i redukcji. Określ, które z indywiduów pełni funkcję utleniacza, a które reduktora.
kwasy o silnych właściwościach utlenijących
Do kwasów o silnych właściwościach utleniających zaliczamy: kwas azotowy() stężony i rozcieńczony () i stężony kwas siarkowy() ().
Kwasy o silnych właściwościach utleniających reagują z metalami aktywniejszymi od wodoru (z wyjątkiem metali pasywujących), jak i z metalami szlachetnymi – mniej aktywnymi od wodoru (z wyjątkiem platyny i złota). W wyniku reakcji chemicznej, pomiędzy metalem a kwasem utleniającym powstaje sól i tlenek otrzymany w wyniku redukcji reszty kwasowej.
Żelazo, w wyniku reakcji ze stężonymi kwasami utleniającymi, ulega pasywacji, pokrywając się szczelnie warstewką odpowiedniego tlenku, przez co nie reaguje ze stężonymi kwasami utleniającymi.
W reakcjach chemicznych żelaza z rozcieńczonym kwasem azotowym() powstają sole żelaza na stopniu utlenienia. Wyjaśnijmy to na przykładzie.
Zapisz w zeszycie równanie reakcji żelaza z rozcieńczonym kwasem azotowym(), a współczynniki chemiczne dobierz, korzystając z metody bilansu elektronowego. Zapisz równania procesów utleniania i redukcji. Określ, które z indywiduów pełni funkcję utleniacza, a które reduktora.
Czy wiesz, jak żelazo zachowuje się w reakcji z tlenem oraz kwasami? Przeanalizuj poniższą symulację interaktywną i sprawdź, jaką reaktywnością charakteryzuje się ten metal. Następnie wykonaj ćwiczenia sprawdzające.
Czy wiesz, jak żelazo zachowuje się w reakcji z tlenem oraz kwasami? Przeanalizuj opis poniższej symulacji interaktywnej i sprawdź, jaką reaktywnością charakteryzuje się ten metal. Następnie wykonaj ćwiczenia sprawdzające.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D758EEUXQ
Żelazo pod wpływem ogrzewania: Możliwe odpowiedzi: 1. zachowuje swój pierwotny stan, nie zmienia zabarwienia., 2. zmienia zabarwienie, brunatnieje na powietrzu., 3. zmienia zabarwienie, robi się czarne.
azotowym(pięć), ponieważ ulega pasywacji.. Możliwe odpowiedzi: Prawda, Fałsz. Żelazo, reagując z rozcieńczonym kwasem azotowym(pięć), roztwarza się i barwi wówczas roztwór na kolor jasnozielony.. Możliwe odpowiedzi: Prawda, Fałsz