Berylowce - właściwości fizykochemiczne i otrzymywanie
Berylowce są miękkimi, srebrzystobiałymi metalami, które, będąc aktywne chemicznie, występują w przyrodzie wyłącznie w postaci związków chemicznych. Wapń, bar oraz stront, ze względu na dużą reaktywność, przechowuje się w nafcie. W związkach chemicznych berylowce przyjmują stopień utlenienia.
Jakie pierwiastki zaliczamy do berylowców? Zapoznaj się z poniższym filmem samouczkiem, a następnie rozwiąż ćwiczenia sprawdzające.

Film dostępny pod adresem /preview/resource/R9ApUChtuch35
Film opowiada o pierwiastkach należących do berylowców. Została omówiona ich charakterystyka oraz zastosowania.
Konfiguracje elektronowe wybranych berylowców
Berylowiec | Konfiguracja elektronowa | Konfiguracja elektronowa (zapis z użyciem rdzenia gazu szlachetnego) | Konfiguracja elektronowa (pełna) |
|---|---|---|---|
Właściwości fizykochemiczne berylowców
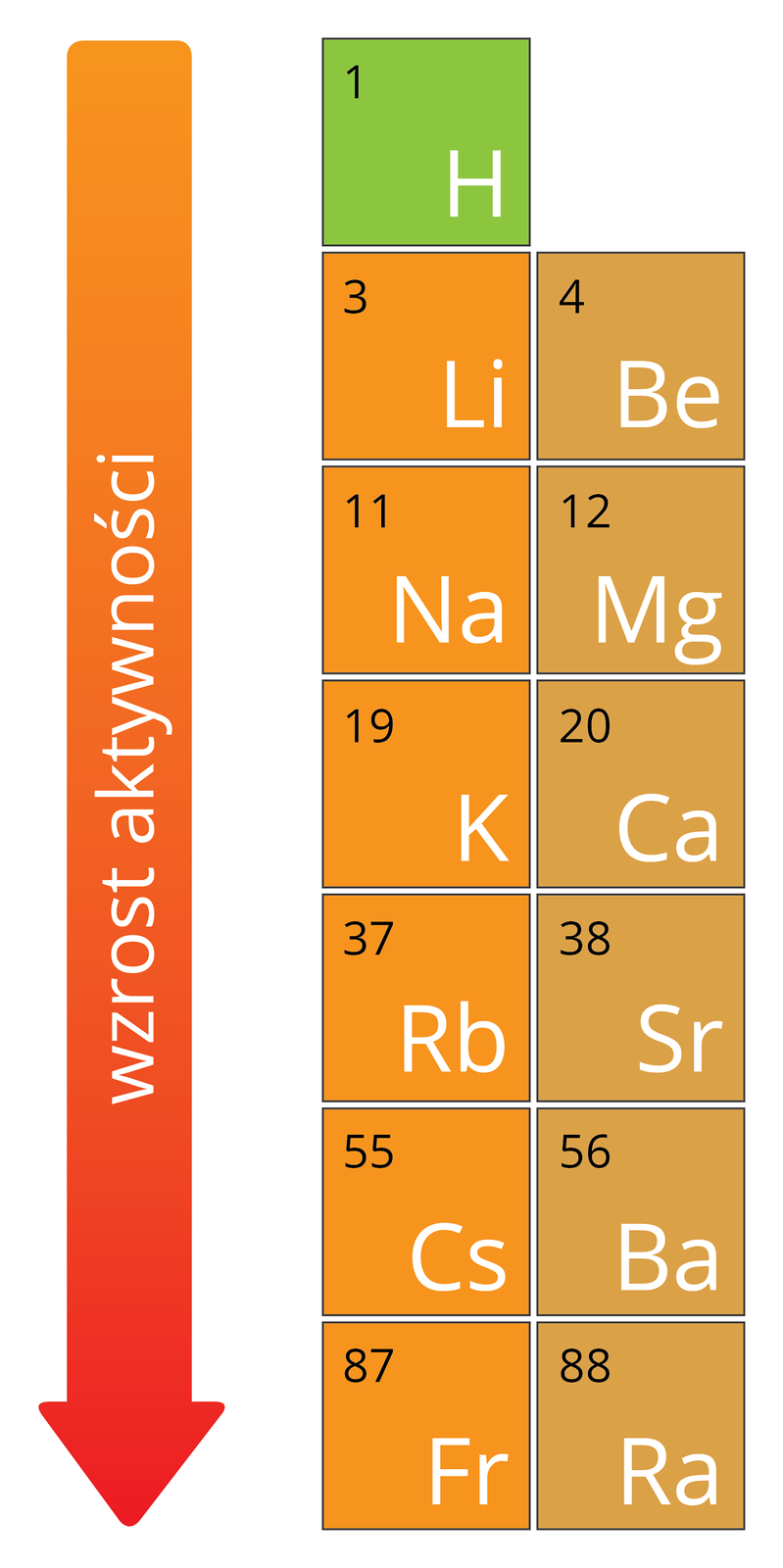
Porównując konfigurację elektronową berylowców i litowców – które posiadają tylko jeden elektron walencyjny – można zauważyć, że do uzyskania konfiguracji gazu szlachetnego, czyli do całkowitego zapełnienia powłok elektronowych, berylowce muszą oddać dwa elektrony. Wymaga to większej energii niż w przypadku oddania tylko jednego elektronu, dlatego wartość energii jonizacji berylowców jest większa niż litowców, a ich reaktywność mniejsza.
Berylowce reagują z wodą, ale nie aż tak gwałtownie jak litowce. Reaktywność berylowców rośnie w dół grupy, wynika to z tego, że elektrony walencyjne znajdują się dalej od jądra atomowego, które słabiej na nie oddziałuje. Są więc bardziej ekranowane od jądra.
Promienie atomowe i jonowe litowców i berylowców
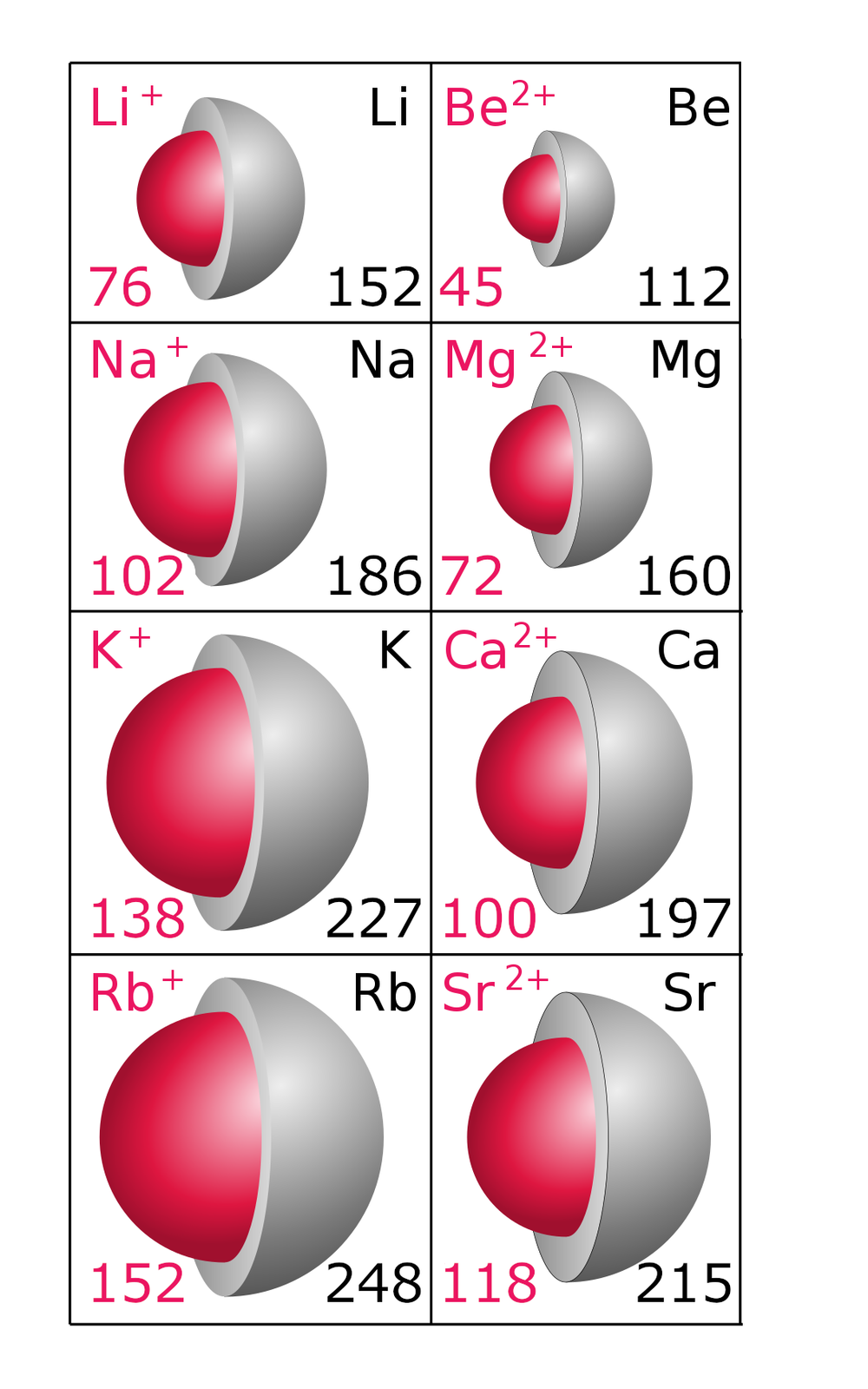
Porównując promienie jonowe litowców i berylowców można zauważyć, że berylowce z tego samego okresu co litowce mają mniejszy promień atomowy. Ponieważ jądra berylowców zawierają o jeden proton więcej niż litowców, to silniej przyciągają elektrony, co powoduje skrócenie promieni atomowych oraz wzrost energii potrzebnej do oderwania elektronów.
Jednym ze znanych minerałów, zawierających w swojej cząsteczce jony berylu, jest szmaragd.

Zmiany właściwości berylowców związane ze wzrostem liczby atomowej
Jakimi właściwościami charakteryzują się berylowce? Dlaczego beryl różni się od pozostałych berylowców?

Film dostępny pod adresem /preview/resource/RqeOtoEsrlO7l
Film nawiązujący do treści materiału
Zaznacz prawidłową odpowiedź.
Który z berylowców ma większą skłonność do tworzenia wiązań kowalencyjnych niż pozostałe?
Magnez wykazuje dobre przewodnictwo elektryczne ze względu na: Możliwe odpowiedzi: 1. obecność gazu elektronowego., 2. występowanie kationów., 3. budowę kowalencyjną., 4. stosunkowo wysoką aktywność chemiczną.
Dlaczego wapń przechowywany jest w argonie lub nafcie?

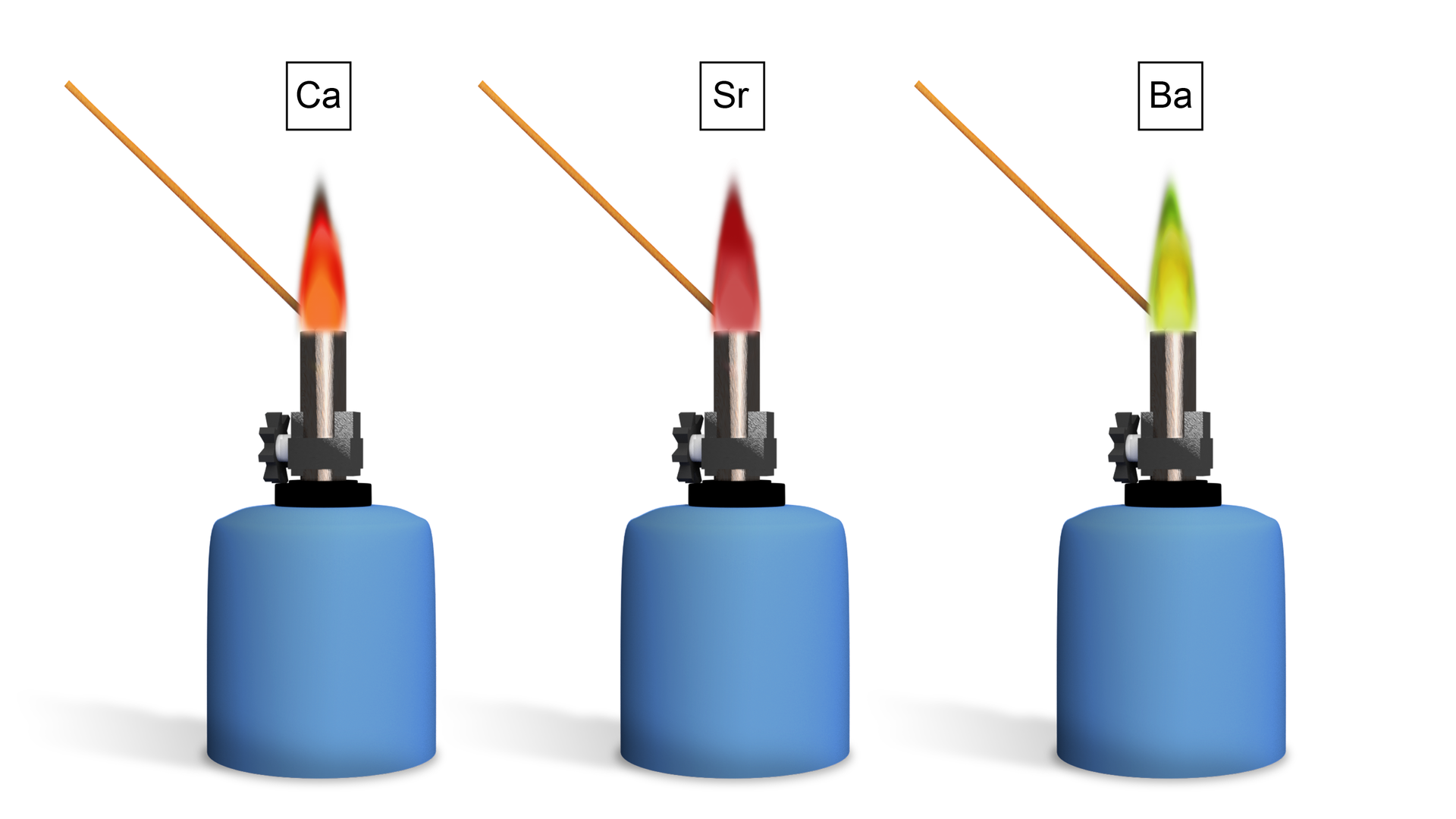
Sole berylowców wprowadzone do płomienia palnika barwią go w charakterystyczny sposób
Podczas wprowadzenia roztworu soli berylowców do płomienia następuje wzbudzenie atomu metalu, co skutkuje zabarwieniem się płomienia na odpowiedni kolor. Tą metodę wykorzystuje się do analizy kationów.
Otrzymywanie berylowców
Magnez można otrzymać w wyniku elektrolizy stopionego chlorku magnezu. Wapń i stront otrzymuje się podczas elektrolizy soli, takich jak chlorek wapnia czy chlorek strontu.
Elektroliza stopionego
Elektroliza stopionego
A nawias, plus, zamknięcie nawiasu luka do uzupełnienia luka do uzupełnienia strzałka w prawo, C l indeks dolny, dwa, koniec indeksu dolnego, plus luka do uzupełnienia luka do uzupełnienia
K nawias, minus, zamknięcie nawiasu luka do uzupełnienia plus, dwa e indeks górny, minus, koniec indeksu górnego, strzałka w prawo luka do uzupełnienia
Przeprowadzono doświadczenie, w którym do probówki ze wody dodano magnezu oraz kilka kropel roztworu fenoloftaleiny. Zapisz cząsteczkowe równanie reakcji chemicznej, jakie zaszło w probówce, oraz obserwacje. Dodatkowo oblicz, ile gramów gazu wydzieliło się z probówki (do zakończenia reakcji). Wynik zaokrąglij do dwóch miejsc po przecinku.