Co warto wiedzieć o związkach wodoru z innymi pierwiastkami?
Czym są wodorki?
Wodorki to związki wodoru z innymi pierwiastkami. Ze względu na skład, wodorki możemy podzielić na:
wodorki niemetali – związki, w których wodór występuje na stopniu utlenienia;
wodorki metali – związki, w których wodór występuje na stopniu utlenienia.
Zmiany wartościowości pierwiastków bloku i względem wodoru
Pierwiastki chemiczne mogą tworzyć wodorki metali i niemetali. Tworzą je głównie pierwiastki bloku i , jak na poniższej grafice.
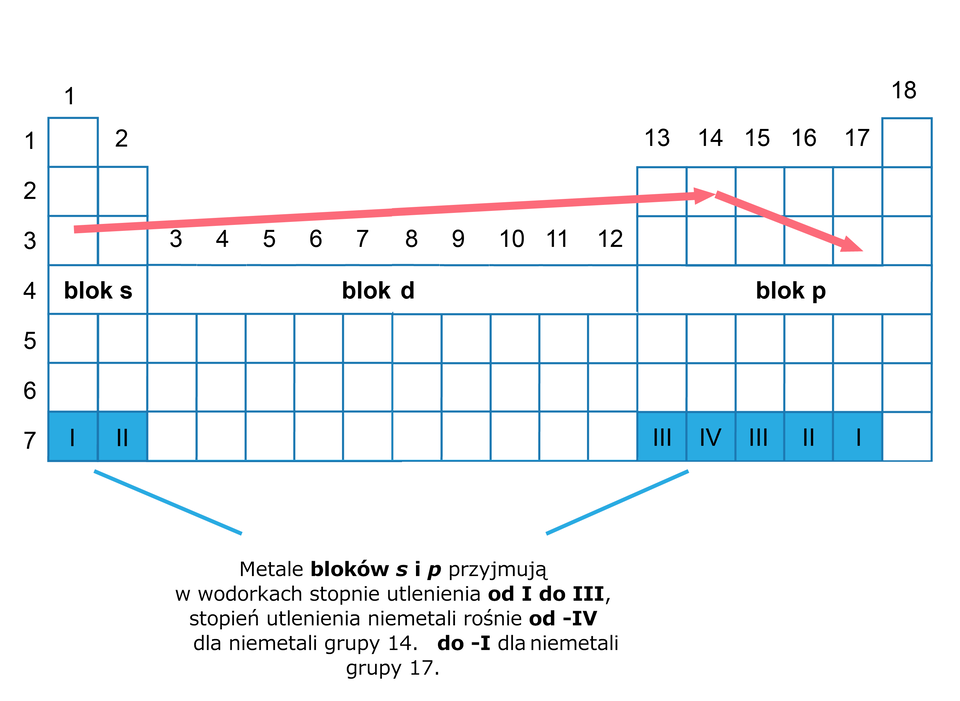
Pierwiastki bloku tworzą z wodorem tzw. wodorki metaliczne (śródwęzłowe). W większości nie można wyrazić ich prostymi wzorami, ponieważ są to związki niestechiometryczne.
Nomenklatura i wzory
Wzory sumaryczne wodorków tworzy się poprzez umieszczenie pierwiastka bardziej elektroujemnego po prawej stronie. Zatem poprawny zapis dla tego typu związku z sodem to a nie , natomiast dla związku wodoru z chlorem to , nie . Do ustalenia wzoru sumarycznego wodorków ważne jest ustalenie, z jakim typem związku mamy do czynienia i jaki jest stopień utlenienia pierwiastka macierzystego (innego niż wodór), który go tworzy:
Wodorki pierwiastków i grupy układu okresowego
Wzory wodorków pierwiastków grupy i włącznie zapisuje się następująco:
– atom metalu lub niemetalu grupy , , , , oraz metale bloku ;
– symbol wodoru;
– indeks stechiometryczny, będący, co do wartości, równy stopniowi utlenienia metalu.
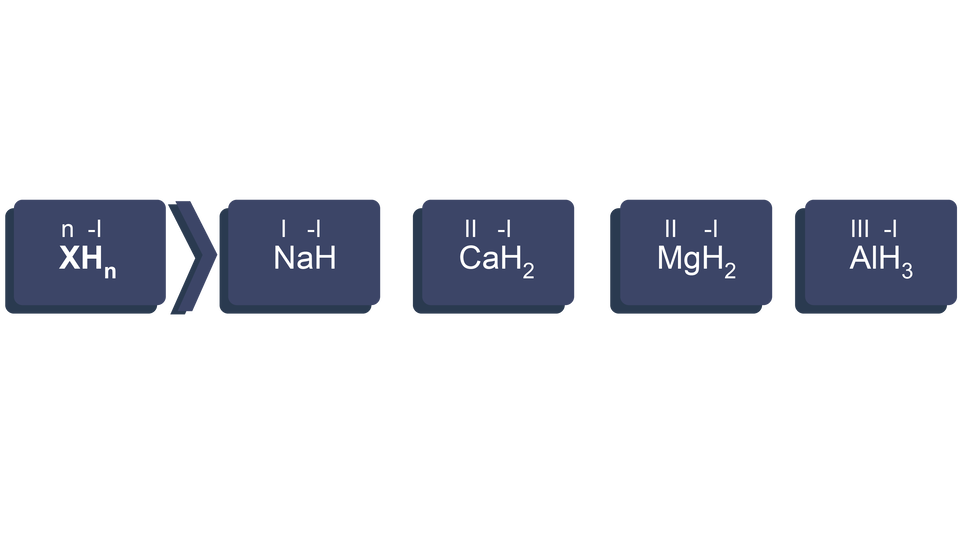
Nazwy takich wodorków tworzymy przez podanie słowa „wodorek” oraz podanie nazwy pierwiastka w dopełniaczu:
– wodorek sodu;
– wodorek wapnia;
– wodorek magnezu;
– wodorek glinu.
Wodorki pierwiastków i grupy układu okresowego
Wzory wodorków i grupy układu okresowego można zapisać ogólnie:
– atom niemetalu grupy i ;
– atom wodoru;
– indeks stechiometryczny, będący, co do wartości, równy wartości bezwzględnej ze stopnia utlenienia atomu niemetalu, połączonego z atomem wodoru.
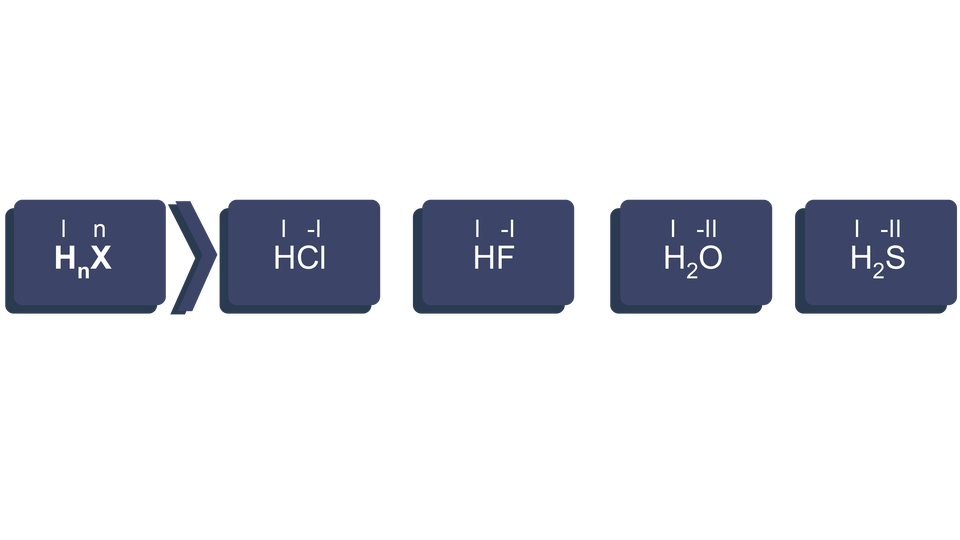
Nazwy tych wodorków tworzymy przez połączenie nazwy pierwiastka ze słowem „wodór” za pomocą litery „o”:
– chlorowodór;
– fluorowodór;
– siarkowodór;
– dla tego związku zwyczajowo stosujemy nazwę: woda.
Oczywiście dopuszczalne jest stosowane nazw „wodorek fluoru” w miejsce „chlorowodór”, czy „wodorek siarki” w miejsce „siarkowodór”, etc. Jako ciekawostkę należy wskazać, że nazwą zalecaną dla tlenku wodoru, czyli wody, jest oksydan, a dla amoniaku – (wodorku azotu) azan.
Pozostałe
Do innych znanych wodorków niemetali można zaliczyć następujące związki:
związek wodoru z azotem na stopniu utlenienia: (amoniak);
związek wodoru z fosforem na stopniu utlenienia: ;
związek wodoru z krzemem: .
Ustal wzór sumaryczny wodorku wapnia.
Wapń występuje w drugiej grupie głównej układu okresowego pierwiastków. Jego stopień utlenienia zatem to . Analizując tę informacje w kontekście wzoru ogólnego wodorków metali:
Otrzymujemy wzór wodorku wapnia:
Ustal nazwę wodorku .
Dla wodorków niemetali moglibyśmy zastosować dwie alternatywne nazwy. Jedna, opisowa, polega na zastosowaniu słowa „wodorek”, a następnie określenie, czego (dopełniacz) ten wodorek jest. W tym wypadku byłby to wodorek krzemu. Drugi sposób to połączenie nazwy pierwiastka ze słowem „wodór” za pomocą litery „o”, zatem krzemowodór.
Budowa wybranych wodorków
Wodorki litowców
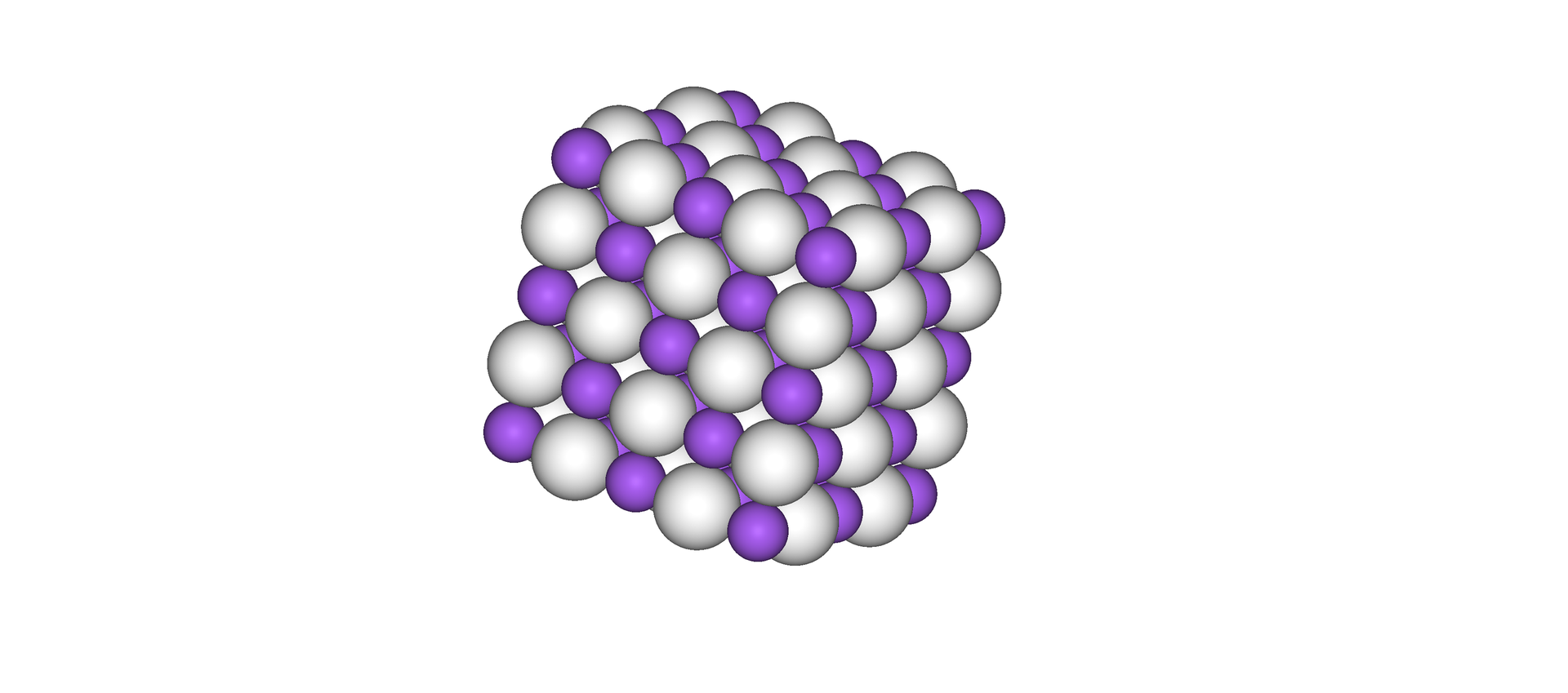
Wodorki litowców są związkami o budowie jonowej – typu soli, w których metal występuje w postaci kationu, a wodór w postaci anionu. Tworzą one sieci krystaliczne typu chlorku sodu.
Wodorki berylowców
Wodorek berylu
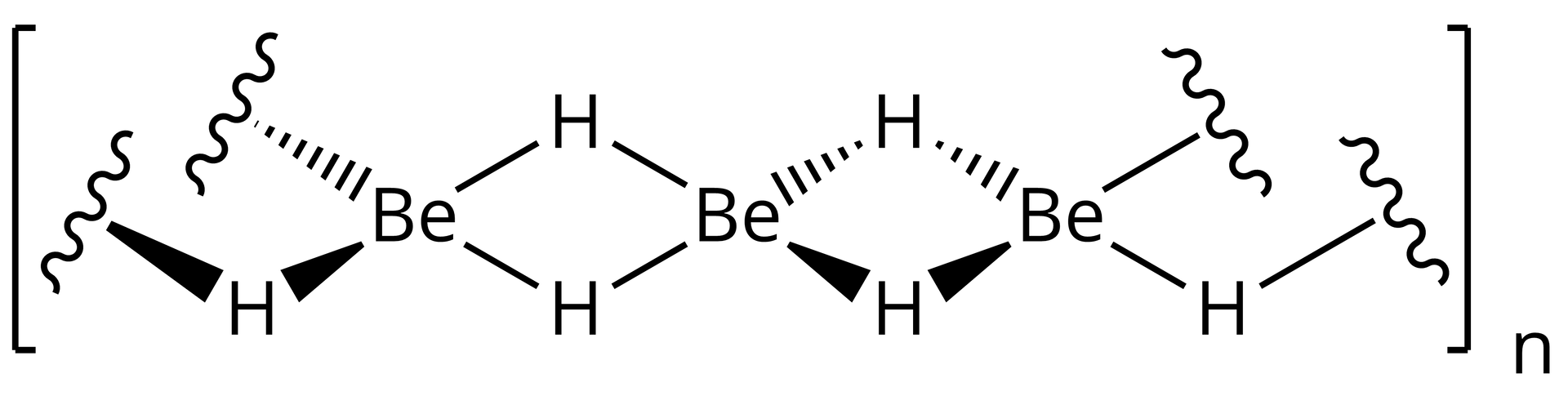
Beryl tworzy wodorek o wiązaniach kowalencyjnych. Wodorek berylu to substancja bezbarwna, która ulega rozkładowi w temperaturze .
Jego sieć przestrzenną tworzą polimeryczne łańcuchy, beryl w nich jest związany kowalencyjnymi wiązaniami trójcentrowymitrójcentrowymi .
Wodorek magnezu
Można znaleźć dwie przeciwstawne informacje w literaturze – jedna z nich mówi o budowie jonowej wodorku magnezu, a druga o występowaniu w nim wiązań kowalencyjnych. W praktyce wodorek wagnezu wykazuje strukturę pośrednią w zależności od warunków.
Wodorki pozostałych berylowców
Pozostałe pierwiastki drugiej grupy układu okresowego (wapń, stront, bar, rad) tworzą wodorki typowo jonowe.
Budowa cząsteczki amoniaku
Czy wiesz, jaki związek kryje się pod nazwą „azan”? Czy wiesz, jak zbudowana jest cząsteczka azanu? Zapoznaj się z animacją, a następnie wykonaj zadania znajdujące się poniżej.

Film dostępny pod adresem /preview/resource/R1HFfgTjC3iQH
Film nawiązujący do treści materiału - dotyczy budowy cząsteczki azanu.
Otrzymywanie wodorków
Wodorki można otrzymać różnymi metodami:
bezpośrednia synteza w określonych warunkach (czasami w obecności katalizatora), np.:
wodorki niemetali, np.
wodorki metali, np.
inne wybrane przykłady:
— substraty są stopione;
(reakcja zachodzi w środowisku eteru).
Otrzymywanie wodorków 17. grupy w wyniku syntezy bezpośredniej
Tak jak większość wodorków, wodorki pierwiastków 17. grupy można otrzymać w reakcji syntezy bezpośredniej danego pierwiastka z wodorem.
Spośród fluorowców wyróżnia się fluor, który z wodorem łączy się samorzutnie. Reakcja ta jest gwałtowna, wybuchowa, oraz przebiega bez dostępu światła i w niskiej temperaturze. W jej wyniku powstaje fluorowodór:
Otrzymany fluorowodór – nawet przy śladowych ilościach wody – staje się bardzo aktywny. Jego roztwór wodny, czyli kwas fluorowodorowy, ma właściwości żrące i silnie toksyczne.

Synteza wodorków innych fluorowców przebiega z udziałem światła, płomienia lub katalizatorów.
Reakcja chloru z wodorem wymaga światła lub płomienia:
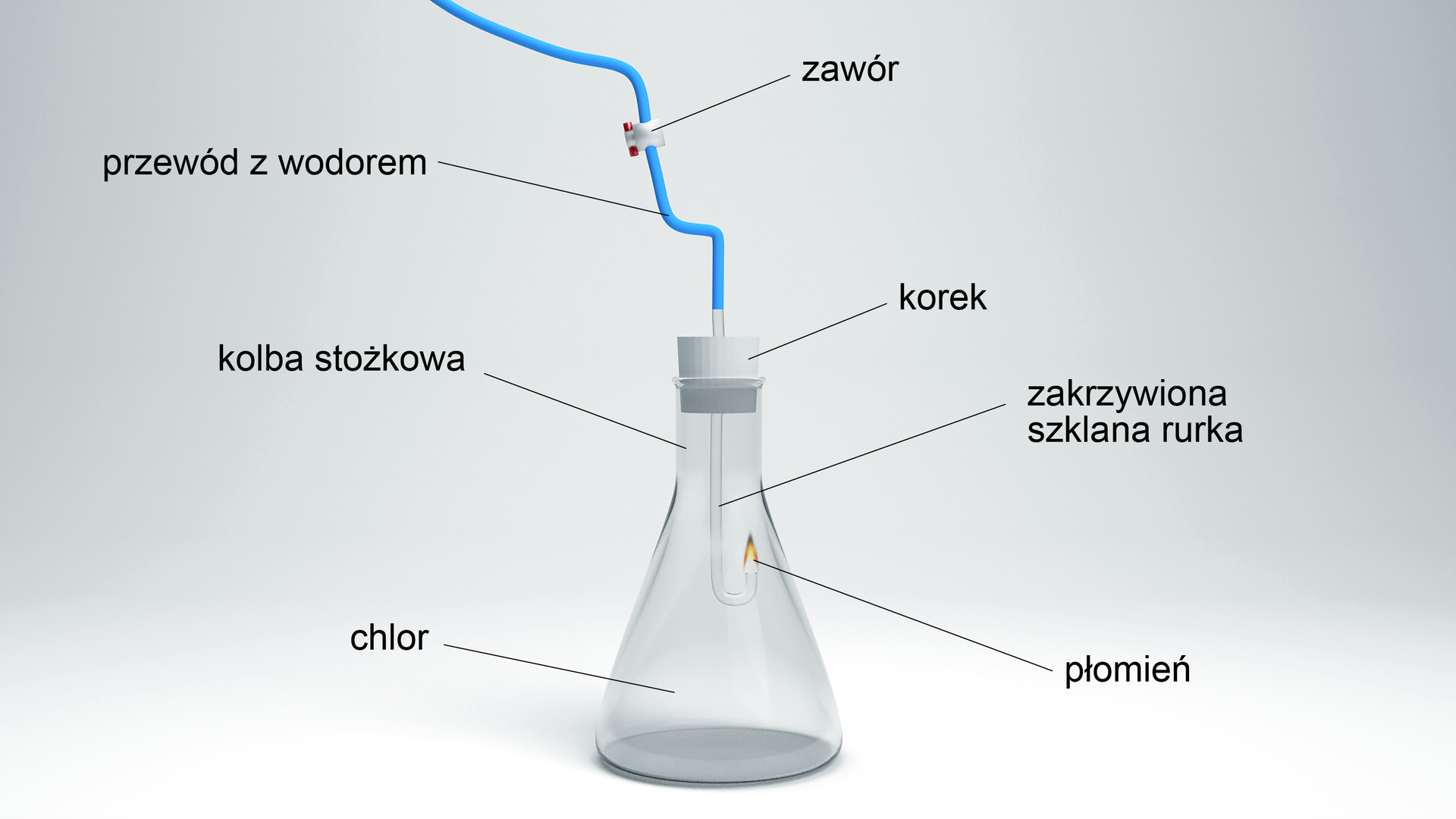
Syntezę chlorowodoru w laboratorium przeprowadza się pod sprawnie działającym wyciągiem. Zarówno chlor, jak i produkt reakcji, a mianowicie chlorowodór, są gazami drażniącymi i toksycznymi.
Brom i jod reagują z wodorem znacznie łagodniej.
Ciekły brom łączy się z wodorem po podgrzaniu lub w obecności katalizatora (np. platyny). W wyniku reakcji powstaje gazowy bromowodór. Jest to reakcja odwracalna, ponieważ bromowodór dość łatwo rozkłada się na pierwiastki.
Podobnie przebiega reakcja syntezy jodwodoru:
Jak budowa związku wpływa na jego właściwości fizykochemiczne?
Właściwości fizyczne, takie jak np. stan skupienia w temperaturze pokojowej oraz właściwości chemiczne (rozpuszczalność w wodzie, charakter kwasowo–zasadowy), wynikają z budowy danego związku oraz z charakteru występującego w nim wiązania.
Na podstawie temperatury wrzenia można wysnuć wnioski dotyczące rodzaju wiązania oraz oddziaływań międzycząsteczkowych. Niskie temperatury wrzenia cechują substancje zbudowane z cząsteczek o charakterze niepolarnym, wówczas jedynym rodzajem oddziaływań, które zachodzą między cząsteczkami, są wyłącznie słabe oddziaływania van der Waalsa. Silniejsze oddziaływania obserwuje się między dipolami, a z kolei obecność atomu wodoru, związanego z silnie elektroujemnym atomem fluoru, tlenu lub azotu, warunkuje możliwość tworzenia wiązań wodorowych. Najwyższe temperatury wrzenia są obserwowane dla substancji o budowie jonowej, ponieważ wiązanie jonowe ma charakter kolektywny, tj. obejmuje wszystkie jony, które wchodzą w skład kryształu.
Budowa związku chemicznego warunkuje także właściwości chemiczne, takie jak charakter kwasowy lub zasadowy.
Właściwości fizyczne i chemiczne wodorków
Wodorki niemetali mają następujące właściwości:

Wodorki metali mają odmienne właściwości:
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje i wyniki, a następnie sformułuj wnioski. Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się pod ikoną notatnika w lewym górnym rogu.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5HSUC797
Analiza doświadczenia: Badanie właściwości fizykochemicznych wodorków.
Problem badawczy: Czy właściwości fizykochemiczne wodorków zależą od rodzaju wodorku?
Hipoteza: Właściwości fizykochemiczne wodorków są zależne od rodzaju wodorku.
Odczynniki: wodorek wapnia, metan, amoniak, siarkowodór, chlorowodór, alkoholowy roztwór fenoloftaleiny, roztwór oranżu metylowego, woda destylowana.
Sprzęt laboratoryjny: pięć probówek podłużnych – naczynie szklane do przeprowadzania prostych reakcji chemicznych; statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki; cztery korki – niewielki element wykonany z plastiku, służący do szczelnego zamykania probówek; pięć zlewek – naczynia szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych; cztery rurki szklane.
Instrukcja wykonania doświadczenia:
1. Zbadano właściwości fizyczne następujących związków: wodorku wapnia, metanu, amoniaku, siarkowodoru oraz chlorowodoru.
2. Zbadano właściwości chemiczne tych samych związków.
3. Do pięciu zlewek dodano wodę destylowaną. Do zlewek numer i dodano kilka kropli alkoholowego roztworu fenoloftaleiny, a do zlewek numer i roztwór oranżu metylowego.
4. Do pierwszej zlewki wsypano wodorek wapnia.
5. W probówkach z gazami, zatkanych korkiem, umieszczono rurki, a następnie umieszczono je dnem do góry w zlewkach w sposób następujący: zlewka numer – metan, zlewka numer – amoniak, zlewka numer – siarkowodór, zlewka numer – chlorowodór.
6. Zaobserwowano zmiany.
Obserwacje:
Badanie właściwości fizycznych:
Stan skupienia: metan, amoniak, kwas siarkowodorowy i kwas chlorowodorowy są bezbarwnymi gazami, zaś wodorek wapnia białym ciałem stałym.
Zapach: wodorek wapnia i metan są bezwonne, amoniak i kwas siarkowodorowy mają charakterystyczny zapach, natomiast kwas chlorowodorowy ma ostry, drażniący zapach.
Badanie właściwości chemicznych:
Zlewka : po wprowadzeniu wodorku wapnia do zlewki z wodą destylowaną wydziela się bezbarwny gaz oraz pojawia się biały osad.
Zlewka : brak dostrzegalnych zmian.
Zlewka : gaz rozpuszcza się w wodzie, powstały roztwór zmienia zabarwienie na kolor malinowy.
Zlewka : gaz rozpuszcza się w wodzie, powstały roztwór zmienia zabarwienie na kolor czerwony.
Zlewka : gaz rozpuszcza się w wodzie, powstały roztwór zmienia zabarwienie na kolor czerwony.
Wyniki:
Wydzielającym się gazem w reakcji wodorku wapnia z wodą destylowaną jest wodór. Brak zmiany zabarwienia w przypadku roztworu w zlewce numer świadczy o jego obojętnym odczynie. W zlewce numer dostrzegalna jest zmiana zabarwienia roztworu na kolor malinowy, co charakteryzuje roztwory o odczynie zasadowym. W zlewce numer i roztwory zmieniają zabarwienie na kolor czerwony, co warunkuje ich kwasowy odczyn.
Wnioski:
Hipoteza została potwierdzona – właściwości fizyczne i chemiczne są zależne od rodzaju wodorku.
Przeanalizuj poniższą symulację. Zwróć uwagę, jak zmieniają się właściwości fizykochemiczne wodorków pierwiastków grupy, a następnie rozwiąż ćwiczenia sprawdzające.
Zapoznaj się z opisem symulacji. Zwróć uwagę, jak zmieniają się właściwości fizykochemiczne wodorków pierwiastków grupy, a następnie rozwiąż ćwiczenia sprawdzające.
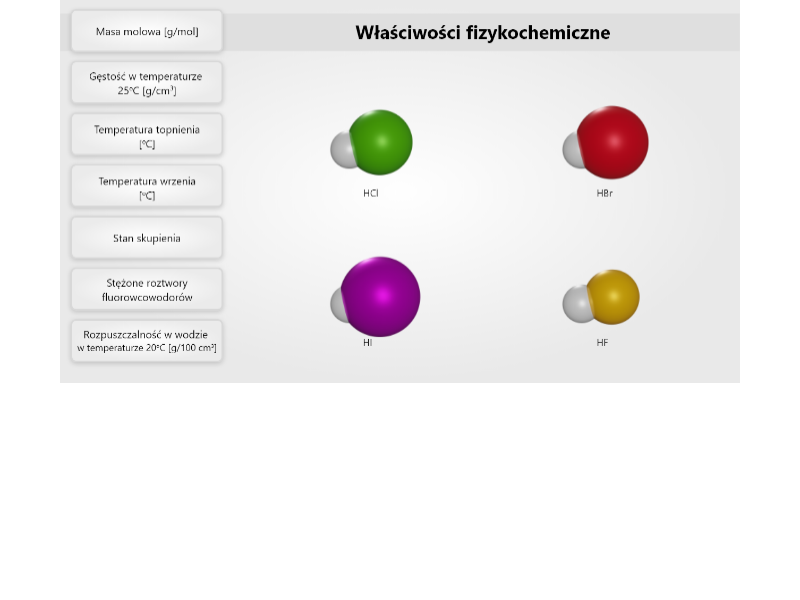
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5HSUC797
Przeanalizuj dane zawarte w symulacji i odpowiedz na poniższe pytanie.
W jaki sposób zmieniają się temperatury topnienia i wrzenia wodorków fluorowców, w zależności od położenia fluorowców w układzie okresowym?