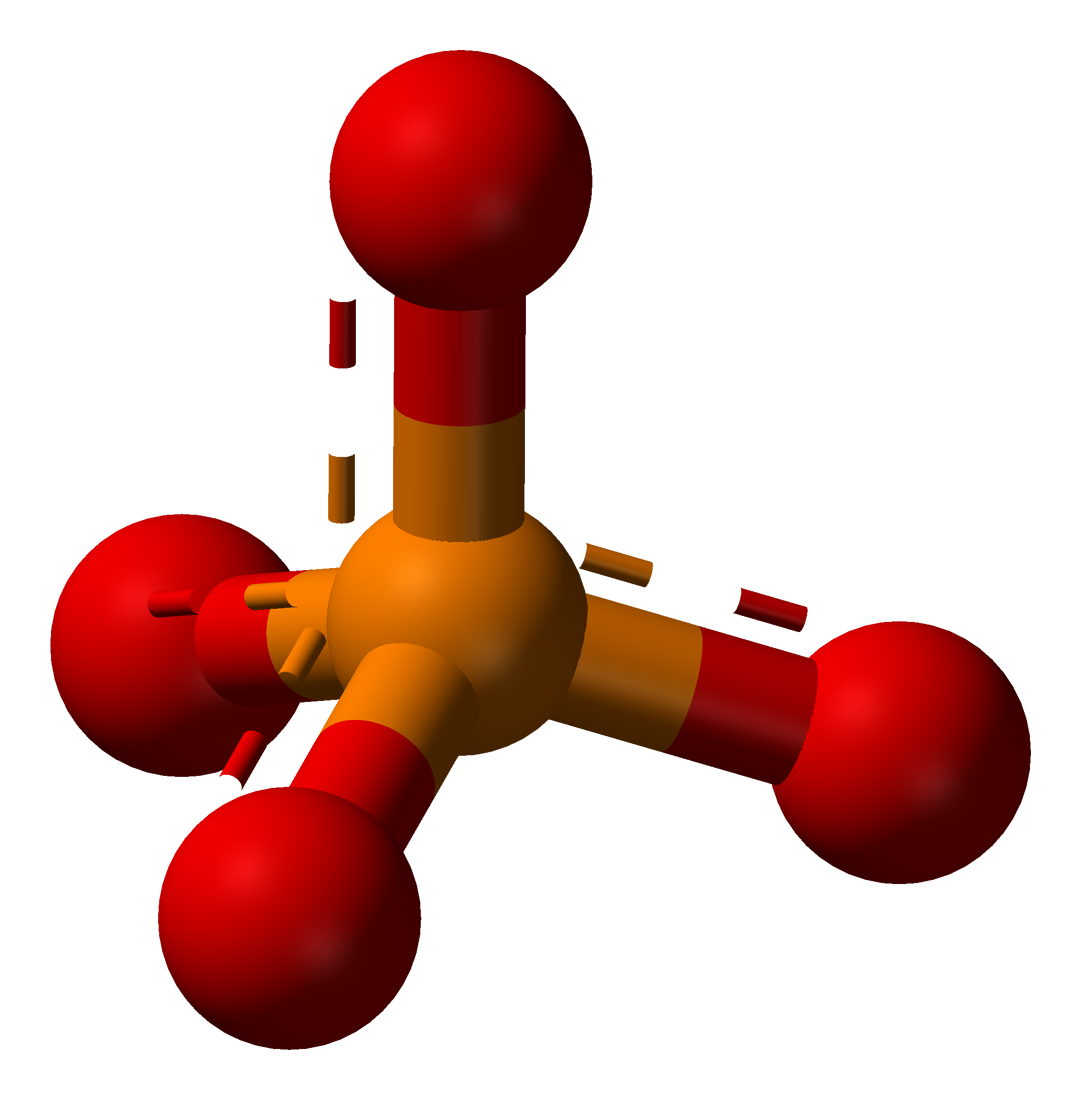
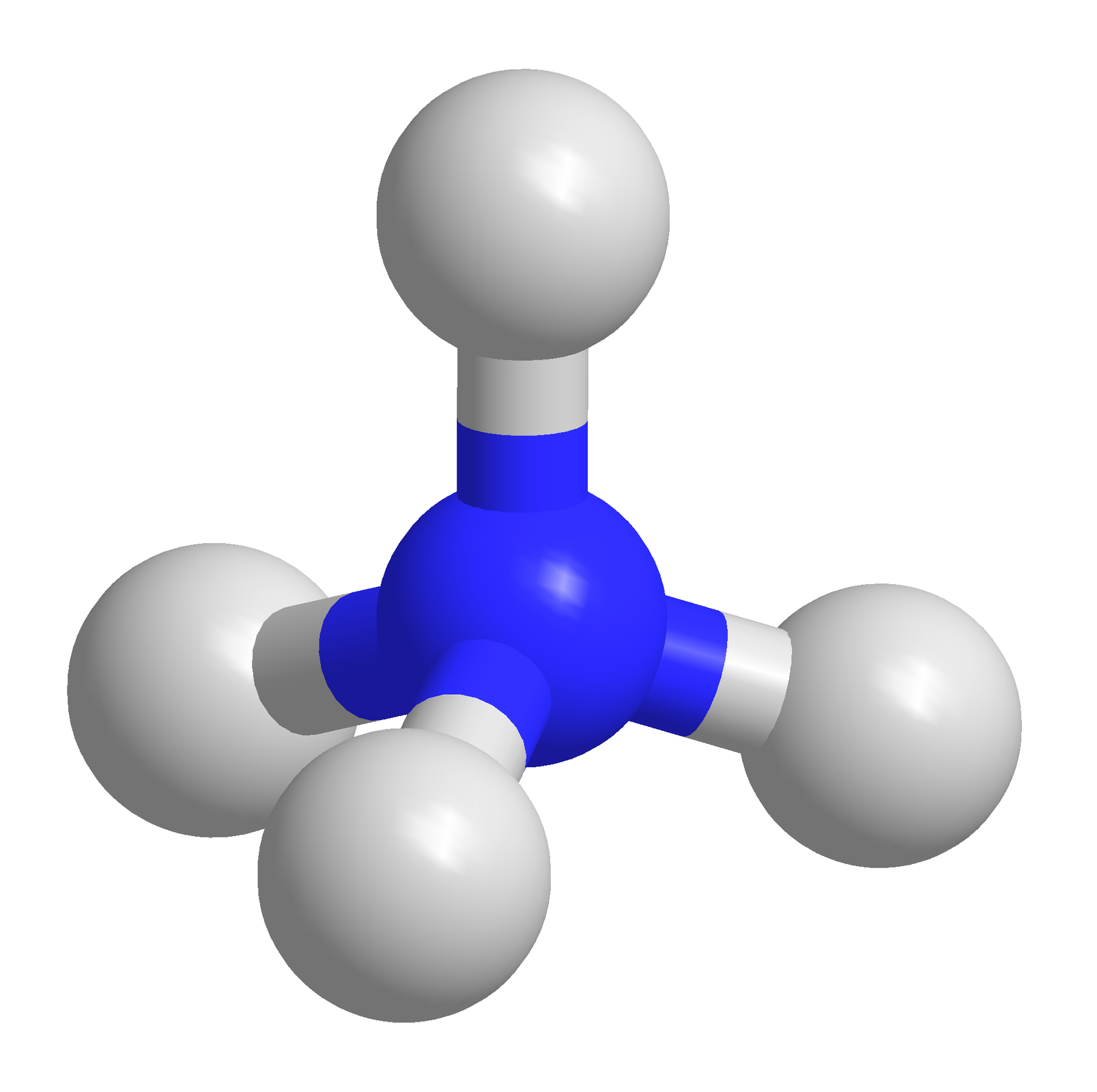
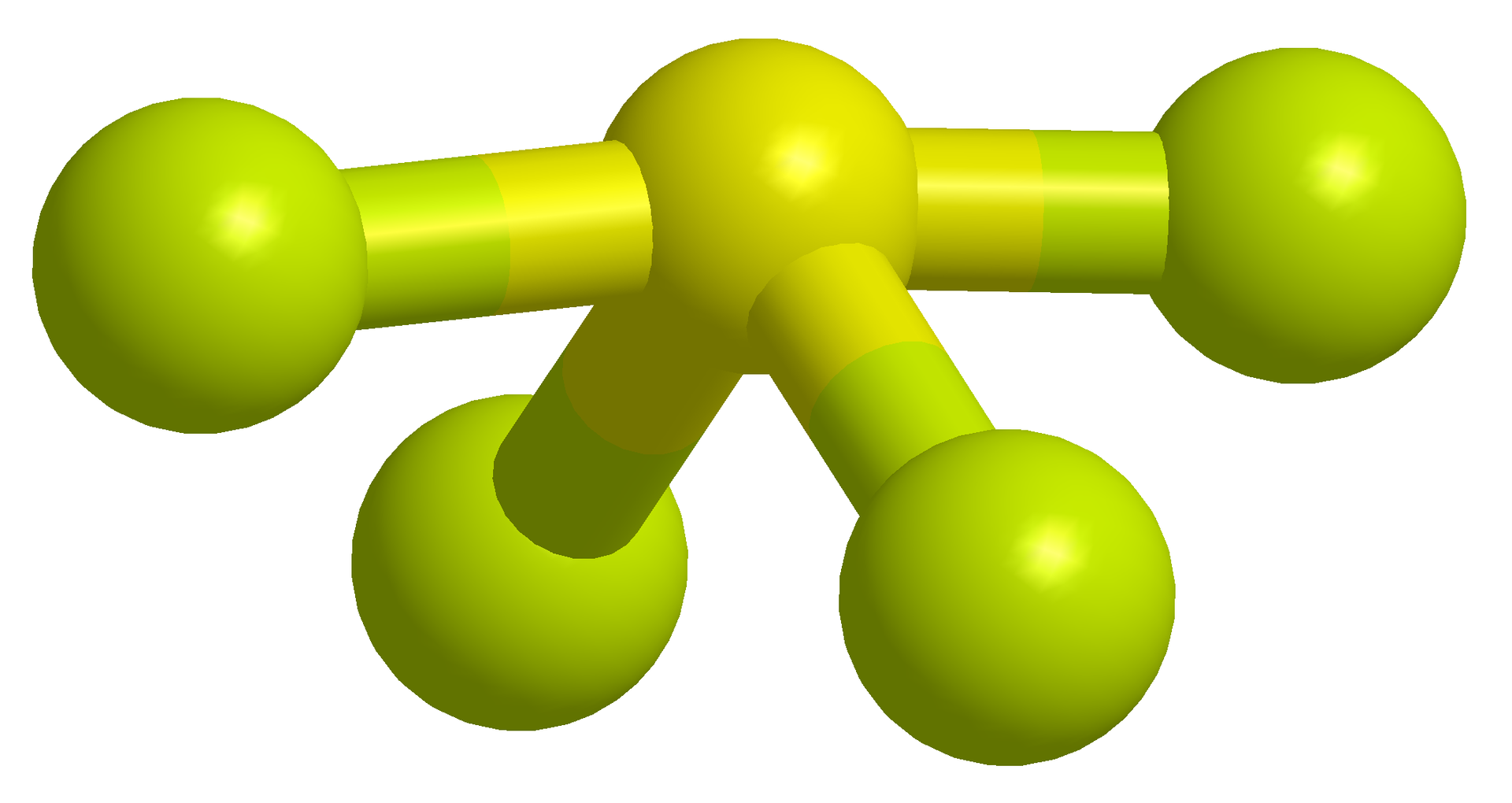
Czy można przewidzieć kształt cząsteczki?
Liczba przestrzenna a kształt
Metoda VSEPR jest jedną z dokładniejszych, a zarazem najprostszych metod przewidywania kształtu cząsteczek. W metodzie tej, typ hybrydyzacji oraz orientacja przestrzenna cząsteczki są ustalane na podstawie liczby przestrzennej ()iczby przestrzennej (), co w praktyce sprowadza się do obliczenia jej wartości na podstawie konkretnych wzorów.
Danej wartości można przyporządkować odpowiedni rodzaj hybrydyzacji, co jest podstawą do określenia geometrii cząsteczki. W tabeli poniżej znajdziesz zestawienie liczb przestrzennych oraz odpowiadające im typy hybrydyzacjihybrydyzacji.
Typ cząsteczki zapisano w postaci skrótu, gdzie:
– atom centralnyatom centralny,
– atom otaczający atom centralny,
– liczba wolnych par elektronowych na atomie centralnym.
Kształt cząsteczek lub jonów dla poszczególnych liczb przestrzennych
Jak ustalić kształt jonu lub cząsteczki, korzystając z metody VSEPR?
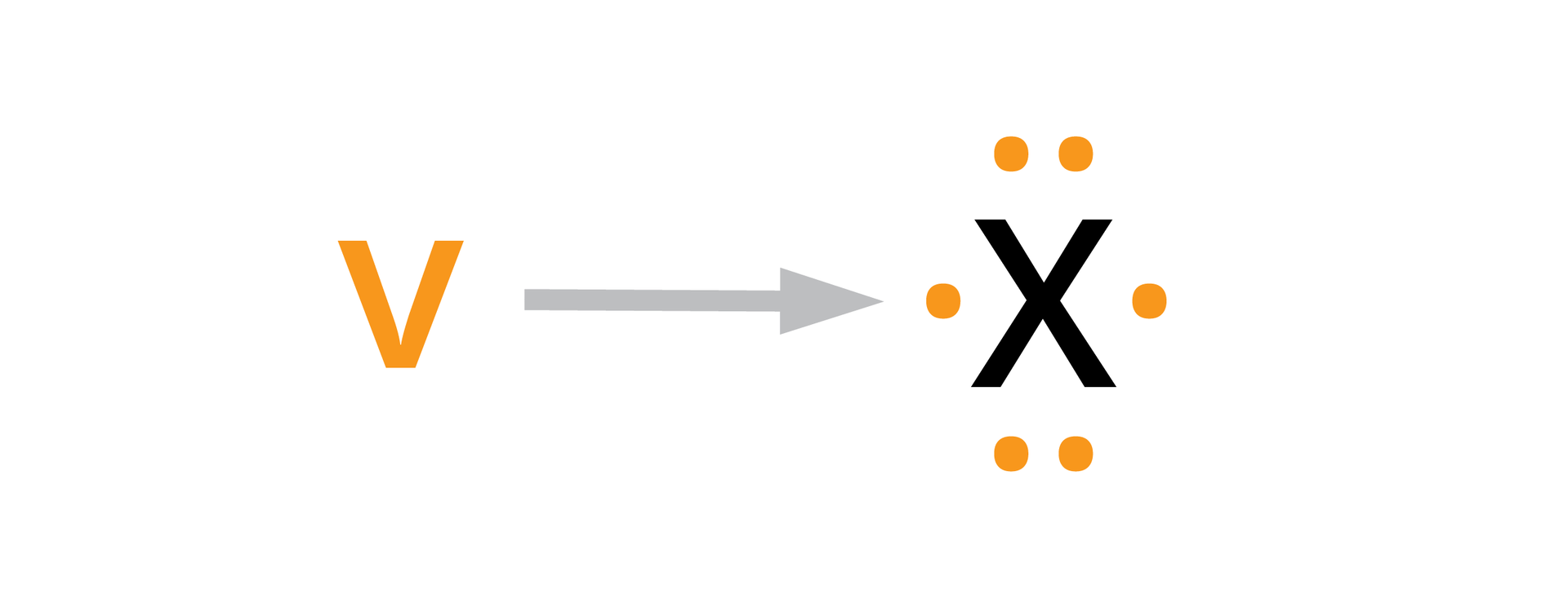
Przykład 1. Ustalanie kształtu cząsteczki obojętnej, np.
Przykład 2. Ustalanie kształtu jonu ujemnego, np.
Przykład 3. Ustalanie kształtu jonu dodatniego, np.
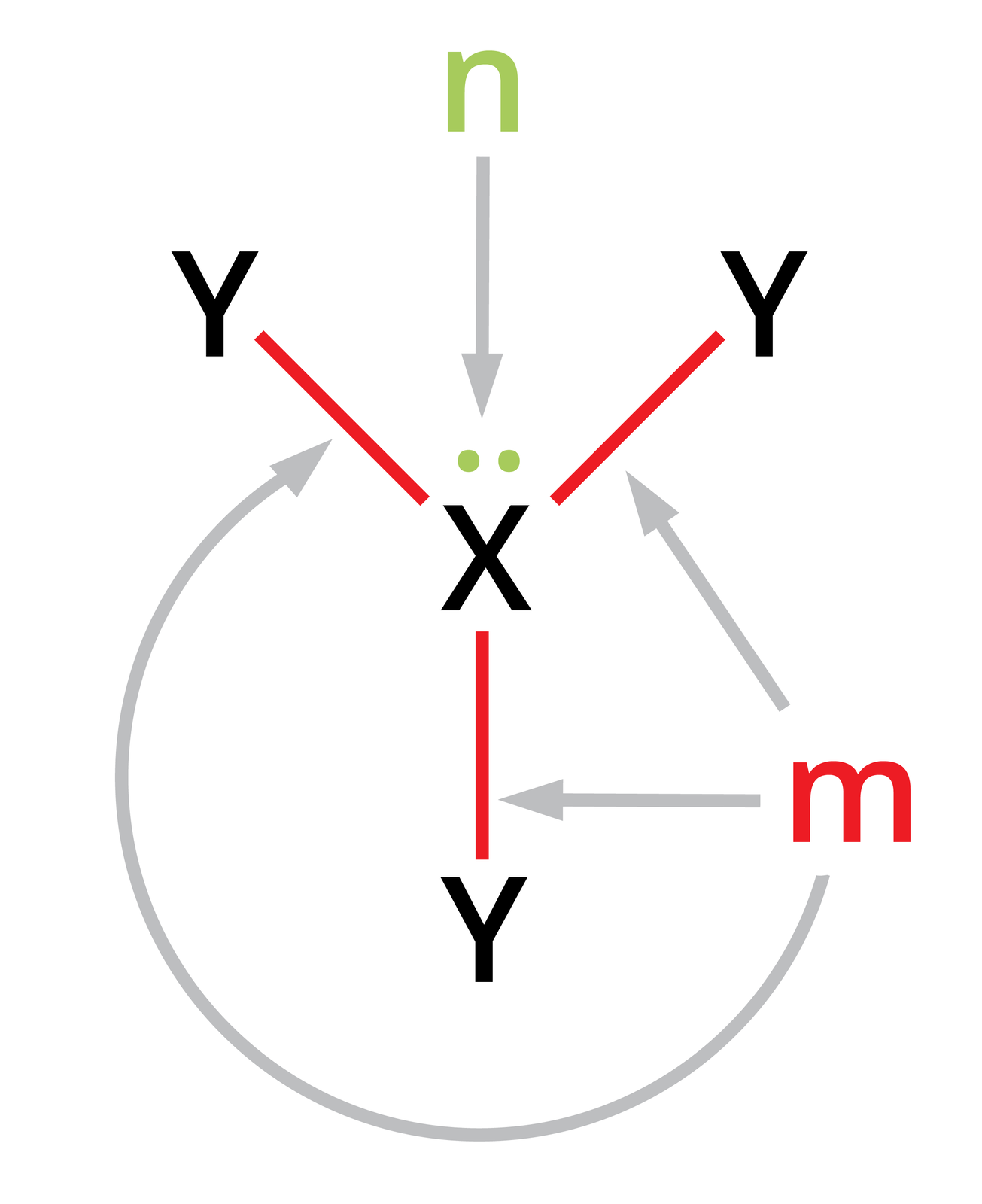
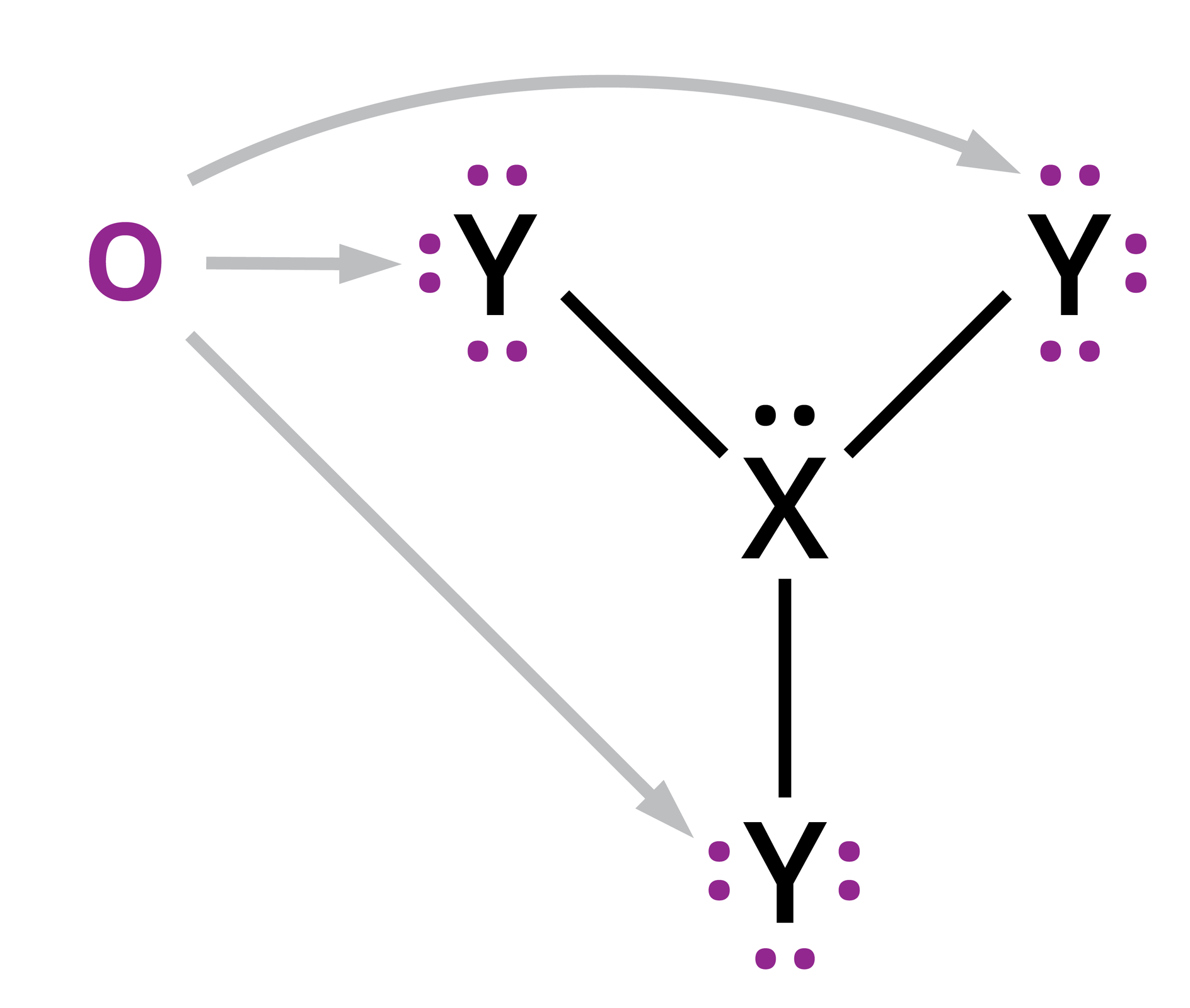
Przykład 4. Ustalenie kształtu cząsteczki na podstawie wzoru elektronowego, np.
Czy wiesz, jak za pomocą obliczeń matematycznych przewidzieć kształt cząsteczki? Aby poznać odpowiedź, zapoznaj się z filmem. Zapoznaj się z kształtami różnych cząsteczek, a następnie wykonaj ćwiczenia.

Film dostępny pod adresem /preview/resource/ROlp0HdrqT5l4
Nagranie filmowe wyjaśniające, jak przewidzieć kształt cząsteczki. Aby ustalić kształt cząsteczki, należy obliczyć jej liczbę przestrzenną lp.
Napisz, jaki kształt przewidujesz dla cząsteczki .
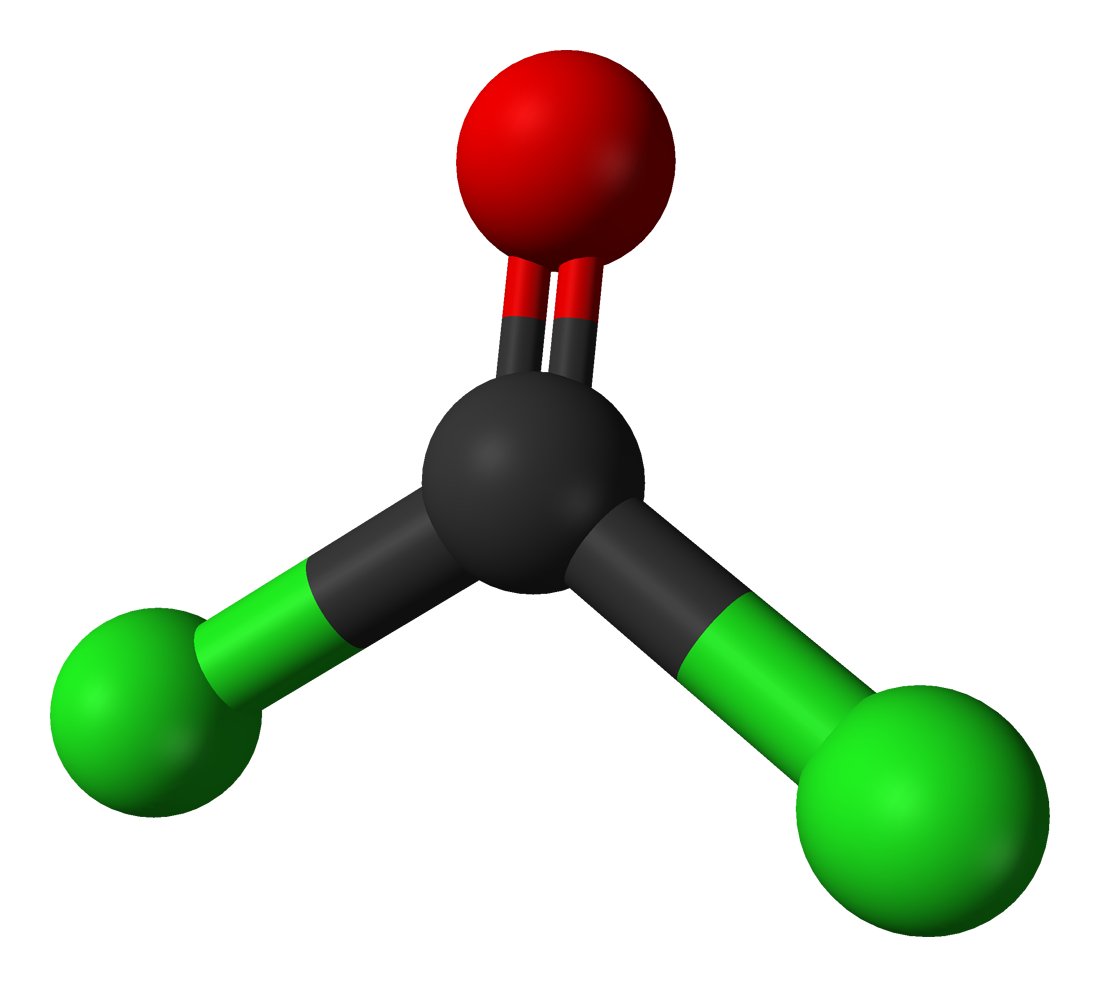
Stwórz model cząsteczki, w którym atom centralny, bez wolnych par elektronowych, łączy się z dwoma atomami za pomocą wiązań podwójnych. Jaki kąt występuje między wiązaniami w tej cząsteczce?
Zastanów się nad modelem cząsteczki, w którym atom centralny, bez wolnych par elektronowych, łączy się z dwoma atomami za pomocą wiązań podwójnych. Jaki kąt będzie występował między wiązaniami w tej cząsteczce?
Jaka jest różnica w strukturze pomiędzy bipiramidą trygonalną, a strukturą otrzymaną w wyniku utworzenia sześciu wiązań pomiędzy atomem centralnym a atomami otaczającymi atom centralny?
Zapoznaj się z poniższą grą edukacyjną, z pomocą której nauczysz się konstruować modele bazując na metodzie VSEPR.
Zasada działania: Na początku wybierz z listy atom główny i naciśnij przycisk „Dodaj”. Następnie, aby przyłączyć kolejne atomy, do wybranego przez Ciebie atomu głównego, ponownie wybierz je z listy, zaznacz jakim wiązaniem maja być one połączone i naciśnij przycisk „Dodaj”. Jeśli uznasz, że dodany przez Ciebie atom jest błędny wystarczy, że klikniesz na niego i wybierzesz przycisk „Usuń”. Pamiętaj, że każdy utworzony przez Ciebie model jest przestrzenny i możesz go dowolnie obracać, klikając na niego i przesuwając kursorem myszy.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DO1K15LMS
Sprawdź swoją wiedzę i odpowiedz na pytania.
Zaznacz, w jaki sposób należy zbudować model podanego związku chemicznego. Wybierz odpowiednią ilość oraz rodzaj atomów pierwiastka. Pamiętaj o wiązaniach łączących poszczególne atomy.
Narysuj model dowolnej cząsteczki o budowie tetraedrycznej.