Dysocjacja elektrolityczna kwasów
Teoria dysocjacji, opisana przez Svantego Arrheniusa, pozwoliła wyjaśnić wiele zjawisk chemicznych i fizycznych. W otrzymał Nagrodę Nobla za doniosłość swego odkrycia. Zbadajmy zatem, czy roztwory kwasów przewodzą prąd elektryczny i jaki ma to związek z ich budową.

przebieg procesu dysocjacji elektrolitycznej;
zjawisko przewodzenia prądu elektrycznego przez wodne roztwory wodorotlenków;
sposoby zapisywania procesu dysocjacji elektrolitycznej wodorotlenków oraz przedstawienie tego procesu za pomocą modeli.
badać przepływ prądu elektrycznego przez roztwory wodne kwasów;
wyjaśniać, dlaczego wodne roztwory kwasów przewodzą prąd elektryczny;
zapisywać równania dysocjacji elektrolitycznej kwasów beztlenowych i tlenowych.
1. Badanie przewodnictwa prądu elektrycznego przez kwasy
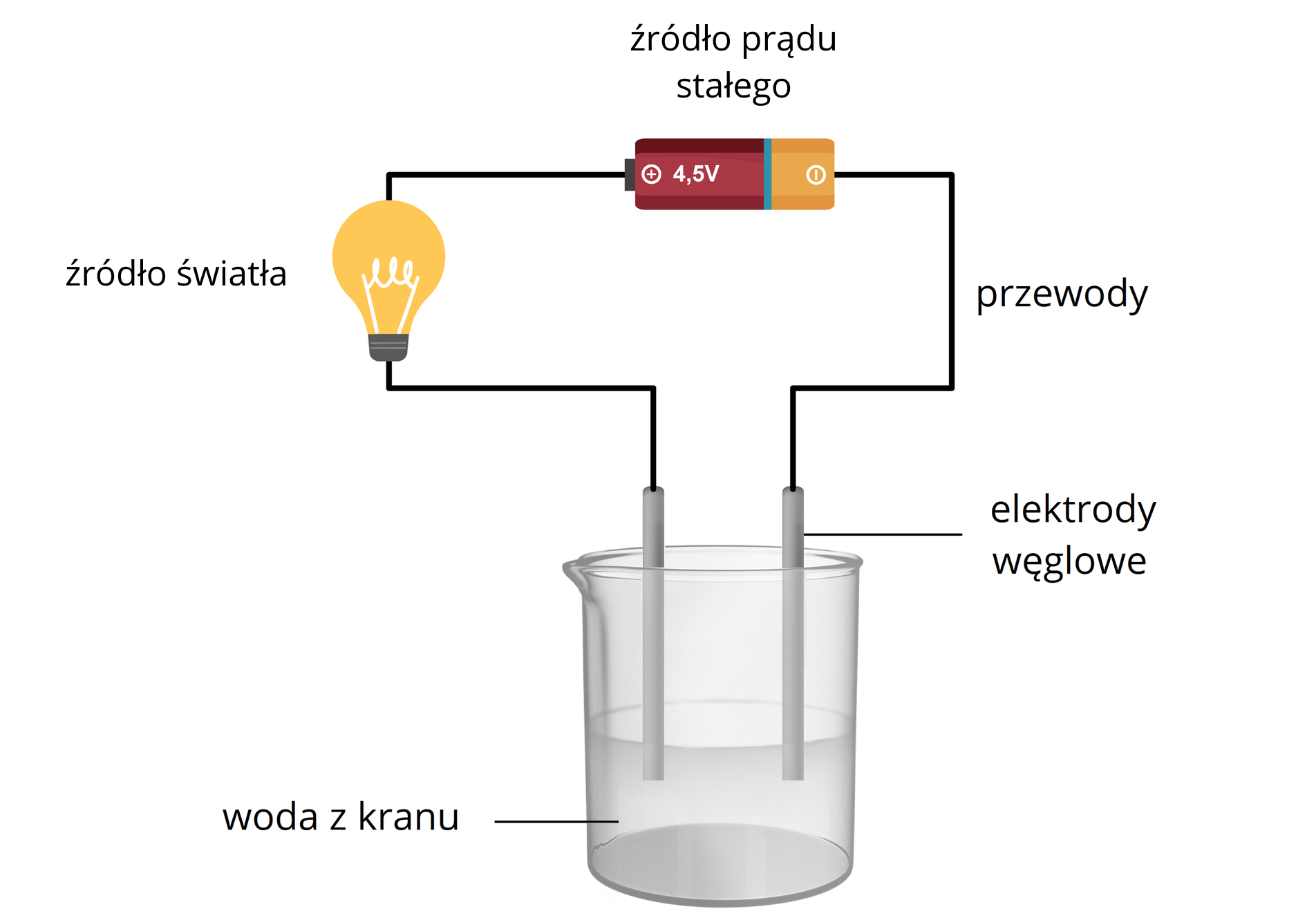
Czy woda kranowa i woda destylowana przewodzą prąd elektryczny? Wykonaj doświadczenie, budując obwód elektryczny.
Opisz przebieg doświadczenia z wykorzystaniem obwodu elektrycznego, który należałoby przeprowadzić w celu zbadania, czy woda kranowa przewodzi prąd elektryczny.
Zbadaj przewodzenie prądu elektrycznego przez wodę i roztwory wodne , i . Wstaw końcówki elektrod do przygotowanych roztworów, zamykając w ten sposób obwód elektryczny. Obserwuj, w których roztworach zaświeci się dioda LED.
Podsumowanie doświadczenia (symulacji)
Woda destylowana nie przewodzi prądu. Przez pozostałe roztwory przepływa prąd elektryczny, o czym świadczy świecenie diody LED. Roztwory wodne kwasów przewodzą prąd elektryczny – znajdują się w nich jony, które są nośnikami ładunku elektrycznego.
Cząsteczki wody są zdysocjowane w znikomej ilości, przez co możemy traktować wodę jako nieelektrolitnieelektrolit. KwasyKwasy przedstawione w symulacji są elektrolitamielektrolitami i przewodzą prąd elektryczny.
2. Dysocjacja elektrolityczna kwasów beztlenowych
Dysocjacja elektrolityczna chlorowodoru
W jaki sposób przebiega dysocjacja elektrolitycznadysocjacja elektrolityczna chlorowodoru? Obejrzyj film, a następnie rozwiąż zadanie zamieszczone w Poleceniu .

Film dostępny pod adresem /preview/resource/R5X1cEGlbJ8XS
Film pod tytułem Dysocjacja chlorowodoru
Niektóre cząsteczki, takie jak chlorowodór, ulegają w wodzie praktycznie całkowitej dysocjacji elektrolitycznej. Oznacza to, że w utworzonym roztworze kwasu chlorowodorowego nie występują cząsteczki , lecz jedynie jony. Takie elektrolity nazywamy mocnymi. Strzałka wskazuje na to, że proces dysocjacji przebiega jednokierunkowo. Należy przy tym pamiętać, że jon (kation wodoru) nie występuje samodzielnie w roztworze wodnym. W obecności cząsteczek , łączy się z nimi, tworząc jon hydroniowyjon hydroniowy (najprostszy jon oksoniowy) o wzorze . Dlatego równanie reakcji dysocjacji elektrolitycznej chlorowodoru ma następującą postać:
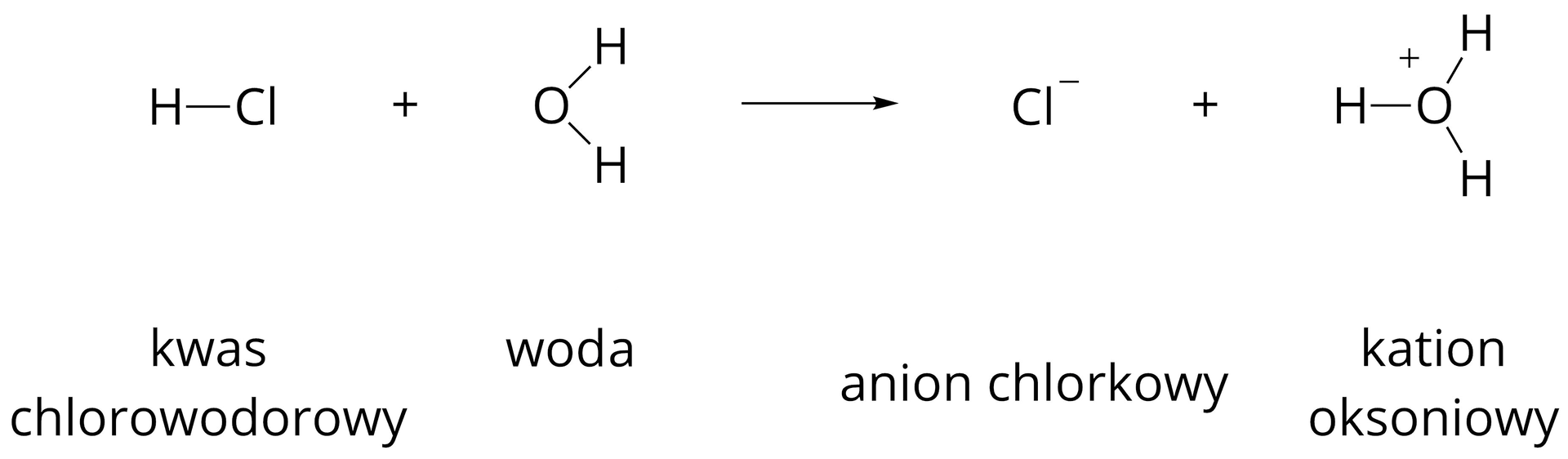
Często stosuje się jednak zapis uproszczony, w którym powstają kationy wodoru i aniony chlorkowe, zgodnie z następującym równaniem:
Cząsteczka wody składa się z dwóch atomów wodoru i jednego atomu tlenu. W wiązaniach kowalencyjnych spolaryzowanych, między atomem tlenu a atomem wodoru wiążąca para elektronowa jest przesunięta w stronę atomu tlenu. Zatem wokół atomów wodoru i tlenu gromadzą się cząstkowe ładunki. Wokół atomu wodoru – cząstkowy ładunek dodatni, a wokół atomu tlenu – cząstkowy ładunek ujemny. Taką cząsteczkę, w której po jednej stronie gromadzi się ładunek dodatni, a po drugiej ujemny, nazywamy dipolem elektrycznym. Tej właściwości woda zawdzięcza zdolność do rozpuszczania innych substancji, których cząsteczki również są dipolami.
W jaki sposób przebiega dysocjacja elektrolityczna siarkowodoru?
Cząsteczka siarkowodoru należy do słabych elektrolitów. Oznacza to, że w wodnym roztworze, obok jonów, występują również niezdysocjowane cząsteczki . W przypadku słabych wieloprotonowych elektrolitów, dochodzi do wielostopniowej dysocjacji elektrolitycznej.
W pierwszym etapie dysocjacji następuje oderwanie kationu wodoru od cząsteczki siarkowodoru. Powstaje zatem anion wodorosiarczkowy o wzorze . Jednocześnie kation wodoru łączy się z cząsteczką wody, tworząc kation oksoniowy (kation hydroniowy).
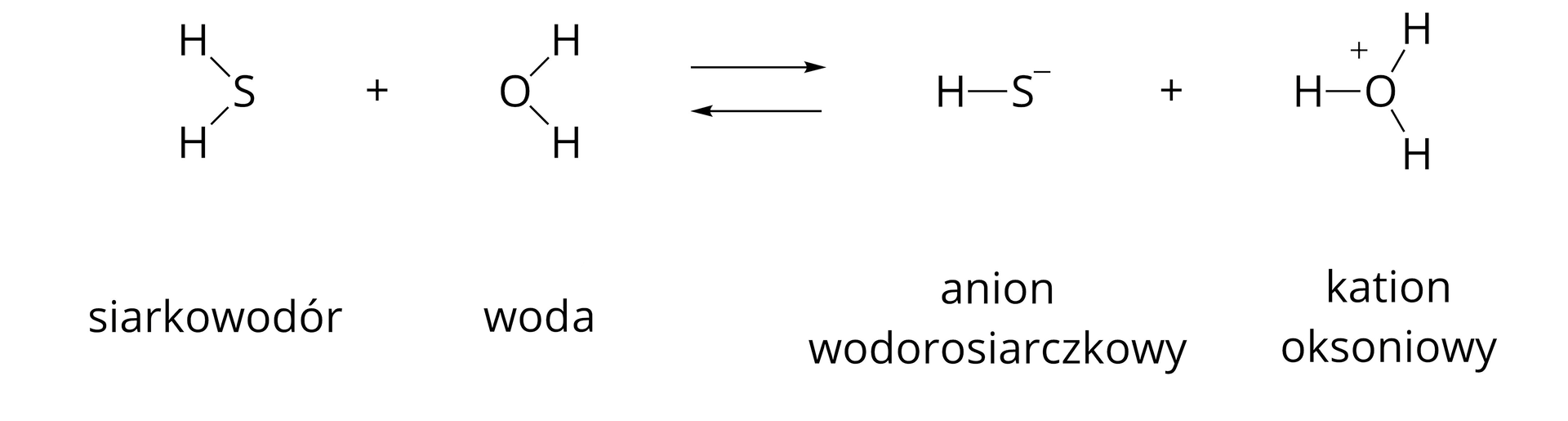
W drugim etapie dysocjacji następuje oderwanie kationu wodoru od anionu wodorosiarczkowego. Powstaje zatem anion siarczkowy o wzorze . Jednocześnie kation wodoru łączy się z cząsteczką wody tworząc jon oksoniowy (kation hydroniowy).
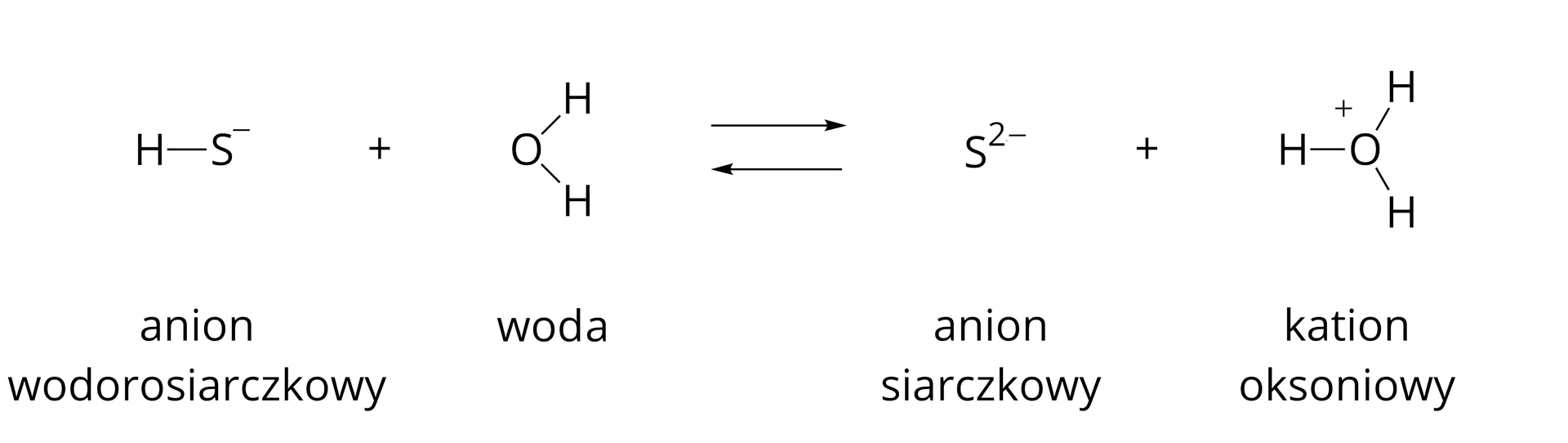
Dysocjacja elektrolityczna słabych elektrolitów jest procesem odwracalnym – cząsteczki rozpadają się na jony, które mogą się ponownie łączyć, tworząc cząsteczki. W roztworze wodnym powstałym poprzez rozpuszczenie w wodzie siarkowodoru występują więc jony , , , a także niezdysocjowane cząsteczki
(i ).
W przypadku takich kwasów, w równaniach reakcji dysocjacji elektrolitycznej stosuje się dwie strzałki skierowane w przeciwne strony.
Możemy również spotkać się z uproszczonym zapisem powyższych równań reakcji, w którym uwzględnia się kationy wodoru.
Pierwszy etap dysocjacji elektrolitycznej:
Drugi etap dysocjacji elektrolitycznej:
Które kwasy beztlenowe należą do mocnych, a które do słabych elektrolitów?
Kwasy beztlenowe | |
|---|---|
Mocne (dysocjują praktycznie całkowicie) | Słabe (ulegają częściowej dysocjacji) |
3. Dysocjacja elektrolityczna kwasów tlenowych
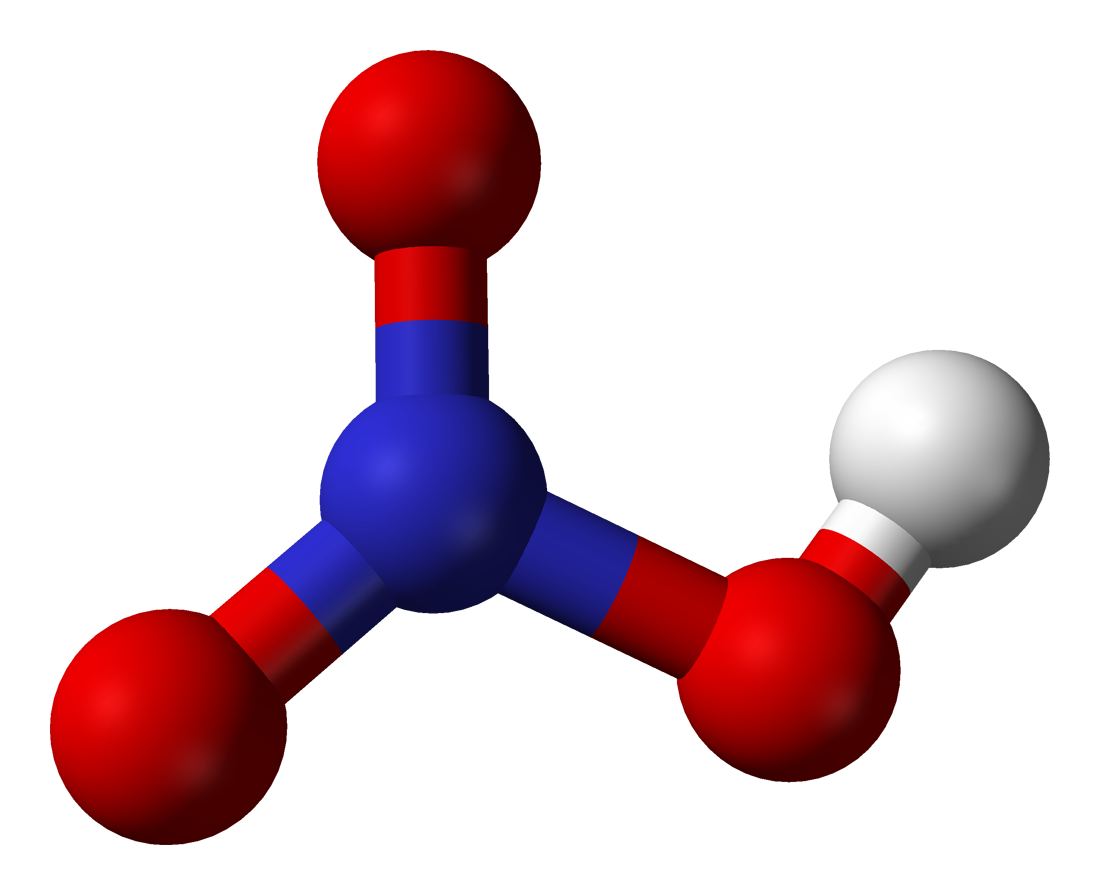
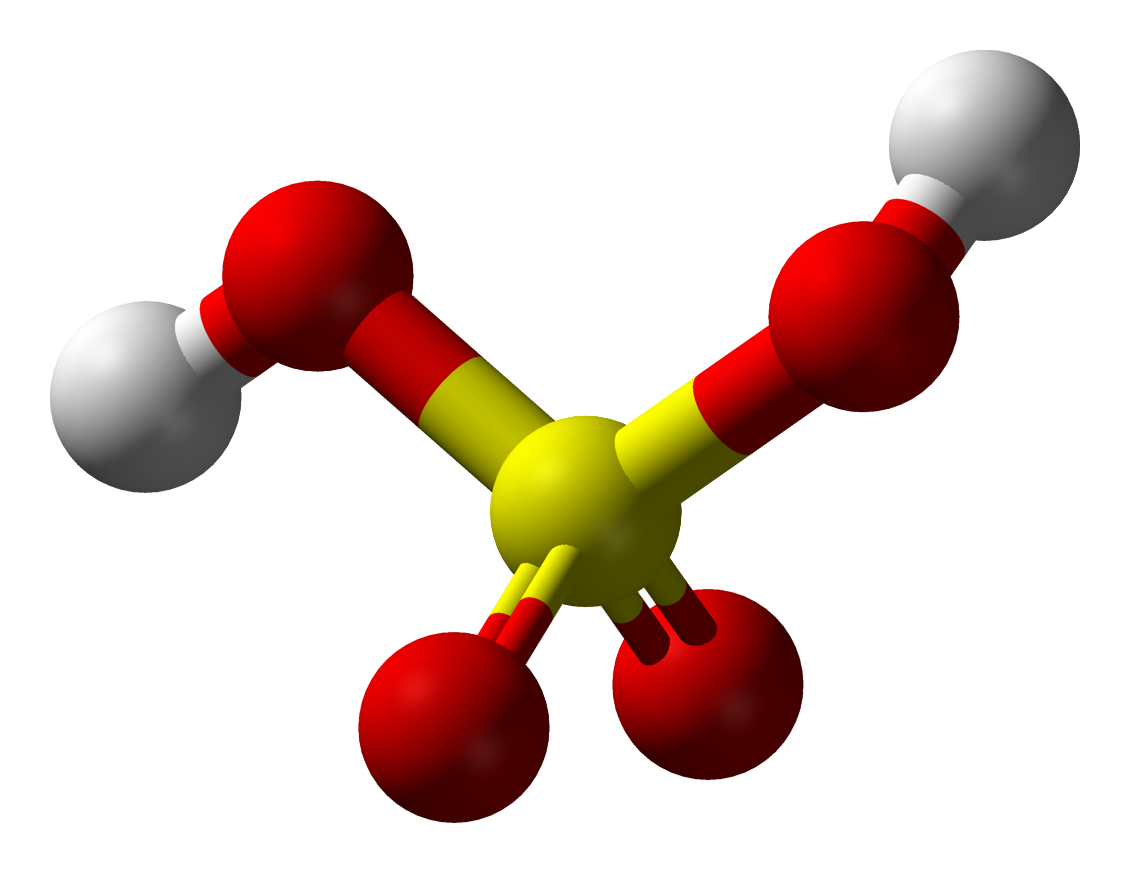
Wykonaj z plasteliny, patyczków lub za pomocą programu graficznego uproszczone modele, które przedstawiają cząsteczki kwasu azotowego i kwasu siarkowego. W obu policz liczbę atomów wodoru, zdolnych do dysocjacji. W ilu etapach będzie zachodził proces dysocjacji elektrolitycznej kwasu azotowego, a w ilu kwasu siarkowego?
W jaki sposób dysocjuje kwas azotowy?
Kwas azotowy ulega w wodzie praktycznie całkowitej dysocjacji. Oznacza to, że w utworzonym roztworze występują przede wszystkim jony. Kwas azotowy jest zatem mocnym elektrolitem. Podobnie jak w przypadku kwasów beztlenowych, należy pamiętać, że jon (kation wodoru) nie występuje samodzielnie w roztworze wodnym. W obecności cząsteczek , łączy się z nimi, tworząc jon hydroniowy (najprostrzy jon oksoniowy) o wzorze . Dlatego równanie procesu dysocjacji zapisujemy następująco:
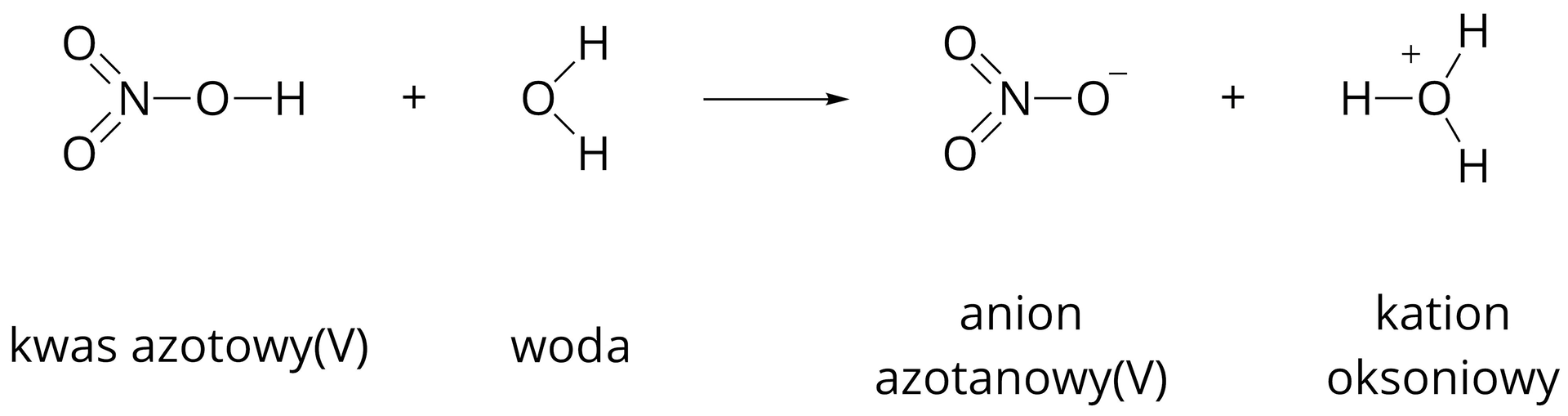
Często stosuje się jednak zapis uproszczony, w którym powstają kationy wodoru i aniony azotanowe, zgodnie z następującym równaniem:
W jaki sposób dysocjuje kwas
siarkowy()?
Kwas siarkowy() jest kwasem dwuprotonowym. Oznacza to, że posiada dwa atomy wodoru, zdolne do odszczepienia w procesie dysocjacji, czyli taki proces zachodzi w dwóch etapach. Kwas siarkowy() należy do mocnych elektrolitów, dlatego w roztworze wodnym obecne będą tylko jony, nie zaś cząsteczki . Pierwszy etap dysocjacji elektrolitycznej zapisujemy ze strzałką w jedną stronę, z kolei drugi etap ze strzałkami w obie strony.
W pierwszym etapie dysocjacji następuje oderwanie kationu wodoru od cząsteczki kwasu siarkowego(). Powstaje zatem anion wodorosiarczanowy() o wzorze . Jednocześnie kation wodoru łączy się z cząsteczką wody tworząc jon oksoniowy o wzorze .
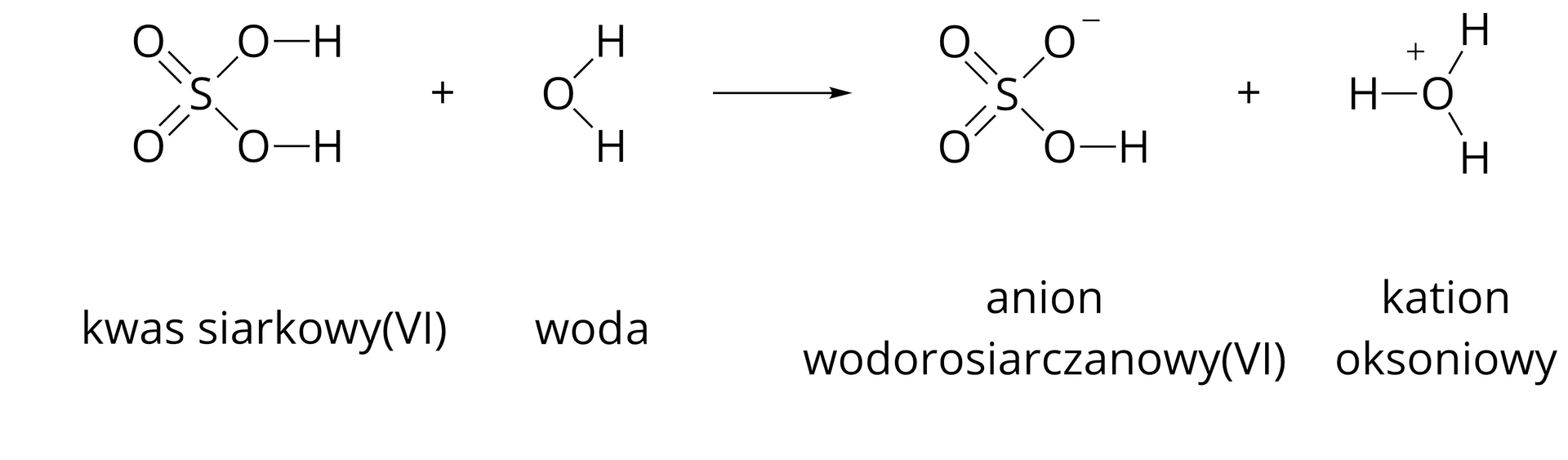
Zwróć uwagę, że strzałka wskazuje, że dysocjacja w tym etapie zachodzi praktycznie całkowicie i nieodwracalnie.
W drugim etapie dysocjacji następuje oderwanie kationu wodoru od anionu wodorosiarczanowego(). Powstaje dzięki temu anion siarczanowy() o wzorze . Jednocześnie kation wodoru łączy się z cząsteczką wody, dając tym samym jon oksoniowy .
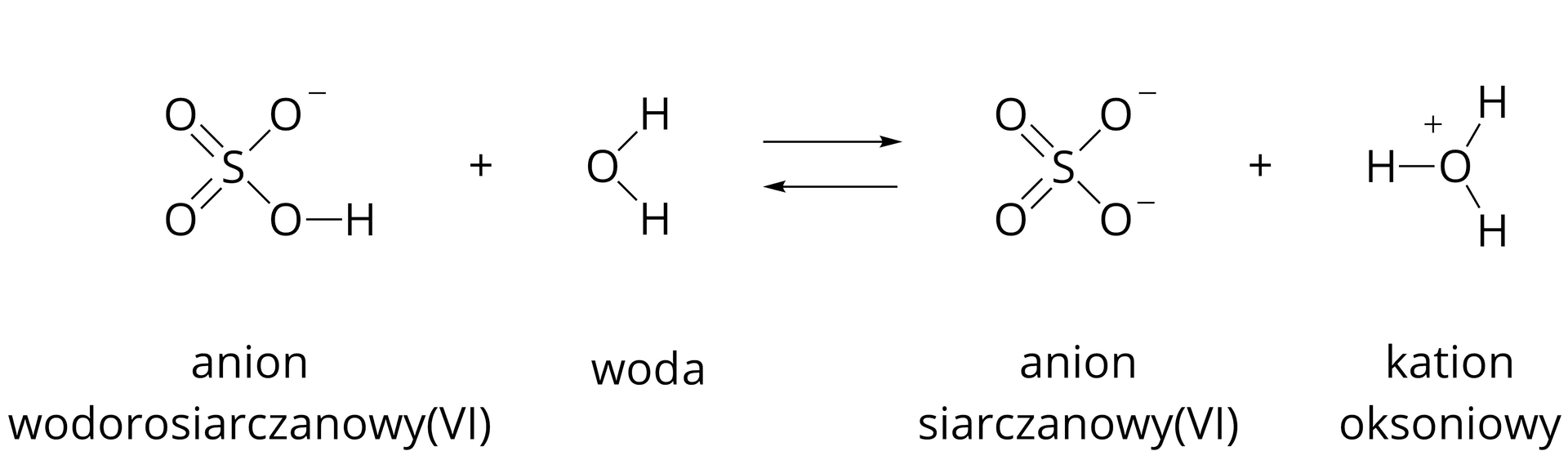
Ponieważ kwas siarkowy jest mocnym elektrolitem, to ulega całkowitej dysocjacji elektrolitycznej i w równaniu pierwszego jej etapu zapisujemy strzałkę skierowaną w jedną stronę. Oznacza to, że w roztworze kwasu siarkowego nie ma cząsteczek tego kwasu. Jednak powstające w pierwszym etapie aniony wodorosiarczanowe nie ulegają już całkowitej dysocjacji elektrolitycznej. Dlatego też w równaniu drugiego etapu dysocjacji zapisujemy strzałki w dwie strony, które wskazują na to, że w roztworze będą obecne zarówno wspomniane jony wodorosiarczanowe jak i jony siarczanowe.
Możemy również spotkać się z uproszczonym zapisem powyższych równań reakcji, gdzie uwzględnia się kationy wodoru.
Pierwszy etap dysocjacji elektrolitycznej:
Drugi etap dysocjacji elektrolitycznej:
Kwasy tlenowe dysocjują na jony oksoniowe (jony dodatnie) i aniony reszty kwasowej (jony ujemne), podobnie jak kwasy beztlenowe. Jeśli zachodzi taka konieczność, w nazwie anionu podajemy wartościowość niemetalu, charakterystyczną dla danego kwasu. Przeanalizuj zatem poniższą tabelę, a następnie wykonaj ćwiczenie.
Kwas | Anion kwasu |
|---|---|
węglowy | anion wodorowęglanowy |
anion węglanowy | |
siarkowy() | anion wodorosiarczanowy() |
anion siarczanowy() | |
siarkowy() | anion wodorosiarczanowy() |
anion siarczanowy() | |
fosforowy() | anion diwodorofosforanowy() |
anion wodorofosforanowy() | |
anion fosforanowy() |
1. , 2. , 3. , 4. , 5.
1. , 2. , 3. , 4. , 5. 1. , 2. , 3. , 4. , 5.
Które kwasy tlenowe należą do mocnych, a które do słabych elektrolitów?
Do porównywania mocy kwasów często stosuje się wielkość nazywaną stałą dysocjacji. Wielkość ta określana jest dla każdego etapu dysocjacji. Im większa jest jej wartość, tym mocniejszy jest kwas, a co za tym idzie w roztworze wodnym więcej jest jonów powstałych z jego dysocjacji. W poniższej tabeli uszeregowano wybrane kwasy tlenowe według malejącej mocy i podzielono je na kwasy mocne i słabe.
Podział kwasów ze względu na moc | |
|---|---|
Wzór sumaryczny kwasu | Stała dysocjacji kwasu () |
Kwasy mocne | |
| |
Kwasy słabe | |
| |
| |
| |
Jak możesz zauważyć, kwasy mocne, to takie których stała dysocjacji jest wyższa niż .
W poniższej tabeli zestawiono wartości stałej dysocjacji dla pierwszych etapów dysocjacji wybranych kwasów nieorganicznych. Zapoznaj się z informacjami zawartymi w tabeli, a następnie wykonaj polecenie.
Moc wybranych kwasów nieorganicznych | |
|---|---|
Wzór sumaryczny kwasu | Stała dysocjacji () |
Podsumowanie
Wodne roztwory kwasów przewodzą prąd elektryczny, ponieważ są w nich obecne jony oksoniowe (kationy hydroniowe) i aniony reszt kwasowych.
Jon oksoniowy ma zawsze ładunek jednododatni.
Nie wszystkie elektrolity w jednakowym stopniu rozpadają się na jony.
Mocne kwasy, takie jak kwasy chlorowodorowy czy kwas azotowy(), są całkowicie zdysocjowane.
W roztworach słabych kwasów, takich jak kwas siarkowodorowy czy kwas węglowy, znajdują się także cząsteczki niezdysocjowane.
Kwasy wieloprotonowe dysocjują wielostopniowo.
Opracuj w odpowiednim programie prezentację, która ilustruje proces dysocjacji elektrolitycznej kwasu siarkowego(), a następnie przedstaw ją nauczycielowi.
Opisz proces dysocjacji elektrolitycznej kwasu siarkowego().
Nagraj film z komentarzem, który wyjaśnia, na czym polega proces dysocjacji elektrolitycznej kwasów.
Wyjaśnij, na czym polega proces dysocjacji elektrolitycznej kwasów.
Słownik
rozkład cząsteczek substancji na jony (kationy i aniony) pod wpływem rozpuszczalnika, np. wody
substancja, której wodny roztwór przewodzi prąd elektryczny
; występujący w roztworach wodnych jednododatni jon, będący hydratowanym protonem
(wg teorii Arrheniusa) związki, które pod wpływem wody ulegają dysocjacji na kationy wodoru i aniony reszty kwasowej
substancja, której wodny roztwór nie przewodzi prądu elektrycznego
Ćwiczenia
Kwasy pod wpływem wody dysocjują na: Możliwe odpowiedzi: 1. kationy hydroniowe i aniony reszty kwasowej., 2. kationy wodoru i aniony wodorotlenkowe., 3. kationy wodoru i kationy metalu., 4. kationy niemetalu i aniony wodorotlenkowe., 5. kationy metalu i aniony wodorotlenkowe.
azotowego(pięć) i kwasu siarkowego(sześć), wybierając odpowiednie elementy spośród podanych. H N O indeks dolny, trzy, koniec indeksu dolnego, H indeks dolny, dwa, koniec indeksu dolnego, O powyżej, strzałka w prawoH1. indeks górny, trzy, plus, koniec indeksu górnego, 2. indeks górny, plus, koniec indeksu górnego, 3. indeks górny, dwa, minus, koniec indeksu górnego, 4. trzy, 5. indeks górny, minus, koniec indeksu górnego, 6. zero, 7. dwa, 8. cztery, 9. indeks górny, trzy, minus, koniec indeksu górnego, 10. indeks górny, minus, koniec indeksu górnego, 11. indeks górny, minus, koniec indeksu górnego, 12. indeks górny, plus, koniec indeksu górnego, 13. indeks górny, dwa, plus, koniec indeksu górnego, 14. indeks górny, plus, koniec indeksu górnego plus, N O indeks dolny, trzy, koniec indeksu dolnego1. indeks górny, trzy, plus, koniec indeksu górnego, 2. indeks górny, plus, koniec indeksu górnego, 3. indeks górny, dwa, minus, koniec indeksu górnego, 4. trzy, 5. indeks górny, minus, koniec indeksu górnego, 6. zero, 7. dwa, 8. cztery, 9. indeks górny, trzy, minus, koniec indeksu górnego, 10. indeks górny, minus, koniec indeksu górnego, 11. indeks górny, minus, koniec indeksu górnego, 12. indeks górny, plus, koniec indeksu górnego, 13. indeks górny, dwa, plus, koniec indeksu górnego, 14. indeks górny, plus, koniec indeksu górnego
H indeks dolny, dwa, koniec indeksu dolnego, S O indeks dolny, cztery, koniec indeksu dolnego, H indeks dolny, dwa, koniec indeksu dolnego, O powyżej, strzałka w prawo, H1. indeks górny, trzy, plus, koniec indeksu górnego, 2. indeks górny, plus, koniec indeksu górnego, 3. indeks górny, dwa, minus, koniec indeksu górnego, 4. trzy, 5. indeks górny, minus, koniec indeksu górnego, 6. zero, 7. dwa, 8. cztery, 9. indeks górny, trzy, minus, koniec indeksu górnego, 10. indeks górny, minus, koniec indeksu górnego, 11. indeks górny, minus, koniec indeksu górnego, 12. indeks górny, plus, koniec indeksu górnego, 13. indeks górny, dwa, plus, koniec indeksu górnego, 14. indeks górny, plus, koniec indeksu górnego plus, H S O indeks dolny, cztery, koniec indeksu dolnego1. indeks górny, trzy, plus, koniec indeksu górnego, 2. indeks górny, plus, koniec indeksu górnego, 3. indeks górny, dwa, minus, koniec indeksu górnego, 4. trzy, 5. indeks górny, minus, koniec indeksu górnego, 6. zero, 7. dwa, 8. cztery, 9. indeks górny, trzy, minus, koniec indeksu górnego, 10. indeks górny, minus, koniec indeksu górnego, 11. indeks górny, minus, koniec indeksu górnego, 12. indeks górny, plus, koniec indeksu górnego, 13. indeks górny, dwa, plus, koniec indeksu górnego, 14. indeks górny, plus, koniec indeksu górnego
H S O indeks dolny, cztery, koniec indeksu dolnego1. indeks górny, trzy, plus, koniec indeksu górnego, 2. indeks górny, plus, koniec indeksu górnego, 3. indeks górny, dwa, minus, koniec indeksu górnego, 4. trzy, 5. indeks górny, minus, koniec indeksu górnego, 6. zero, 7. dwa, 8. cztery, 9. indeks górny, trzy, minus, koniec indeksu górnego, 10. indeks górny, minus, koniec indeksu górnego, 11. indeks górny, minus, koniec indeksu górnego, 12. indeks górny, plus, koniec indeksu górnego, 13. indeks górny, dwa, plus, koniec indeksu górnego, 14. indeks górny, plus, koniec indeksu górnegoH indeks dolny, dwa, koniec indeksu dolnego, O powyżej strzałki równowagowe H1. indeks górny, trzy, plus, koniec indeksu górnego, 2. indeks górny, plus, koniec indeksu górnego, 3. indeks górny, dwa, minus, koniec indeksu górnego, 4. trzy, 5. indeks górny, minus, koniec indeksu górnego, 6. zero, 7. dwa, 8. cztery, 9. indeks górny, trzy, minus, koniec indeksu górnego, 10. indeks górny, minus, koniec indeksu górnego, 11. indeks górny, minus, koniec indeksu górnego, 12. indeks górny, plus, koniec indeksu górnego, 13. indeks górny, dwa, plus, koniec indeksu górnego, 14. indeks górny, plus, koniec indeksu górnego plus, S O indeks dolny, cztery, koniec indeksu dolnego1. indeks górny, trzy, plus, koniec indeksu górnego, 2. indeks górny, plus, koniec indeksu górnego, 3. indeks górny, dwa, minus, koniec indeksu górnego, 4. trzy, 5. indeks górny, minus, koniec indeksu górnego, 6. zero, 7. dwa, 8. cztery, 9. indeks górny, trzy, minus, koniec indeksu górnego, 10. indeks górny, minus, koniec indeksu górnego, 11. indeks górny, minus, koniec indeksu górnego, 12. indeks górny, plus, koniec indeksu górnego, 13. indeks górny, dwa, plus, koniec indeksu górnego, 14. indeks górny, plus, koniec indeksu górnego
W procesie dysocjacji elektrolitycznej związki chemiczne rozpadają się na kationy (jony obdarzone ładunkiem 1. ujemnym, 2. elektrolitami, 3. dodatnim, 4. przewodnikami, 5. nieelektrolitami, 6. rozpuszczalnikami, 7. obojętnym, 8. anionami, 9. dodatnim, 10. jonami, 11. kationami, 12. ujemnym ) i aniony (jony obdarzone ładunkiem 1. ujemnym, 2. elektrolitami, 3. dodatnim, 4. przewodnikami, 5. nieelektrolitami, 6. rozpuszczalnikami, 7. obojętnym, 8. anionami, 9. dodatnim, 10. jonami, 11. kationami, 12. ujemnym ).
Dokończ zdania, wybierając odpowiednie elementy z listy.
dodatnim, ujemnym, rozpuszczalnikami, obojętnym, dodatnim, elektrolitami, ujemnym, jonami, nieelektrolitami, anionami, kationami, przewodnikami
Związki chemiczne, które pod wpływem wody ulegają dysocjacji elektrolitycznej, nazywamy ...................................
W procesie dysocjacji elektrolitycznej związki chemiczne rozpadają się na jony: kationy (jony obdarzone ładunkiem .................................. ) i aniony (jony obdarzone ładunkiem .................................. ).
Przeprowadzono badanie przewodnictwa elektrycznego, zgodnie z poniższym schematem.
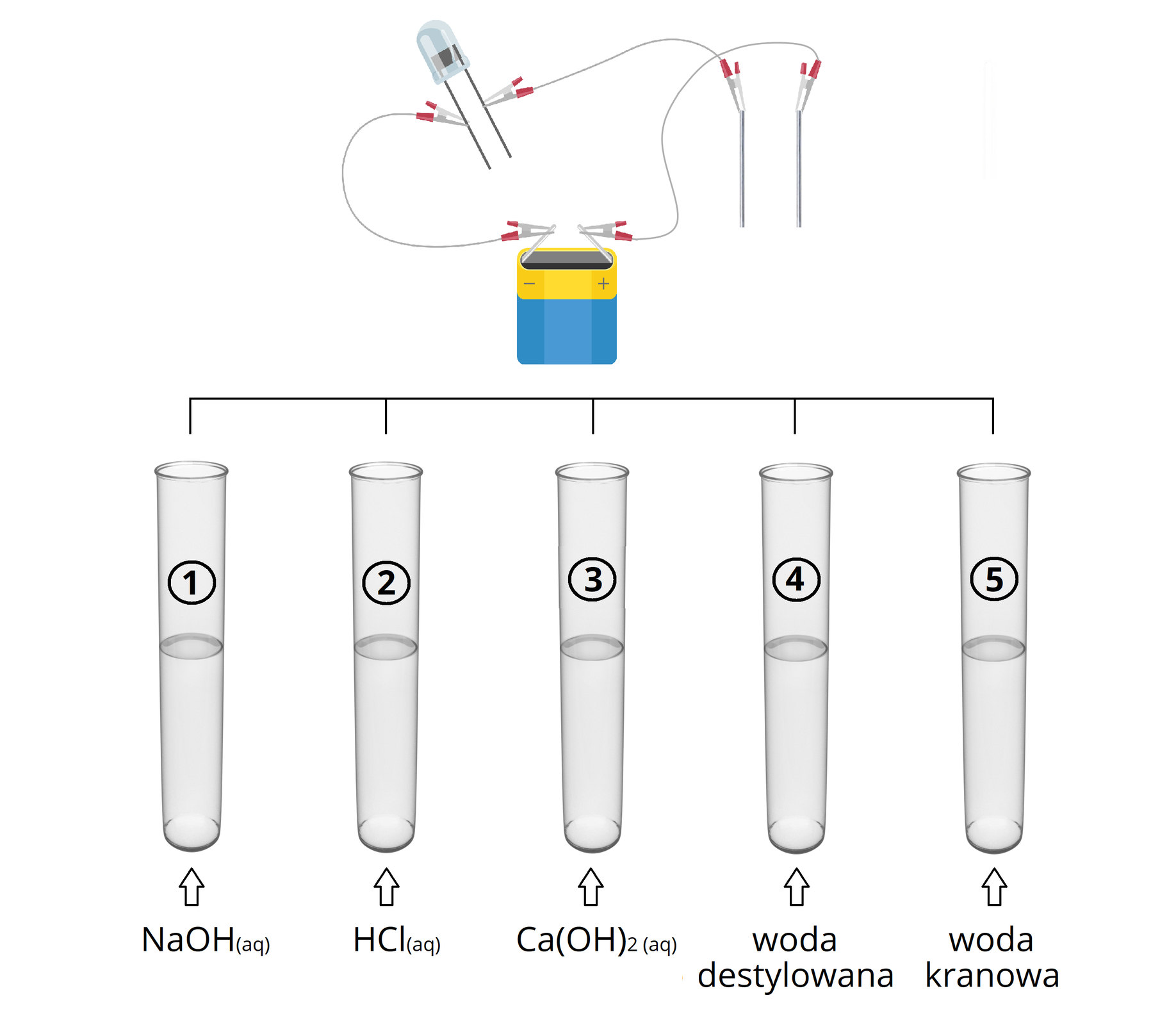
Przy pomocy obwodu elektrycznego, przeprowadzono badanie przewodnictwa elektrycznego pięciu różnych substancji:
;
;
;
wody destylowanej;
wody kranowej.
Który z podanych związków chemicznych nie przewodzi prądu elektrycznego?
- Woda destylowana.
- Zasada wapniowa.
- Kwas solny.
- Kwas siarkowy(VI).
- Kwas siarkowy(IV).
- Zasada sodowa.
Uzupełnij ogólny zapis równań, przeciągając odpowiednie elementy w luki.
zasad, , , , kwasów, , ,
Dysocjacja elektrolityczna ...............
.............. .............. ..............
Dysocjacja elektrolityczna zasad.
.............. ..............
Kwas fosforowy() jest kwasem wieloprotonowym, dlatego ulega wielostopniowej dysocjacji elektrolitycznej. Poszczególne etapy tej dysocjacji w formie uproszczonej można opisać następującymi równaniami reakcji:
Kwas fosforowy() jest kwasem wieloprotonowym, dlatego ulega wielostopniowej dysocjacji elektrolitycznej. Poszczególne etapy tej dysocjacji w formie uproszczonej można opisać następującymi równaniami reakcji:
, 2.
, 3.
- 1. carbonate ion, 2. hydroxide ion, 3. oxonium cation, 4. sulfate ion, 5. fluoride ion, 6. sulfite ion, 7. nitrate ion, 8. chloride ion
- 1. carbonate ion, 2. hydroxide ion, 3. oxonium cation, 4. sulfate ion, 5. fluoride ion, 6. sulfite ion, 7. nitrate ion, 8. chloride ion
- 1. carbonate ion, 2. hydroxide ion, 3. oxonium cation, 4. sulfate ion, 5. fluoride ion, 6. sulfite ion, 7. nitrate ion, 8. chloride ion
Bibliografia
Encyklopedia PWN
Bielański A., Podstawy Chemii Nieorganicznej, Warszawa 2008.
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy siódmej szkoły podstawowej, Warszawa 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy siódmej szkoły podstawowej, Mac Edukacja 2020.