Hydroliza cukrów złożonych
Hydroliza cukrów złożonych
Hydroliza cukrów złożonych stanowi kluczowy etap ich przemian chemicznych i biologicznych. Proces ten polega na rozkładzie polisacharydów oraz oligosacharydów do cukrów prostych przy udziale wody, często wspomaganej przez odpowiednie enzymy. Aby w pełni zrozumieć mechanizm hydrolizy, warto przypomnieć sobie sposób tworzenia wiązania glikozydowego – podstawowego połączenia łączącego poszczególne monocukry w większe struktury. Znajomość budowy tego wiązania pozwala lepiej wyjaśnić, dlaczego poszczególne cukry złożone różnią się podatnością na hydrolizę oraz jakie znaczenie ma ten proces w organizmach żywych. W celu badania hydrolizy cukrów złożonych i wykrywania produktów reakcji, można wykonać kilka doświadczeń chemicznych.
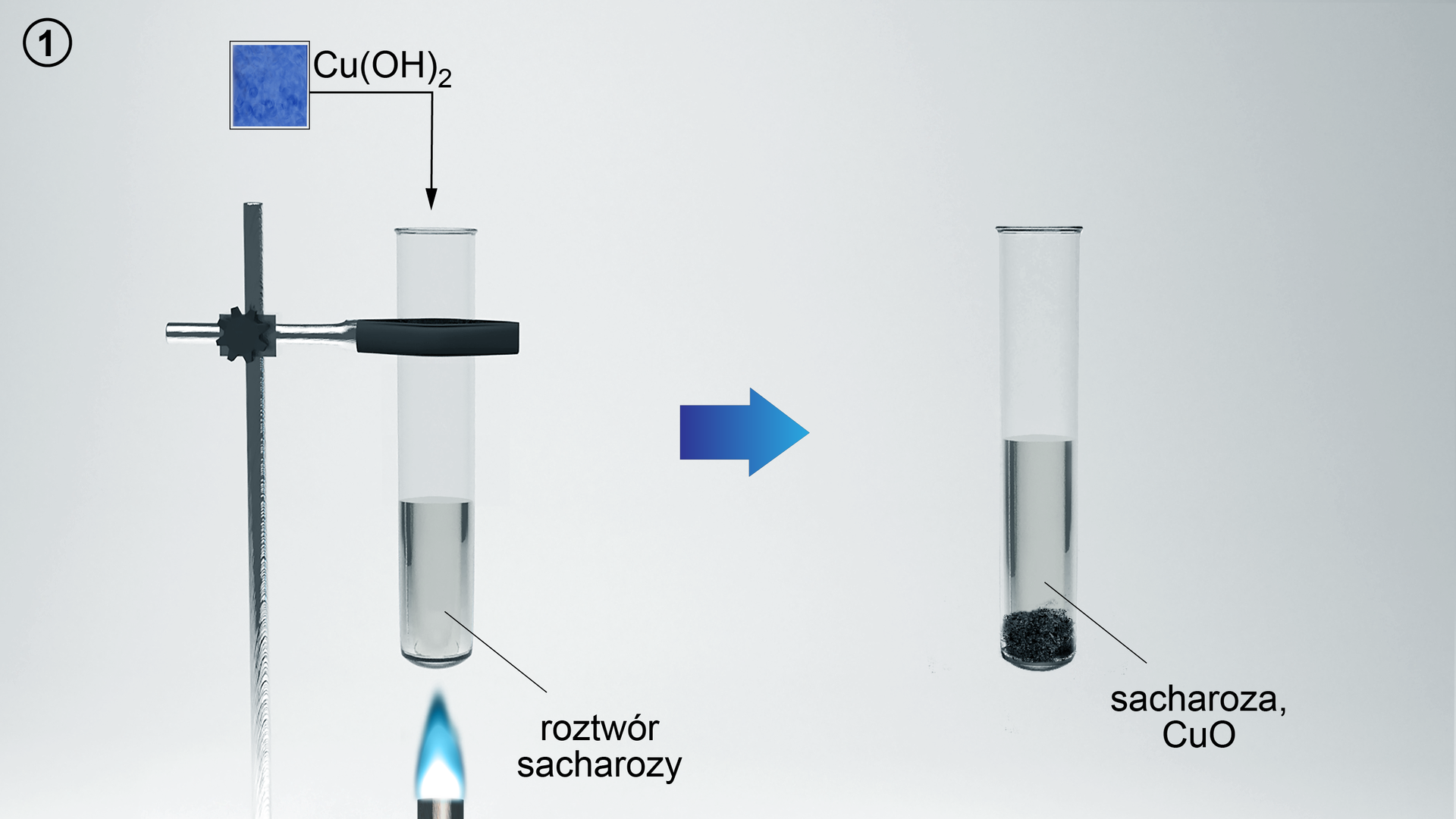
Hydroliza sacharozy
Schemat doświadczenia:
Równania reakcji chemicznych:


Badanie hydrolizy sacharozy oraz wykrywanie produktów reakcji – metoda polarymetryczna
Hydrolizę cukrów złożonych można badać za pomocą metody polarymetrycznej. Polega ona na pomiarze skręcalności właściwej w danego związku podczas jego hydrolizy. Do pomiaru stosuje się specjalne urządzenie – polarymetr.
Skręcalność właściwa sacharozy wynosi . Produktami hydrolizy sacharozy są glukoza i fruktoza. Taka mieszanina cukrów nazywana jest cukrem inwertowanym. Skręcalność właściwa takiej mieszaniny wynosi , co świadczy o tym, że w wyniku hydrolizy sacharozy doszło do zmiany skręcalności.
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Szafa laboratoryjna
Badanie procesu hydrolizy sacharozy
Zapoznaj się z opisem doświadczenia w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz wyniki, a następnie sformułuj wnioski oraz wykonaj poniższe ćwiczenia.
Analiza doświadczenia:
Badanie procesu hydrolizy sacharozy.
Problem badawczy:
Czy niskie środowiska powoduje hydrolizę sacharozy?
Hipoteza:
Sacharoza w kwasowym środowisku ulega hydrolizie.
Odczynniki chemiczne:
–procentowy roztwór sacharozy;
–procentowy roztwór kwasu chlorowodorowego;
–procentowy roztwór wodorotlenku sodu;
roztwór siarczanu() miedzi() o stężeniu
woda destylowana.
Sprzęt laboratoryjny:
dwie probówki – podłużne U–kształtne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
zlewka ( ) – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
trójnóg laboratoryjny;
palnik gazowy – urządzenie techniczne umożliwiające podtrzymywanie płomienia spalanego gazu w kontrolowany sposób;
zapałki – drewniane patyczki nasączone substancją ułatwiającą spalanie i zakończone substancją ulegającą zapłonowi, która obecna jest w tak zwanej główce zapałki;
papierki wskaźnikowe – kawałki bibuły nasączone substancją będącą indykatorem, a następnie wysuszone, które umożliwiają badanie odczynu roztworu;
zlewka ( ) – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
pipeta Pasteura – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości służące do odmierzania cieczy;
waga laboratoryjna – urządzenie do odmierzania masy substancji chemicznych.
Przebieg doświadczenia:
Przygotowano łaźnię wodną: a) włączono palnik; b) umieszczono nad nim trójnóg; c) postawiono na trójnogu zlewkę wypełnioną wodą.
Sporządzono w zlewce roztwór sacharozy i wlano do probówki.
Dodano do probówki kilka kropli roztworu kwasu chlorowodorowego i ogrzano w łaźni wodnej.
Sprawdzono odczyn roztworu za pomocą papierka wskaźnikowego.
Następnie dodano kilka kropli roztworu wodorotlenku sodu w celu zneutralizowania roztworu.
Sprawdzono odczyn roztworu za pomocą papierka wskaźnikowego.
Do innej suchej probówki dodano roztworu wodorotlenku sodu oraz kilka kropli roztworu siarczanu() miedzi().
Następnie do probówki z powstałym roztworem wlano roztworu sacharozy po dodaniu kwasu.
Probówkę włożono do gorącej łaźni wodnej i obserwowano zmiany.
Obserwacje:
Po dodaniu roztworu kwasu do roztworu sacharozy, papierek wskaźnikowy zmienił kolor na pomarańczowoczerwony. Po zneutralizowaniu roztworu i wykonaniu testu z wodorotlenkiem miedzi(), niebieski, galaretowaty osad zmienił zabarwienie na ceglastoczerwone.
Poniższa symulacja przedstawia pomiar skręcalności właściwej. Mając kilka przykładowych roztworów, przeprowadź dla nich pomiary, a następnie rozwiąż poniższe zadania.
Zapoznaj się z opisem symulacji przedstawiającej pomiar skręcalności właściwej, a następnie rozwiąż zadania.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D2M5TPN4M
Maltoza zbudowana jest z: Możliwe odpowiedzi: 1. cząsteczek D‑fruktozy i D‑glukozy., 2. cząsteczek D‑fruktozy., 3. cząsteczek D‑glukozy.
Podaj wartość skręcalności właściwej sacharozy.
Podaj obserwacje oraz wnioski wyciągnięte po wykonaniu symulacji interaktywnej.
Podaj obserwacje oraz wnioski wyciągnięte po zapoznaniu się z opisem symulacji interaktywnej.
Hydroliza skrobi
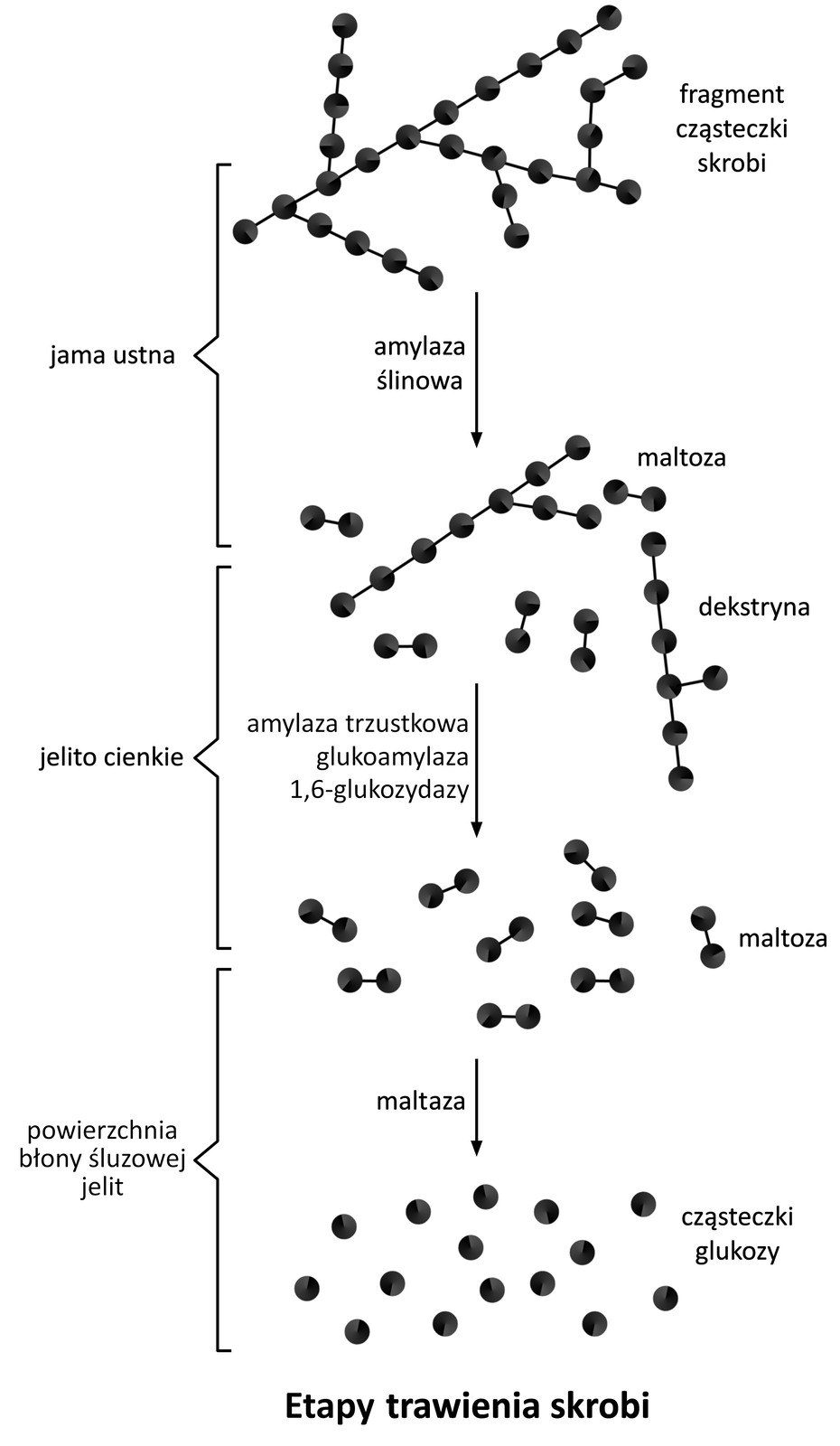
W pierwszym etapie skrobia ulega hydrolizie pod wpływem kwasu chlorowodorowego lub w obecności enzymu – ptialiny, czyli amylazy ślinowej. Wynikiem tej reakcji jest powstanie cząsteczek dekstryn oraz maltozy (). W ludzkim organizmie etap ten zachodzi w jamie ustnej.
Kolejnym etapem jest hydroliza dekstryn do maltozy pod wpływem kwasu chlorowodorowego lub zespołu enzymów: amylazy trzustkowej, glukoamylazy i -. Ostatnim etapem jest hydroliza powstałego dwucukru - maltozy, do D‑glukozy. Reakcja ta może zajść pod wpływem kwasu chlorowodorowego lub maltazy.
W uproszczeniu, równanie reakcji hydrolizy skrobi można zapisać następująco:
Hydroliza celulozy
Celuloza ulega hydrolizie pod wpływem kwasów lub w obecności enzymów – celulaz oraz celobiazy. Hydroliza celulozy zachodzi w dwóch etapach: najpierw jako produkt pośredni powstaje celobioza, a następnie powstaje produkt końcowy – glukoza. Poniżej przedstawiono schemat reakcji hydrolizy skrobi:
W uproszczeniu, równanie reakcji hydrolizy skrobi można zapisać następująco:
W jaki sposób przebiega proces hydrolizy polisacharydów? Na przykładzie skrobi i celulozy przeanalizuj podaną reakcję, a następnie rozwiąż podane poniżej zadania.
W jaki sposób przebiega proces hydrolizy polisacharydów? Na przykładzie skrobi i celulozy przeanalizuj opis podanej reakcji, a następnie rozwiąż podane poniżej zadania.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D2M5TPN4M
Produktem końcowym hydrolizy polisacharydów jest: Możliwe odpowiedzi: 1. maltoza., 2. fruktoza., 3. glukoza., 4. galaktoza.
Polisacharydy ulegają hydrolizie w środowisku: Możliwe odpowiedzi: 1. kwasowym., 2. zasadowym., 3. obojętnym.