Jaką rolę w atomie odgrywają elektrony?
Elektrony poruszają się wokół jądra atomowego, niektóre elektrony znajdują się bliżej, a inne dalej od niego. Oznacza to, że zajmują określone pozycje – poziomy energetyczne. Jednak w porównaniu do planet, nie jesteśmy w stanie określić jednocześnie ich dokładnego położenia i pędu. Elektrony podlegają prawom mechaniki kwantowej (działu fizyki teoretycznej), podczas gdy my na co dzień obserwujemy następstwa fizyki klasycznej. W tym materiale dowiesz się, jakie poziomy energetyczne zajmują elektrony, krążąc wokół jądra atomowego, i w jaki sposób zapisujemy je dla różnych atomów pierwiastka chemicznego.
Jak rozmieszczone są elektrony w atomie?
Rozmieszczenie elektronów na poszczególnych powłokach nazywa się konfiguracją elektronową.
Konfiguracje elektronowe atomów możemy zapisać na różne sposoby. Do najbardziej podstawowych należy zapis graficzny oraz zapis powłokowy. Na przykład konfigurację elektronową atomu sodu możemy zapisać następująco:
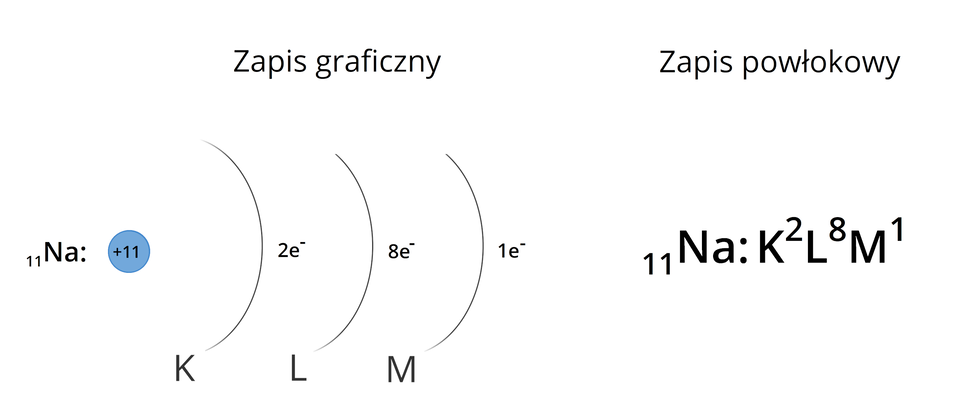
Zapisy te pokazują wyłącznie, ile elektronów mieści się na konkretnej powłoce elektronowej, a nie sposób, w jaki są one na niej rozmieszczone. Musimy bowiem pamiętać, że w obrębie powłok istnieją również podpowłoki, a w obrębie podpowłok – przestrzenie orbitalne, zwane poziomami orbitalnymi. Dlatego wprowadzony został podpowłokowy zapis konfiguracji elektronowej atomów, aby uwzględnić rodzaje podpowłok oraz orbitalny (klatkowy) zapis konfiguracji elektronowej. Dzięki temu możemy określić sposób rozmieszczenia elektronów na poszczególnych poziomach orbitalnych. Poniższe rozważania opierają się na konfiguracjach elektronowych atomów w stanie podstawowym, czyli o najmniejszej możliwej energii.
Przedstawienie konfiguracji elektronowej atomu rozpoczniemy od atomu helu, który ma dwa elektrony. Mogą one przebywać na pierwszej powłoce K. Tę informację możemy zaprezentować na kilka sposobów, więc przedstawiono je w tabeli.
Sposób zapisu konfiguracji elektronowej | Ogólne zasady zapisu konfiguracji elektronowej wybranym sposobem | Konfiguracja elektronowa |
|---|---|---|
Zapis z użyciem nawiasów kwadratowych | W nawiasie kwadratowym wymieniamy kolejno liczby elektronów, które znajdują się na powłokach: pierwszej, drugiej i kolejnych. Liczby te oddzielamy przecinkami. | |
Zapis z użyciem symboli powłok | Podajemy symbole zajętych przez elektrony powłok. Z prawej strony każdego symbolu, w indeksie górnym, zapisujemy liczbę elektronów, które znajdują się na powłoce. | KIndeks górny 22 |
Zapis w postaci schematu | Na schemacie modelu atomu zaznaczamy ładunek jądra równy liczbie protonów. Rysujemy powłoki elektronowe jako półokręgi, podpisujemy je ich symbolami. Następnie zaznaczamy ilość elektronów na poszczególnych powłokach. | 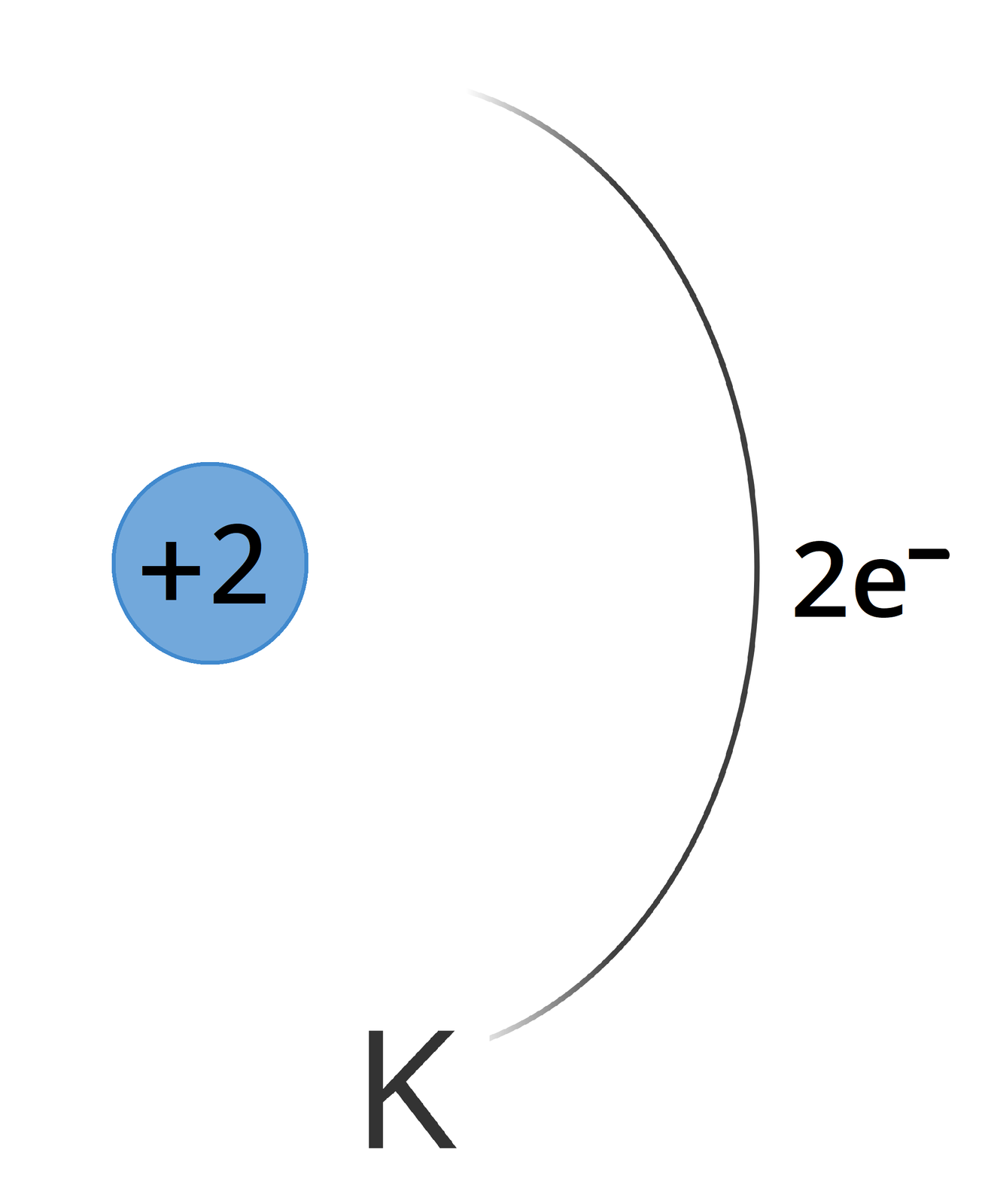 Hel Źródło: GroMar Sp. z o. o., licencja: CC BY-SA 3.0. |

Film dostępny pod adresem /preview/resource/R1cRdnklls0cI
W filmie określono liczbę elektronów w atomie tlenu oraz ukazano rozmieszczenie elektronów na poszczególnych powłokach. Konfigurację tę przedstawiono także przy użyciu symboli powłok oraz wykorzystując zapis w nawiasach kwadratowych.
Konfiguracja elektronowa atomu krzemu
Zapis z użyciem nawiasów kwadratowych:
Zapis z użyciem symboli powłok:
KIndeks górny 22LIndeks górny 88MIndeks górny 44
Zapis z użyciem symboli powłok:
KIndeks górny 22LIndeks górny 88MIndeks górny 44
Zapis w postaci schematu:
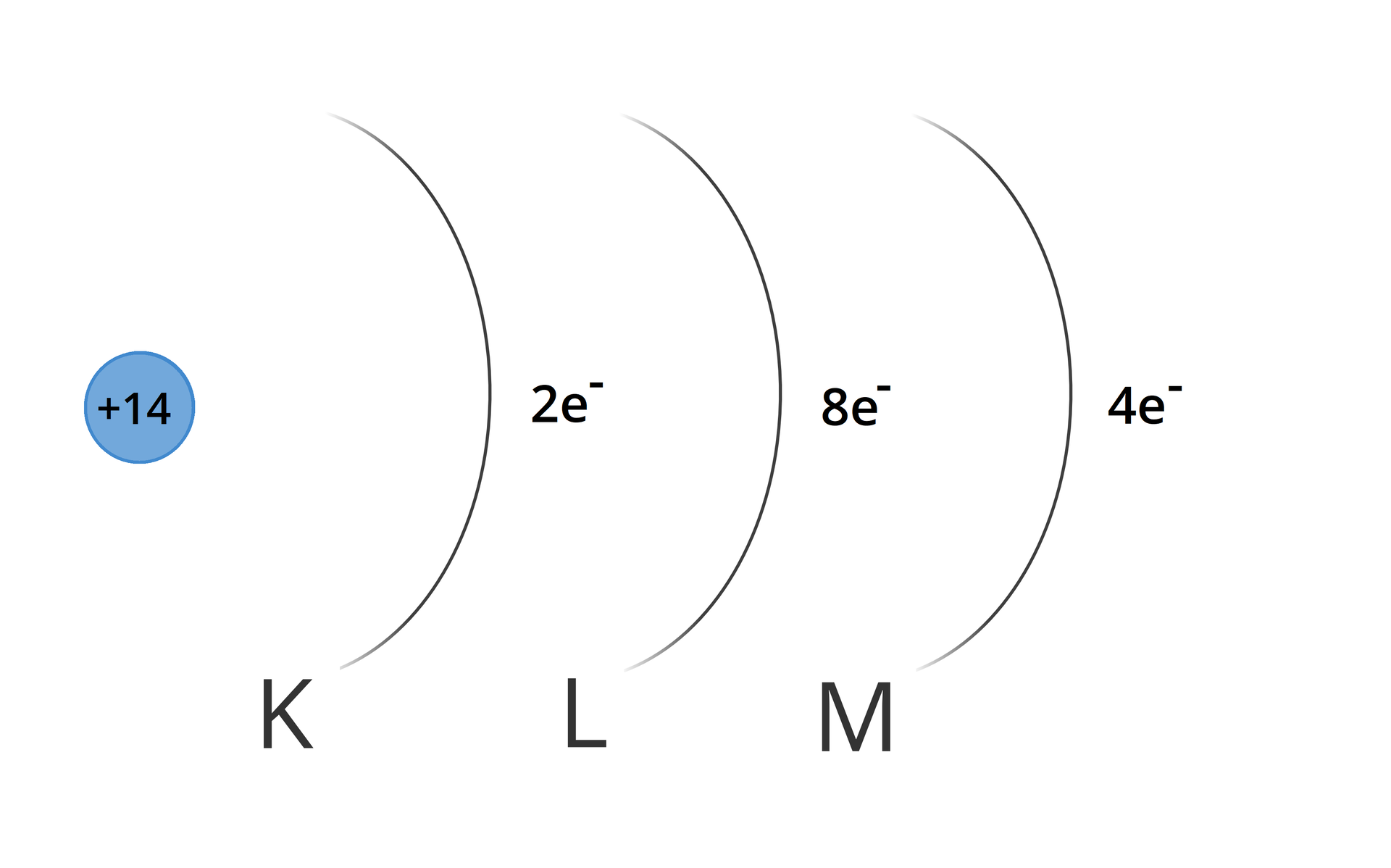
Dopasuj symbol pierwiastka do jego konfiguracji elektronowej, zapisanej w postaci schematu.
Dopasuj symbol pierwiastka do jego konfiguracji elektronowej, zapisanej z użyciem symboli powłok.
1. Si, 2. He, 3. O, 4. Ar, 5. Cl, 6. Zn, 7. H, 8. K K indeks górny, dwa, koniec indeksu górnego, L indeks górny, osiem, koniec indeksu górnego, M indeks górny, osiem, koniec indeksu górnego
1. Si, 2. He, 3. O, 4. Ar, 5. Cl, 6. Zn, 7. H, 8. K K indeks górny, jeden, koniec indeksu górnego
1. Si, 2. He, 3. O, 4. Ar, 5. Cl, 6. Zn, 7. H, 8. K K indeks górny, dwa, koniec indeksu górnego, L indeks górny, osiem, koniec indeksu górnego, M indeks górny, cztery, koniec indeksu górnego
Ile elektronów mogą pomieścić powłoki elektronowe?
Maksymalną liczbę elektronów na danej powłoce możemy obliczyć ze wzoru , gdzie n oznacza numer powłoki. Na przykład powłokę pierwszą mogą zajmować maksymalnie elektrony, gdyż . Powłokę drugą może z kolei zajmować maksymalnie elektronów, gdyż , a powłokę trzecią – maksymalnie elektronów, gdyż .
Wskaż maksymalną liczbę elektronów w obrębie powłoki piątej.
Obejrzyj poniższy film, a następnie zapoznaj się z poleceniem pod nim zawartym.
Film dostępny pod adresem /preview/resource/REN89HNcLTckp
W filmie ukazano budowę atomu, rozmieszczenie powłok elektronowych w atomie oraz porównanie energii elektronów występujących na poszczególnych powłokach.
Powłoki elektronowe nie mają fizycznego odzwierciedlenia w budowie atomu. To przede wszystkim energia danego elektronu oraz obecność pozostałych elektronów decydują, w jakim obszarze wokół jądra będzie się on poruszał. W przestrzeni wokół jądra nie ma żadnych fizycznych barier, które utrzymywałyby elektron na określonej powłoce.
Czy elektrony ostatniej powłoki są ważne?
Elektrony, które znajdują się najdalej od jądra atomowego, są najsłabiej przez to jądro przyciągane i często oddziałują na elektrony innych atomów. Można o nich w przenośni powiedzieć, że reprezentują atom na zewnątrz. Decydują o właściwościach atomu i nazywane są elektronami walencyjnymi, a powłoka, na której się znajdują, to powłoka walencyjna. Pozostałe elektrony nazywane są elektronami rdzenia atomowego.
Atomy mogą mieć różną liczbę elektronów walencyjnych (od 1 do 12). Dla pierwiastków chemicznych z grup od 1. do 12. liczba elektronów walencyjnych jest równa numerowi grupy. Ale dla pierwiastków chemicznych grup od do , liczbę elektronów walencyjnych oblicza się, odejmując od numeru grupy liczbę (wyjątek stanowi hel, który ma 2 elektrony walencyjne).

Film dostępny pod adresem /preview/resource/RH3mytlYxajbe
W filmie wyjaśniono, w jaki sposób odległość elektronów od jądra wpływa na siłę, z jaką są one przez nie przyciągane. Przedstawiono również rolę elektronów walencyjnych, a także omówiono ich położenie oraz liczbę w atomach helu i tlenu.
Uzupełnij poniższą tabelę, przeciągając liczby elektronów walencyjnych dla poszczególnych pierwiastków.