Miedź i jej związki.
Rola związków miedzi
Spośród całkowitej światowej produkcji, związki miedzi stanowią niewielki odsetek – w porównaniu do jej stopów oraz metalicznej miedzi. Mimo wszystko związki te odgrywają ważną i zróżnicowaną rolę w różnych gałęziach przemysłu i w rolnictwie. Niska toksyczność związków miedzi względem zwierząt i roślin wyższych sprawiła, że był to jeden z pierwszych znanych środków grzybobójczych. Obecnie ten trend jest utrzymywany. Miedź tworzy szereg różnych związków chemicznych. Wśród nich wyróżnia się związki miedzi na i stopniu utlenienia oraz związki kompleksowe na i stopniu utlenienia.
Tlenek miedzi()

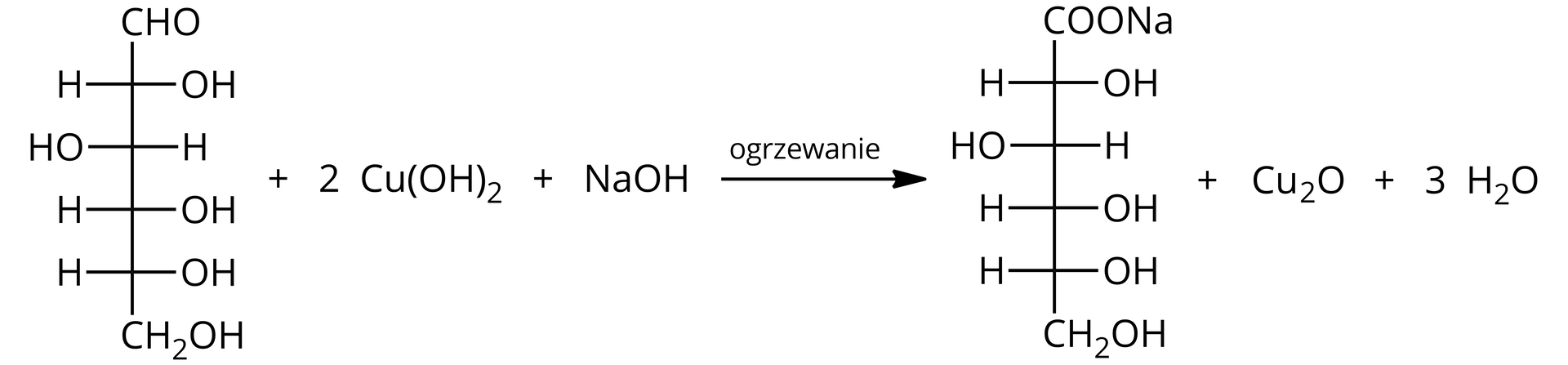
Związek ten powstaje również w wyniku działania substancji redukujących – takich jak aldehydy, cukry, ale również hydrazyny czy hydroksyloaminy – na mieszaninę zawierającą świeżo strącony wodorotlenek miedzi() lub związki kompleksowe miedzi() w roztworze o odczynie zasadowym. Tę właściwość wykorzystuje się w czterech próbach: TrommeraTrommera, FehlingaFehlinga, Benedicta oraz w próbie Barfoeda, które stosowane są w celu wykrywania i ilościowego oznaczania aldehydów oraz cukrów. Pozwalają one odróżnić ketony od aldehydów, dlatego stosuje się je między innymi w analityce laboratoryjnej. Przykładowo, w wyniku próby Trommera, najczęściej wykorzystywanej i spotykanej w czasie szkolnej nauki chemii, zachodzi następujący proces redukcji:
Co więcej, to właśnie stosowany jest w rolnictwie jako środek grzybobójczy (dla nasion i roślin uprawnych), ale także jako katalizator w reakcjach organicznych, dodatek do nawozów, pigment do ceramiki, szkła i tworzyw sztucznych, adsorbent tlenku węgla(). W postaci farb wykorzystywany jest do pokrywania den łodzi i statków w celu ochrony przed pąklami i glonami.
Na czym polega próba Fehlinga?
Próba Fehlinga wymaga zastosowania kompleksów winianowych miedzi(). Kompleksy te otrzymuje się w wyniku zmieszania roztworu siarczanu() miedzi() (roztwór Fehlinga ) z zasadowym roztworem winianu potasowo‑sodowego () (roztwór Fehlinga ). Ogrzewanie tego roztworu z cukrami prostymi i dwucukrami o właściwościach redukujących prowadzi do wytrącenia ceglastoczerwonego osadu tlenku miedzi() (osad początkowo ma barwę żółtą, będąc w stanie dużego rozdrobnienia).
Na czym polega próba Benedicta
Podobnie jak w próbie Fehlinga, próba Benedicta ukazuje właściwości redukujące niektórych cukrów (z wolnymi grupami karbonylowymi) poprzez wytrącenie ceglastoczerwonego tlenku miedzi(). W tym celu stosowany jest odczynnik Benedicta, który składa się z soli miedzi (siarczanu() miedzi()), alkalizującego węglanu sodu oraz cytrynianu sodu w celu zapobiegania wytrącania się wodorotlenku miedzi(). Próba ta jest znacznie bardziej precyzyjna w porównaniu do próby Fehlinga, ponieważ już stężenie cukru o wartości powoduje zmianę barwy (z niebieskiej na zieloną – zmieszanie barwy niebieskiej z ceglastoczerwoną). Ponadto jest ona bardziej selektywna względem cukrów, ponieważ chloroform, kreatynina i kwas moczowy nie ulegają redukcji przez ten odczynnik.
Barwa i osad | Przybliżona zawartość cukru [] |
|---|---|
zielona, bez osadu | – |
zielona, osad | |
żółtozielona, osad | |
pomarańczowa, osad | |
czerwona, osad |
Indeks dolny Źródło: Wydział Chemii Uniwersytetu Gdańskiego, chemia.ug.edu.pl, dostęp: 03.06.2020. Indeks dolny koniecŹródło: Wydział Chemii Uniwersytetu Gdańskiego, chemia.ug.edu.pl, dostęp: 03.06.2020.
Próba Barfoeda
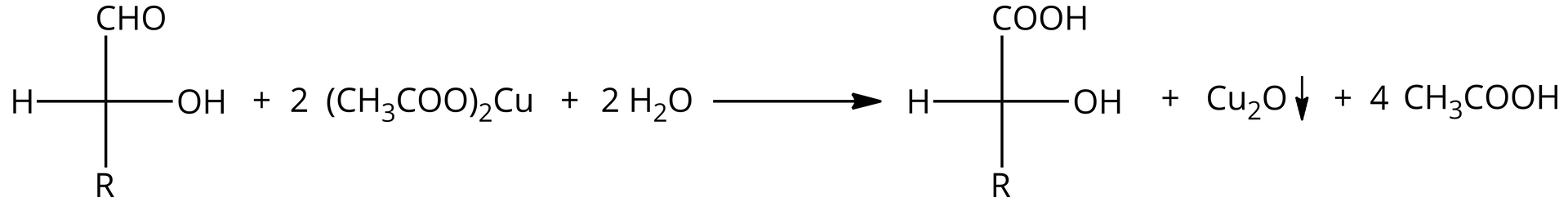
Próba ta jest modyfikacją próby Benedicta. Do redukcji jonów miedzi wykorzystywany jest octan miedzi() (etanian miedzi()). Reakcja przebiega znacznie wolniej niż wspomniana powyżej próba Benedicta.
Doświadczenie: przeprowadź próbę Trommera
Wykonaj próbę Trommera dla roztworu glukozy i dla soku z winogron.
W tym celu do około analizowanego roztworu dodaj roztwór zawierający wodorotlenek miedzi(), przygotowany in situ, czyli roztworu otrzymanego w wyniku zmieszania kropli roztworu z roztworu o stężeniu .
Następnie tak przygotowaną próbkę ogrzej, doprowadzając do wrzenia.
Wytrącenie ceglastoczerwonego osadu tlenku miedzi() będzie świadczyć o obecności redukujących właściwościach cukru.
Zastosowanie innych związków miedzi
Czy wiesz, że istnieje mydło miedziowe? Jakie ma ono zastosowanie? Zapoznaj się z grafiką interaktywną na ten temat, a następnie wykonaj ćwiczenia sprawdzające zdobytą wiedzę.
Czy wiesz, że istnieje mydło miedziowe? Jakie ma ono zastosowanie? Zapoznaj się z opisem grafiki interaktywnej na ten temat, a następnie wykonaj ćwiczenia sprawdzające zdobytą wiedzę.
Punkt pierwszy. nawias, C H indeks dolny, trzy, koniec indeksu dolnego, nawias, C H indeks dolny, dwa, koniec indeksu dolnego, zamknięcie nawiasu, indeks dolny, sześć, koniec indeksu dolnego, C O O, zamknięcie nawiasu, indeks dolny, dwa, koniec indeksu dolnego, C u. Mydło miedziowe stanowi środek grzybobójczy. Jest wytwarzany przez połączenie rozpuszczalnego związku miedzi(dwa) (zazwyczaj C u S O indeks dolny, cztery, koniec indeksu dolnego) z naturalnie występującym kwasem tłuszczowym (kwas oktanowy). Ilustracja przedstawiająca wzór mydła miedziowego o następującej strukturze: w nawiasie kwadratowym znajduje się grupa karboksylanowa C O O indeks górny, minus, koniec indeksu górnego połączona z łańcuchem wodorowęglowym zbudowanym z sześciu grup C H indeks dolny, dwa, koniec indeksu dolnego, z których ostatnia łączy się z grupą C H indeks dolny, trzy, koniec indeksu dolnego. Względem nawiasu w indeksie dolnym znajduje się cyfra dwa. Za nawiasem kation miedzi C u indeks górny, dwa, plus, koniec indeksu górnego. Jego aktywnym składnikiem jest oktanian miedzi(dwa), który, w porównaniu z innymi związkami nieorganicznymi miedzi, może być używany w niższych stężeniach, przez co dawki miedzi w postaci metalu mogą być znacznie zredukowane. A to z kolei ma wpływ na środowisko. Będąc produktem organicznym rozkłada się, tworząc rozpuszczalne związki miedzi i kwas tłuszczowy, które mogą być wykorzystywane przez drobnoustroje i rośliny.
Punkt drugi. Środek grzybobójczy. Jest to środek grzybobójczy o szerokim spektrum działania, który kontroluje choroby grzybowe i grzybopodobne, takie jak: mączniak prawdziwy i mączniak rzekomy na warzywach; rdza na roślinach ozdobnych; zaraza późna na ziemniakach i pomidorach. Zdjęcie przedstawiające dwa pomidory. Pierwszy z nich jest wyraźnie zaatakowany przez grzyba, drugi częściowo. Ich skórkę pokrywa szarawa warstwa pleśni. Podpis. Fotografia przedstawiająca zarazę na pomidorach. Zdjęcie przedstawiające liść winogronowy zaatakowanego przez mączniaka. Blaszka liścia pokryta jest jasnymi plamami, miejscami jest wyraźnie przesuszona. Podpis. Fotografia przedstawiająca objawy mączniaka rzekomego na liściach winogron.
Punkt trzeci. Inne dopuszczalne związki miedzi o działaniach grzybobójczych to: Siarczan(sześć) miedzi(dwa): C u S O indeks dolny, cztery, koniec indeksu dolnego; wodorotlenek miedzi(dwa): C u nawias, O H, zamknięcie nawiasu, indeks dolny, dwa, koniec indeksu dolnego; tlenek miedzi(dwa): C u O; tlenochlorek miedzi(dwa): C u indeks dolny, dwa, koniec indeksu dolnego, nawias, O H, zamknięcie nawiasu, indeks dolny, trzy, koniec indeksu dolnego, C l; węglan tetraaminamiedzi(dwa): C u nawias, N H indeks dolny, trzy, koniec indeksu dolnego, zamknięcie nawiasu, indeks dolny, cztery, koniec indeksu dolnego, C O indeks dolny, trzy, koniec indeksu dolnego
Punkt czwarty. Regulacje prawne. Grafika przedstawiająca drzewo liściaste znajdujące się w bryłce gleby, otoczone jest białymi taśmami. W tle znajduje się gleba. Grafika symbolizuje ochronę środowiska. Podpis. Ochrona środowiska. Według jednego z organów do spraw Certyfikacji ekologicznej (Soil Association), całkowita ilość miedzi, którą można zastosować na gruntach organicznych, wynosi sześć kilogramów na hektar na rok. Limit ten został zaprojektowany w taki sposób, aby ilość miedzi w glebie nie przekraczała limitów określonych w normach Soil Association dla metali ciężkich.
Czy wiesz, co to jest błękit alcjanowy (alcjański) i do czego jest stosowany? Zapoznaj się z grafiką interaktywną prezentującą informację na ten temat, a następnie wykonaj ćwiczenia.
Czy wiesz, co to jest błękit alcjanowy (alcjański) i do czego jest stosowany? Zapoznaj się z opisem grafiki interaktywnej prezentującej informację na ten temat, a następnie wykonaj ćwiczenia.
Punkt pierwszy. Co to jest błękit alcjański? Jest to organiczny związek chemiczny, stanowiący pochodną ftalocyjaniny o wzorze sumarycznym: C indeks dolny, pięćdziesiąt sześć, koniec indeksu dolnego, H indeks dolny, sześćdziesiąt osiem, koniec indeksu dolnego, C l indeks dolny, cztery, koniec indeksu dolnego, C u N indeks dolny, szesnaście, koniec indeksu dolnego, S indeks dolny, cztery, koniec indeksu dolnego. Zdjęcie przedstawiające kultury komórkowe znajdujące się na ośmiu szalkach Petriego, wybarwione błękitem alcjanowym. Na każdej szalce intensywność wybarwienia jest różna, od błękitnego koloru do bladobłękitnego. Podpis. Hodowle komórkowe zabarwione błękitem alcjańskim.
Punkt drugi. Jaka jest rola błękitu alcjanowego w histologii? Błękit alcjanowy różnicuje kwaśne glikozaminoglikany, które wchodzą w skład błon podstawnych, elementów tkanki łącznej, chrzęstnej i kostnej czy wydzielin gruczołów. Barwi kwaśne mukopolisacharydy i glikozoaminoglikany, dając w rezultacie kolor od błękitnego do niebieskozielonego. Zdjęcie przedstawiające wybarwione błękitem alcjanowym komórki kubkowe Barretta. Komórki te tworzą kosmki. Podpis. Barwienie błękitem alcjanowym, podkreślające komórki kubkowe Barretta.
Punkt trzeci. Inne zastosowania błękitu alcjanowego. Oprócz użycia go jako barwnika lub bejcy, błękit alcjanowy znajduje również inne zastosowania: używany jako spoiwo – stosowany był do przyłączania komórek do szklanych szkiełek nakrywkowych w technikach immunofluorescencji, wstępne traktowanie preparatów szklanych roztworem błękitu alcjanowego poprawiło przyczepność skrawków szpiku osadzonych w metakrylanie glikolu; używany jako środek powlekający – ze względu na dużą powierzchnię aromatyczną (uczestnictwo w interakcji Van der Waalsa oraz zlokalizowane ładunki) można nim powlekać powierzchnie, modyfikować jej właściwości i ładunek; używany jako element elektrody – działającej jako bardzo czuły czujnik redoks w porównaniu z elektrodą zbudowaną z pasty węglowej.
Jakie właściwości mydła miedziowego pozwalają na zastosowanie go w walce z na przykład zarazą ziemniaka przedstawioną na poniższym zdjęciu?
