Odmiany alotropowe węgla pierwiastkowego i innych pierwiastków chemicznych
Czy wiesz, że węgiel to niezwykły pierwiastek? Jak to możliwe, że grafit w ołówku i diamenty w najdroższej biżuterii są zbudowane z tego samego pierwiastka? W czym tkwi fenomen najtwardszych minerałów w przyrodzie? Co wspólnego mają węgiel i piłka nożna? Czy wiesz, czym jest grafen i dlaczego tak dużo mówi się o nim w ostatnich latach?
definicję pierwiastka chemicznego jako substancji składającej się wyłącznie z atomów posiadających jednakową liczbę protonów w jądrze np.: , , , ;
znaczenie węgla w chemii organicznej i nieorganicznej;
strukturę elektronową atomu węgla.
wyjaśniać, na czym polega zjawisko alotropii;
wymieniać odmiany alotropowe węgla, opisywać ich budowę, właściwości i zastosowania;
uzasadniać zależność właściwości i zastosowania diamentu, grafitu, fullerenów, grafenu, cyklokarbonu od ich budowy wewnętrznej;
wymieniać inne pierwiastki, które mogą występować pod postaciami różnych odmian alotropowych.
1. Pojęcie alotropia
Niektóre pierwiastki chemiczne, głównie niemetale, występują w różnych postaciach, które mają odmienne właściwości fizyczne i różną aktywność chemiczną. Postaci te zwane odmianami alotropowymiodmianami alotropowymi różnią się budową sieci krystalicznej (np. diament, grafit, fullereny, grafen) i/lub liczbą atomów w cząsteczce (np. – ditlen, – tritlen, czyli ozon, – tetratlen, czyli tlen czerwony). To zjawisko nazywa się alotropiąalotropią, od greckiego: allos (inny) i tropos(rodzaj).

Innym ważnym pojęciem jest anizotropiaanizotropia. Dotyczy ona zmiany właściwości danej substancji w zależności od kierunku, w którym się je bada. Dotyczy między innymi przewodnictwa elektrycznego i cieplnego, łupliwości, właściwości optycznych. Substancje wykazujące anizotropię jednych właściwości fizycznych, mogą nie wykazywać anizotropii innych właściwości, np. optycznych.
2. Grafit – węgiel, którym można pisać
GrafitGrafit jest zbudowany z płaskich warstw ułożonych jedna nad drugą. Każda warstwa przypomina strukturę plastra miodu. Atomy węgla są ułożone w regularne sześciokąty o wspólnych bokach. W obrębie każdej warstwy atomy są połączone silnymi wiązaniami kowalencyjnymi z trzema sąsiednimi atomami tego pierwiastka. Natomiast między warstwami występują tylko słabe oddziaływania (van der Waalsa), dlatego kryształy grafitu są miękkie i łatwo dają się łupać. Odległości między płaszczyznami są niemal razy większe niż długości wiązań między atomami węgla w pierścieniach, stąd siła wiązań między warstwami jest mała. Dlatego poszczególne warstwy grafitu stosunkowo łatwo się rozdzielają, co wykorzystujemy za każdym razem, przyciskając ołówek do kartki papieru.

Grafit jest odmianą węgla o czarnoszarej barwie i połysku, który przypomina połysk metaliczny. Jest bardzo miękki (twardość grafitu w skali Mohsaskali Mohsa wynosi ), podatny na ścieranie i łupliwy. Ma doskonałe właściwości smarne, jest tłusty w dotyku i wytrzymały na wysokie temperatury. Wykazuje wysoką odporność mechaniczną na ściskanie i niewielką – na rozciąganie. Ponadto grafit i wyroby grafitowe nie rozpuszczają się w wodzie, charakteryzują się małą aktywnością chemiczną, łatwością składowania i utylizacji oraz brakiem negatywnego wpływu na środowisko. Dzięki tym cechom zyskał on miano materiału nowoczesnego, a zarazem ekologicznego.
Wykonano doświadczenie, w którym zbadano czy grafit przewodzi prąd elektryczny i ciepło.
Problem badawczy:
Czy grafit przewodzi prąd elektryczny i ciepło?
Hipoteza:
Grafit to odmiana alotropowa węgla, która przewodzi prąd elektryczny i ciepło.
Co było potrzebne:
grafitowy pręcik z ołówka;
dioda typu LED;
przewody z zaciskami typu krokodylki;
bateria ;
kartka papieru;
ołówek;
palnik spirytusowy;
termometr;
szczypce.
Przebieg doświadczenia:
Zbudowano obwód elektryczny składający się z baterii, diody i przewodów elektrycznych zakończonych krokodylkami. Umieszczono w nim pręcik grafitowy z ołówka i sprawdzono, czy po zamknięciu obwodu płynie prąd elektryczny. Następnie na kartce papieru narysowano grubą kreskę ołówkiem (miękkim – typu „B”), na której następnie położono krokodylki wcześniej zmontowanego obwodu elektrycznego. Sprawdzono czy dioda się zaświeciła. W następnym etapie koniec pręcika grafitowego umieszczono w płomieniu palnika i ogrzewano przez około minuty. Po tym czasie zmierzono temperaturę drugiego końca pręcika, przykładając do niego termometr.
Obserwacje:
Po zamknięciu obwodu elektrycznego dioda się zaświeciła. Prąd popłynął również, gdy w obwodzie umieszczono kartkę papieru z grubą kreską narysowaną ołówkiem. Podczas ogrzewania pręcik szybko stał się ciepły, a po usunięciu źródła ciepła także szybko się ochłodził.
Wnioski:
Grafit dobrze przewodzi prąd elektryczny i ciepło.
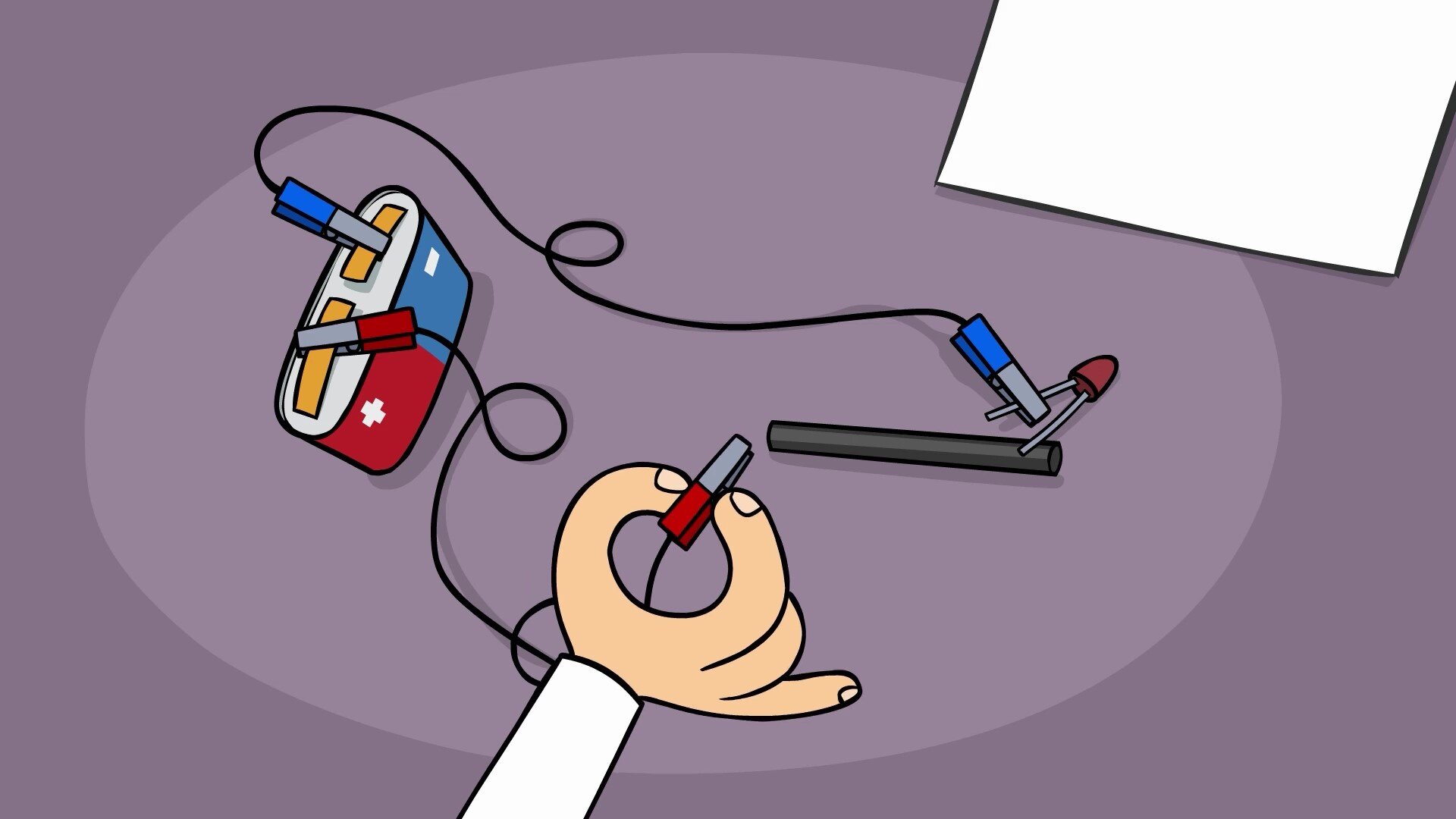
Film dostępny pod adresem /preview/resource/R1RoZYbwTa07Y
Film ukazuje doświadczenie, w którym zbadano, czy grafit dobrze przewodzi prąd elektryczny oraz ciepło.
Ten bardzo niepozorny minerałminerał ma różnorodne zastosowanie w życiu codziennym. Już w średniowieczu używano go do pisania i wyrobu tygli stosowanych w pracowniach alchemików. Dzisiaj również piszemy ołówkami, których rysiki są grafitowe i nadal wytwarza się z niego tygle oraz materiały ogniotrwałe (np. cegły, bloki węglowe, betony grafitowe). Ponadto, odmianę tę wykorzystuje się do produkcji: szczotek węglowych, klocków hamulcowych w samochodach, suchych smarów, farb antykorozyjnych, elektrod używanych do elektrolitycznego otrzymywania metali oraz elektrod do produkcji baterii, moderatorów (prętów spowalniających neutrony) w reaktorach atomowych i materiałów konstrukcyjnych, np. kompozytów grafitowych (te znalazły zastosowanie do produkcji rakiet tenisowych i elementów bolidów Formuły ).

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/Ddz3uqFCY
Co wspólnego mają ołów i ołówek?
Dzisiaj mamy wiele różnych przyborów, których używamy do pisania na papierze. Dawniej, gdy nie znano jeszcze grafitu i ołówków do pisania wykorzystywano kawałki ołowiu, który przestał być używany w roku. Legenda głosi, że pewnego dnia na północy Anglii straszna burza poprzewracała ogromne drzewa, odkrywając duże pokłady czarnej substancji pod ich korzeniami. Wyglądała ona jak węgiel, ale się nie paliła. Pasterze zorientowali się, że jest to idealny materiał do znakowania owiec. I tak odkryto grafit, jednak nazwa ołówek pozostała.
Współczesny ołówek jest pręcikiem wykonanym najczęściej nie tylko z grafitu, lecz również z kaolinu, umieszczonego w oprawie drewnianej lub z tworzywa sztucznego. Podczas pisania grafit ściera się, pozostawiając ślad na powierzchni, np. papieru. Twardość oraz odcień rysika ołówka zależą od proporcji pomiędzy grafitem a glinką kaolinową. Im więcej grafitu, tym ciemniejszy oraz bardziej miękki jest ołówek. Większa ilość kaolinu sprawia, że ołówek jest twardszy i jaśniejszy. Ołówek ma wkład z czystego grafitu. W ołówkach piszących w różnych kolorach nie stosuje się w ogóle grafitu, tylko produkuje się je z mieszanki wosku, kaolinu i barwników. Ołówek z gumką opatentowano dopiero w roku.

3. Diament – symbol bogactwa, piękna i oczarowania
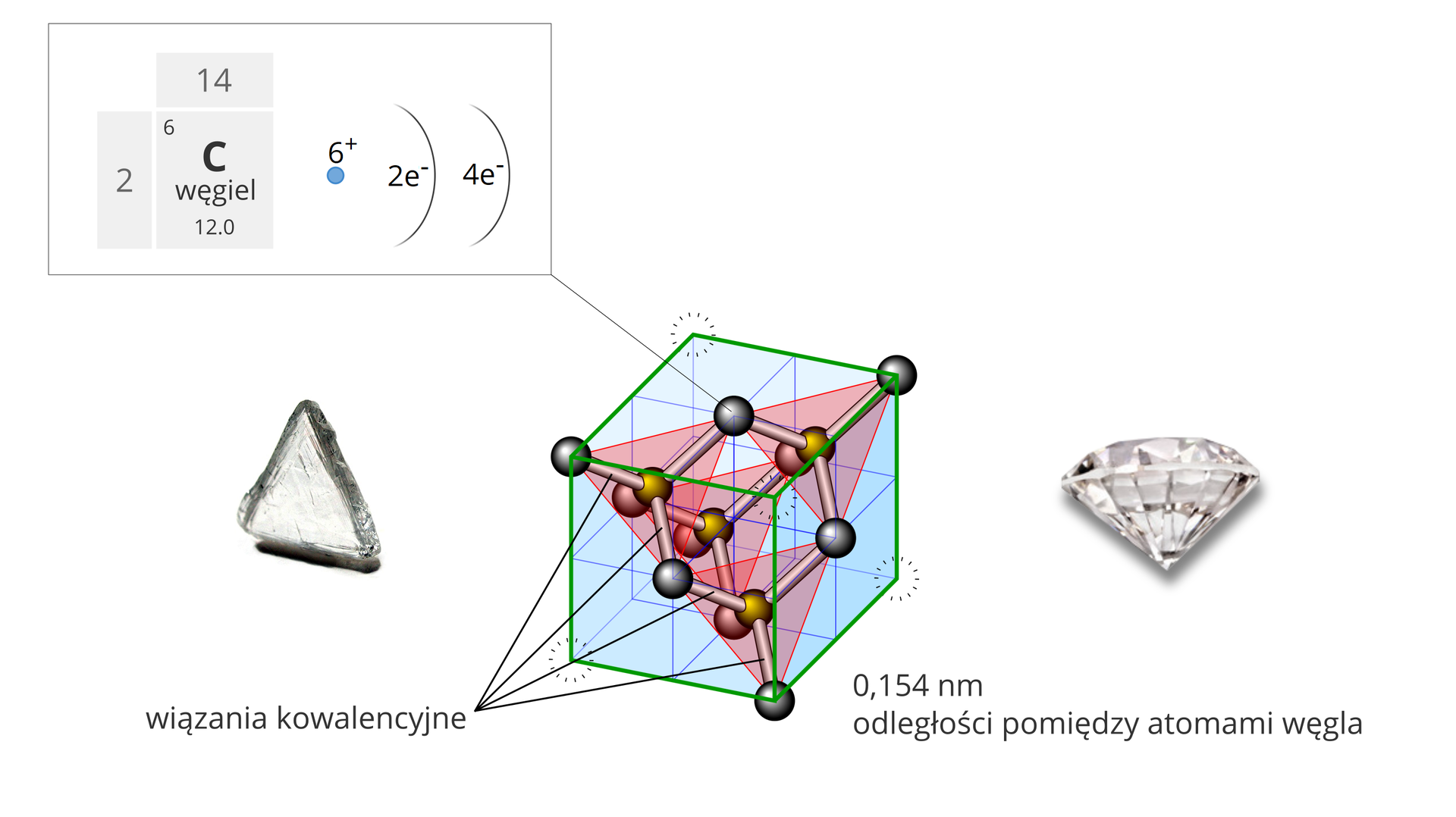
Od stuleci diamenty zachwycają ludzi swoim doskonałym pięknem, rzadkością występowania i niezwykłymi właściwościami. DiamentDiament zbudowany jest z atomów węgla tworzących regularną sieć przestrzenną, o kształcie czworościanu foremnego (tetraedru), w której każdy atom łączy się z czterema innymi atomami węgla. Równomiernie rozłożone, mocne wiązania kowalencyjne wpływają na bardzo dużą twardość tej odmiany alotropowej (w skali Mohsaskali Mohsa twardość diamentu wynosi ).
Cullinan – największy diament świata
Znaleziono go czerwca w Republice Południowej Afryki. Miał wymiary i ważył karatówkaratów, czyli . Pierwotnie był on najprawdopodobniej jeszcze większy. Kamień został ofiarowany królowi Edwardowi na jego urodziny. Na polecenie króla lutego roku znany amsterdamski szlifierz po trzech miesiącach oglądania kamienia zdecydował się podzielić diament na dwie części.
Umieścił precyzyjnie ostrze w najlepiej wybranym punkcie, uderzył młotkiem i ostrze pękło, lecz kamień pozostał nienaruszony. Przy drugim uderzeniu diament pękł tak, jak przewidywał szlifierz, jednak on sam zemdlał na skutek ogromnego stresu wywołanego możliwością uszkodzenia tego wyjątkowego cudu natury. Z Cullinanu uzyskano dużych kamieni i mniejszych o łącznej masie karata, co stanowi masy początkowej i oznacza stratę sięgającą . Kamienie szlifowano wiele miesięcy.

Film dostępny pod adresem /preview/resource/R19rD2MuEWCWX
Film ukazuje jak powstały diamenty, przedstawia sposoby i miejsca ich wydobycia, a także prezentuje najsłynniejsze diamenty świata.
Diamenty w stanie czystym tworzą z reguły bezbarwne, przeźroczyste kryształy. Ponieważ często w ich sieci krystalicznej występują jony innych pierwiastków, np.: boru, azotu, manganu, żelaza, zdecydowana większość wydobywanych kamieni jest zabarwiona. Wyróżnia się diamenty o barwie: żółtej, czerwonej, niebieskiej, fioletowej. Znane są nawet czarne diamenty, tak zwane karbonado. Diamenty są wykorzystywane do cięcia szkła, ze względu na ich największą twardość wśród wszystkich ziemskich minerałówminerałów. Obliczono, że diament o masie karatakarata – – wystarczyłby na przecięcie tafli szkła o długości większej niż odległość z Ziemi do Księżyca. O wyjątkowości diamentów wśród innych minerałów decyduje fascynująca gra świateł. Po oszlifowaniu powstają, tak zwane, brylanty, które silnie załamują światło, a także mocno je rozszczepiają.
Wykorzystując poniższą aplikację, porównaj przewodnictwo elektryczne diamentu i kilku innych minerałów.
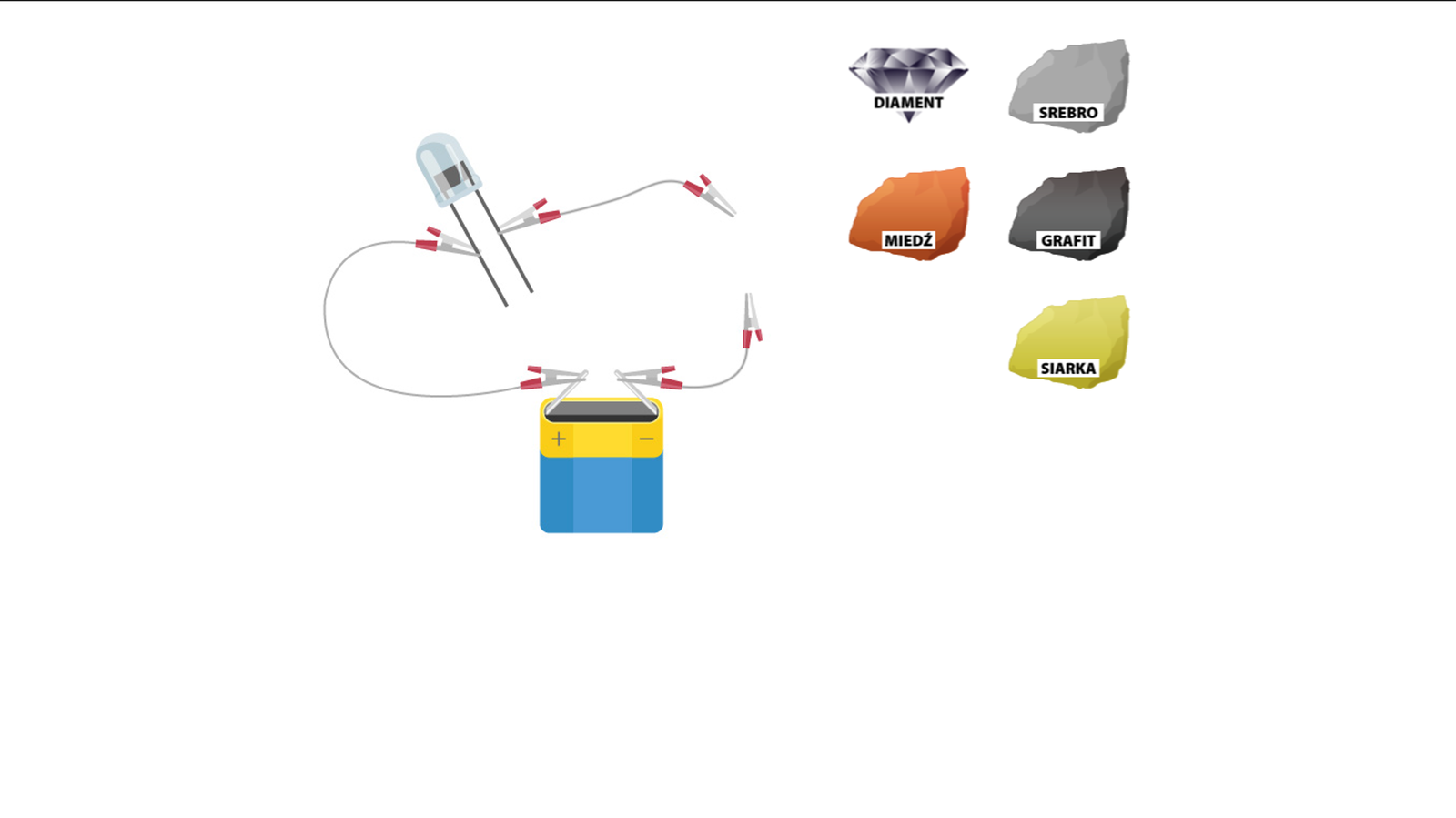
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/Ddz3uqFCY
Diament ze względu na swoją budowę nie przewodzi prądu elektrycznego, ale jest bardzo dobrym przewodnikiem ciepła. Jest bierny chemicznie. Słowo diament pochodzi od greckiego adamas, co oznacza niezwyciężony, ponieważ jest to materiał bardzo twardy, czyli odporny na odkształcenia plastyczne powstałe na niewielkiej powierzchni materiału, wskutek mechanicznego wciskania w nią ciała, które jest bardziej twarde. Jest jednak materiałem kruchym, co oznacza, że po zastosowaniu odpowiednio dużej siły zewnętrznej może pękać. Przy ogrzaniu go do temperatury spala się.

Brylanty nie od jubilera, czyli syntetyczne diamenty
Pod każdą szerokością geograficzną diament wzbudza emocje i jest utożsamiany z prestiżem, bogactwem i luksusem. Grecy uważali, że jego kryształy to łzy bogów. Rzymianie zaś wierzyli, że to okruchy gwiazd. Dla Indian był talizmanem chroniącym przed chorobą. Królowie liczyli, że diament osłoni ich podczas bitwy. Nic dziwnego, że od wieków ludzie marzyli o tym, żeby skraść tajemnicę naturze i nauczyć się wytwarzać diamenty. Udało się to po raz pierwszy lutego szwedzkiej firmie elektroenergetycznej ASEA. Stworzono warunki laboratoryjne podobne do tych, jakie występują głęboko pod powierzchnią Ziemi. Dzięki zastosowaniu olbrzymiego ciśnienia, tzn. atmosfer, w wysokiej temperaturze około i w obecności metali, które pełnią rolę katalizatorów, przeprowadzono reakcję przemiany grafitu w diament. Diamenty syntetyczne nie różnią się praktycznie niczym od diamentów naturalnych – cechują się tą samą strukturą, barwą i właściwościami. Trudności z ich odróżnieniem od diamentów naturalnych mają nawet jubilerzy. Niestety, nie zmniejszyło to ceny diamentów. Syntetyczne diamenty są za małe, żeby oprawiać je w szlachetne kruszce. Największe mają tylko około do karatówkaratów, a koszt ich wytwarzania jest bardzo wysoki. W kwestii klejnotów jesteśmy zdani na to, co oferuje nam natura.

4. Fullereny – najbardziej fascynująca postać węgla
W roku eksperyment naukowców Harolda Kroto, Richarda Smalleya i Roberta Curla doprowadził do odkrycia kolejnej odmiany alotropowej węgla – fullerenówfullerenów. Są to cząsteczki zbudowane z parzystej liczby: od do około atomów węgla, które tworzą zamkniętą bryłę. Najbardziej popularny, fulleren , wyglądem przypomina piłkę futbolową i jest zbudowany z atomów, które tworzą pierścieni pięcioatomowych i pierścieni sześcioatomowych. Takie struktury geodezyjne, przypominające cząsteczki , konstruował niegdyś R. Buckminster Fuller i właśnie od nazwiska tego amerykańskiego architekta, matematyka i filozofa powstała nazwa tej odmiany. Odkrycie to ukazało zupełnie nowe oblicze węgla – pierwiastka, który wydawał się dotąd doskonale znany. Oprócz fullerenów właściwych otrzymano ponadto nanorurki i nanocebulki.

Fullereny stosuje się w medycynie (np.: produkcja kosmetyków niszczących wolne rodniki, nośniki leków np. blokujących aktywne centra wirusa HIV); w życiu codziennym (np.: wzmocnienie foli aluminiowej, wydłużanie trwałości żywności, produkcja materiałów fotoprzewodzących stosowanych w drukarkach); w elektrotechnice i katalizie (np. stabilizatory paliw lotniczych, diody, katalizatory); w nanotechnologii (np. układy mikroelektroniczne); w elektronice polimerowej (np. fotoogniwa polimerowe)
5. Grafen – droga do miniaturyzacji
Niezwykłą odmianą węgla jest też grafengrafen, czyli warstwa grafitu o grubości jednego atomu. Ponieważ warstwa grafenu jest niezmiernie cienka, nanosi się go na inne materiały, którym nadaje on niezwykłe właściwości. Grafen został uzyskany w roku przez Andre Geima i Kostya Novoselova. Udało się im oddzielić pojedynczą warstwę grafenu, przyklejając taśmę samoprzylepną do powierzchni grafitu. Za to doświadczenie zostali uhonorowani Nagrodą Nobla.

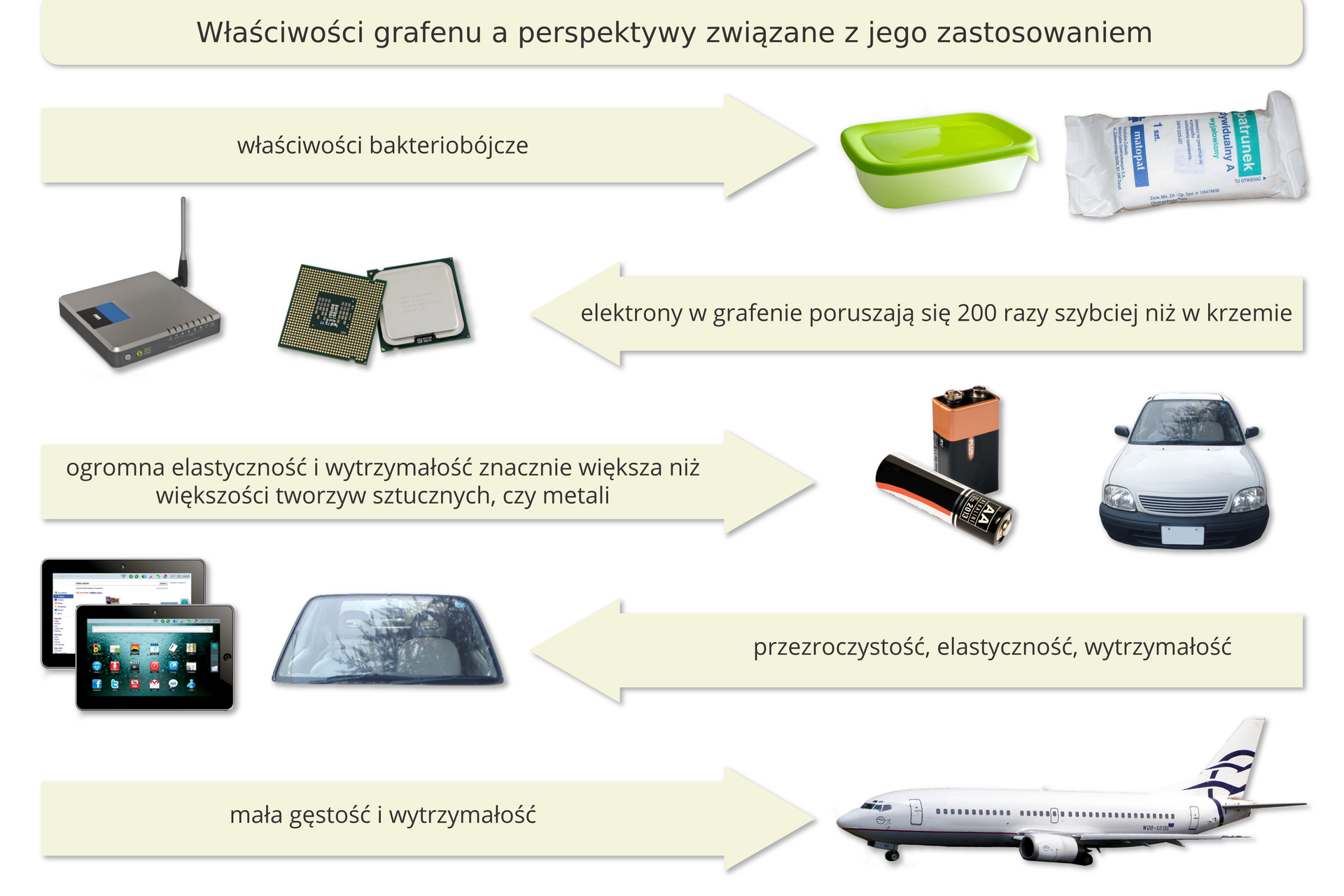
Jest to niezwykle obiecująca substancja. Okazało się bowiem, że nowo odkryta forma węgla jest jedną z najwytrzymalszych i zarazem najbardziej rozciągliwym znanym materiałem. To znakomity przewodnik ciepła – dziesięciokrotnie lepszy od srebra. Podobnie jak grafit jest również bardzo dobrym przewodnikiem prądu elektrycznego, ale jeśli przyłączy się do niego atomy wodoru, to tworzy nowy materiał, zwany grafanem, będący doskonałym izolatorem. W porównaniu ze stalą nowy materiał ma od pięciu do sześciu razy mniejszą gęstość, jest dwukrotnie twardszy, trzynastokrotnie bardziej elastyczny i stukrotnie bardziej wytrzymały na rozciąganie. Jego wiązania atomowe są tak ścisłe, że nie przepuszcza on nawet bakterii.
Grafen jest jak współczesny kamień filozoficzny – podobnie rozbudza nadzieje i wyobraźnię, tyle że potrafimy go produkować. Jego historia jest związana z naszym krajem, ponieważ to właśnie polskim naukowcom zawdzięczamy opracowanie technologii przemysłowego otrzymywania tej niezwykłej substancji. Obecnie to najdroższy materiał, ale ze względu na swoje doskonałe właściwości z pewnością zastąpi w przyszłości krzem.
6. Cyklokarbon
Cyklokarbon zwany inaczej cyklo[]karbonem, cyklooktadekawęglem,
cyklo[]węglem jest alotropową odmianą węgla o strukturze cząsteczkowej – pierścieniem złożonym z atomów węgla, w którym naprzemiennie występują wiązania potrójne i pojedyncze.
Po raz pierwszy jego istnienie w formie gazowej potwierdzono w roku, w fazie stałej otrzymano go w roku. Metoda syntezy, jaką wykorzystano, jest interesująca. W pierwszej kolejności otrzymano związek zwany tlenkiem cyklokarbonu: , który naniesiono na powierzchnię chlorku sodu w temperaturze . Następnie, stosując zaawansowany mikroskop sił atomowychmikroskop sił atomowych, usunięto pojedyncze cząsteczki tlenku węgla(). W ten sposób otrzymano pojedynczą cząsteczkę cyklokarbonu.
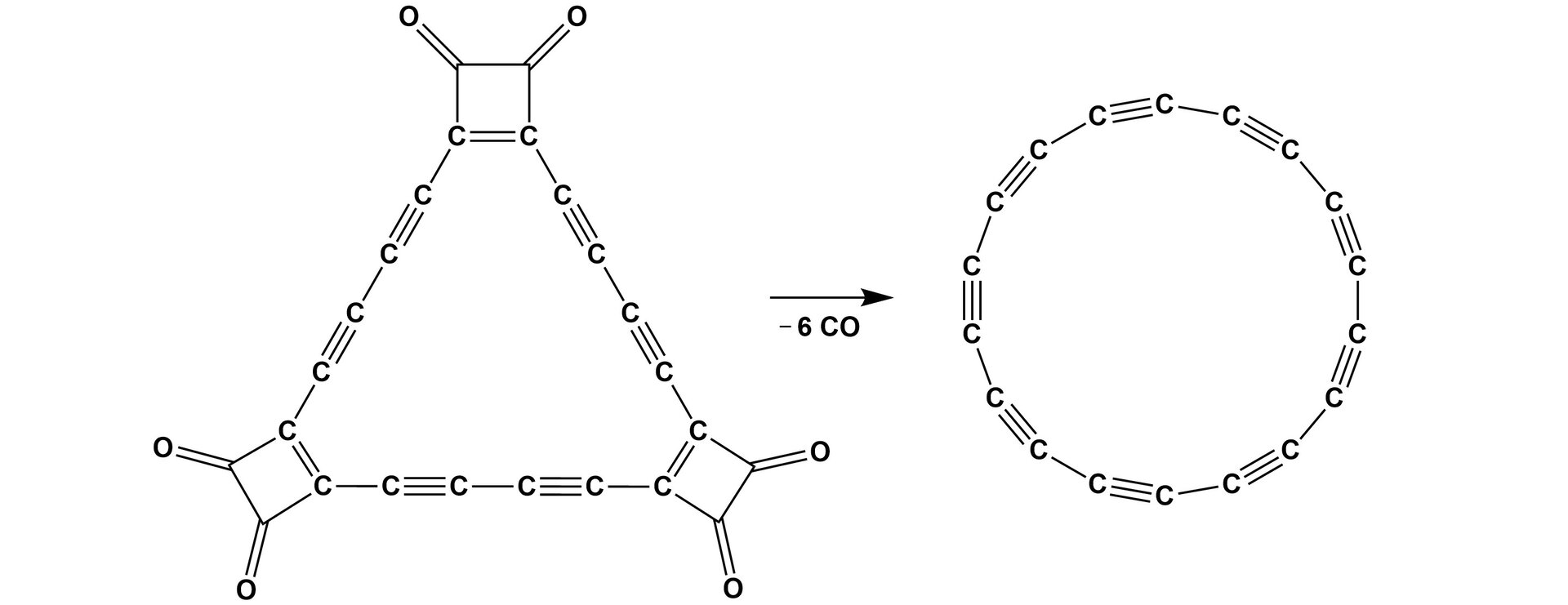
Jest to odmiana alotropowa węgla otrzymana stosunkowo niedawno, dlatego też nie są znane jego właściwości takie jak stabilność. Przewiduje się, że cyklokarbon powinien mieć charakter półprzewodnika.
7. Alotropia siarki
Siarka tworzy najwięcej odmian alotropowych wśród pierwiastków – ponad , z których najważniejsze to siarka rombowa () i siarka jednoskośna (). Obie odmiany zbudowane są z pierścieni ośmioatomowych () różniących się sposobem ułożenia cząsteczek ośmioatomowych w kryształach. Siarka rombowa jest trwała do temperatury . W tej temperaturze przekształca się w siarkę jednoskośną. W temperaturze siarka jednoskośna topi się i przechodzi w ruchliwą jasnożółtą ciecz – . Kiedy temperatura wzrasta, siarka brunatnieje i gęstnieje – powstaje . Podwyższenie temperatury do poziomu powyżej powoduje zmniejszenie się lepkości siarki, ciecz staje się znowu łatwo płynna, nie zmieniając już barwy. W temperaturze siarka wrze, dając pomarańczowe pary składające się z cząsteczek , które podczas dalszego ogrzewania ulegają dysocjacji na coraz mniejsze drobiny (kolejno w i ). Powolne chłodzenie siarki powoduje odwrotną kolejność przemian, aż do otrzymania siarki rombowej. Natomiast gwałtowne chłodzenie stopionej siarki prowadzi do trzymania tak zwanej siarki plastycznej, która ma postać brunatnej masy. Szybko chłodzone pary siarki kondensują w postaci drobnego żółtego proszku, zwanego kwiatem siarczanym.

8. Alotropia fosforu i innych pierwiastków
Fosfor został odkryty w roku przez niemieckiego alchemika Henniga Brandta, który poszukując kamienia filozoficznego, prażył zagęszczony mocz z piaskiem bez dostępu powietrza. W trakcie jednej z takich prób Brandt otrzymał substancję, która wzbudzała wielkie zainteresowanie, głównie dlatego że świeciła w ciemności. W ten sposób został odkryty fosfor biały. Dziś wiemy, że fosfor tworzy jeszcze odmiany: czerwoną, fioletową i czarną. Odmiany te różnią się nie tylko niektórymi właściwościami fizycznymi, ale również aktywnością chemiczną. Najbardziej aktywna jest odmiana biała, a całkowicie bierna chemicznie jest odmiana czarna.

Film dostępny pod adresem /preview/resource/R2Qa6lDHaiin7
Film przedstawia różne odmiany alotropowe fosforu wraz z zdjęciami oraz opisami ich właściwości. Są to: fosfor czarny, fosfor biały, fosfor czerwony i fosfor fioletowy.
Mniej znanymi pierwiastkami występującymi w postaci odmian alotropowych są: tlen, arsen, antymon, cyna, mangan, selen, uran, żelazo.
Podsumowanie
Występowanie pierwiastka w odmianach różniących się budową i właściwościami to alotropia.
Grafit, diament, fullereny i grafen to odmiany alotropowe węgla.
Grafit ma strukturę warstwową. Jest miękki, dobrze przewodzi prąd elektryczny i ciepło. Jest też odporny na wysokie temperatury oraz mało aktywny chemicznie.
W sieci krystalicznej diamentu każdy atom węgla jest połączony wiązaniami o identycznej długości z czterema innymi atomami tego pierwiastka. Diament jest bardzo twardy, nie przewodzi prądu elektrycznego, ale dobrze przewodzi ciepło. Po oszlifowaniu daje wielobarwne efekty świetlne. Jest bardzo mało aktywny chemicznie.
Fullereny to cząsteczkowa odmiana węgla. Wykazują właściwości nadprzewodzące i półprzewodnikowe oraz większą aktywność chemiczną w porównaniu do grafitu.
Grafen to warstwa grafitu o grubości jednego atomu. Jest materiałem bardzo wytrzymałym i elastycznym, najlepiej przewodzącym prąd elektryczny, a po przyłączeniu atomów wodoru staje się izolatorem.
Odmiany alotropowe węgla znajdują wiele ważnych zastosowań, między innymi w elektronice, medycynie, przemyśle.
Słownik
zjawisko występowania tego samego pierwiastka chemicznego w kilku odmianach, które różnią się między sobą strukturą krystaliczną lub liczbą atomów w cząsteczce, co powoduje ich odmienne właściwości
zmiany właściwości danej substancji w zależności od kierunku, w którym się je bada; dotyczy między innymi przewodnictwa elektrycznego i cieplnego, łupliwości, właściwości optycznych
minerał, odmiana alotropowa węgla
minerał, odmiana alotropowa węgla będąca najtwardszą znaną substancją występującą w przyrodzie
cząsteczki węgla składające się z parzystej liczby atomów tworzące zamkniętą, pustą w środku bryłę
odmiana alotropowa węgla o płaskiej strukturze grubości jednego atomu
jednostka masy używana w jubilerstwie do określania wielkości kamieni szlachetnych, pereł, a także czystości złota; karat to zawartości wagowej złota w stopie
mikroskop, umożliwiający uzyskanie obrazu powierzchni z rozdzielczością rzędu wymiarów pojedynczego atomu dzięki wykorzystaniu sił oddziaływań międzyatomowych
ciało krystaliczne, będące zbiorem pierwiastków lub związków chemicznych, które powstało w wyniku procesów geologicznych
odmiany tego samego pierwiastka, różniące się sposobem rozmieszczenia atomów w przestrzeni lub liczbą atomów w cząsteczce, w związku z czym różnią się właściwościami
skala twardości minerałów charakteryzująca odporność na zarysowania materiałów twardszych przez materiały bardziej miękkie
Ćwiczenia
Wymień odmiany alotropowe węgla.
Wymień zastosowania odmian alotropowych węgla.
1. grafen, 2. grafit, 3. fullereny, 4. diament jest znakomitym przewodnikiem ciepła, bardzo dobrze przewodzi prąd elektryczny, a może również w odpowiednich warunkach zachowywać się jak izolator.
Odmianą węgla, która dobrze przewodzi prąd elektryczny i ciepło jest 1. grafen, 2. grafit, 3. fullereny, 4. diament.
Odmiana alotropowa węgla, która wykazuje właściwości nadprzewodzące i półprzewodnikowe to 1. grafen, 2. grafit, 3. fullereny, 4. diament.
Przeczytaj fragment tekstu dotyczący nanocebulek i wykonaj polecenie poniżej.
Carbon nano–onions (CNOs) are a member of the fullerene family, they are also called nested nanoparticle. They are nanoscale carbon structure formed by nested carbon spheres. Carbon nano–onions were first discovered by Ugarte in , who obtained them by intense electron irradiation of carbon soot. These structures remain as one of the most exciting and fascinating carbon forms, along with graphene and its derivatives, due to their unique chemical and physical properties. Their low cytotoxicity allows for high applicability in the biomedical field, in particular, nanomedicine.
Bibliografia
Bielański A., Podstawy chemii nieorganicznej, t. 1–2, Warszawa 2012, wyd. 6.
Encyklopedia PWN
Pazdro K. M., Chemia. Pierwiastki i związki nieorganiczne, Warszawa 2012.

