Podsumowanie
Podsumowanie
W tym wątku poznałeś/łaś wiele ciekawych związków chemicznych. Uproszczony podział związków nieorganicznych przedstawiono na poniższym wykresie:

Tlenki
Tlenki to związki tlenu z innymi pierwiastkami, w których atomy tlenu występują na stopniu utlenienia. Wzór ogólny tlenków prostych ma postać:
gdzie:
– symbol dowolnego pierwiastka chemicznego;
, – odpowiednie indeksy stechiometryczne.
W poniższej tabeli zaprezentowane zostały maks. wartości stopni utlenienia pierwiastków w ich związkach z tlenem.
Tabela 1. Maksymalne wartości stopni utlenienia pierwiastków w ich związkach z tlenem.
Numer grupy | 1. | 2. | 13. | 14. | 15. | 16. | 17. |
|---|---|---|---|---|---|---|---|
Najwyższy stopień utlenienia atomów pierwiastka w tlenkach | I | II | III | IV | V | VI | VII |
Istnieje szereg metod pozwalających na otrzymanie tlenków. Większość z nich można otrzymać w wyniku bezpośredniej reakcji z tlenem, jednak do otrzymania niektórych z nich potrzebne jest użycie bardziej wyselekcjonowanych sposobów (np. dla fluorowców oraz litowców). Poniższa grafika pomoże Ci podsumować metody, w wyniku których można otrzymać tego typu związki.
Jakie tlenki można otrzymać za pomocą jakich metod? Zapoznaj się z grafiką interaktywną, która przedstawia zależności otrzymywanych tlenków za pomocą wybranych metod ich otrzymywania, a następnie stwórz własną propozycję mapy myśli, rozbudowując ją o przykłady tlenków otrzymywanych za pomocą przedstawionych metod. Swoją mapę możesz porównać z mapą umieszczoną w odpowiedzi. Potem wykonaj ćwiczenia.
Jakie tlenki można otrzymać za pomocą jakich metod? Zapoznaj się z opisem grafiki interaktywnej, która przedstawia zależności otrzymywanych tlenków za pomocą wybranych metod ich otrzymywania, a następnie stwórz wypunktowaną listę haseł, rozbudowując ją o przykłady tlenków otrzymywanych za pomocą przedstawionych metod. Swoją listę możesz porównać z mapą umieszczoną w odpowiedzi. Potem wykonaj ćwiczenia.
Stwórz własną mapę myśli
- Nazwa kategorii: Metody otrzymywania tlenków metali i niemetali
- Nazwa kategorii: Reakcja pierwiastka z tlenem
- Nazwa kategorii: Reakcja utleniania niższych tlenków
- Nazwa kategorii: Reakcja redukcji wyższych tlenków
- Nazwa kategorii: Rozkład tlenków, nadtlenków i ponadtlenków
- Nazwa kategorii: Dysproporcjonowanie tlenków
- Nazwa kategorii: Reakcja rozkładu nietrwałych soli kwasów tlenowych
- Nazwa kategorii: Rozkład nietrwałych kwasów tlenowych
- Nazwa kategorii: Reakcja rozkładu wodorotlenków
- Nazwa kategorii: Reakcja kwasu utleniającego z reduktorem
- Nazwa kategorii: Reakcja spalania związków chemicznych
- Nazwa kategorii: Reakcja analizy soli kwasów tlenowych pod wpływem temp. Koniec elementów należących do kategorii Metody otrzymywania tlenków metali i niemetali
- Elementy należące do kategorii Metody otrzymywania tlenków metali i niemetali
Stwórz wypunktowaną listę haseł dotyczącą metod otrzymywania tlenków metali i niemetali. Wykorzystaj punkty podane poniżej.
1. Reakcja pierwiastka z tlenem.
2. Reakcja utleniania niższych tlenków.
3. Reakcja redukcji wyższych tlenków.
4. Rozkład tlenków, nadtlenków i ponadtlenków.
5. Reakcja rozkładu nietrwałych soli kwasów tlenowych.
6. Dysproporcjonowanie tlenków.
7. Rozkład nietrwałych kwasów tlenowych.
8. Reakcja rozkładu wodorotlenków.
9. Reakcja kwasu utleniającego z reduktorem.
10. Reakcja spalania związków chemicznych.
11. Reakcja analizy soli kwasów tlenowych pod wpływem temperatury.
Tlenki mogą wykazywać charakter kwasowy, zasadowy, amfoteryczny lub obojętny. Takie tlenki nazywa się kolejno: kwasowymi, zasadowymi, amfoterycznymi lub obojętnymi. Aby określić, jaki charakter chemiczny wykazuje dany tlenek, należy sprawdzić czy dany tlenek reaguje z kwasem oraz czy reaguje z wodnym roztworem wodorotlenku.
- Nazwa kategorii: Charakter chemiczny tlenków
- Nazwa kategorii: Kwasowy
- Nazwa kategorii: Reagują z wodnymi roztworami wodorotlenków tworząc sole.
- Nazwa kategorii: W większości reagują z wodą tworząc odpowiednie kwasy.
- Nazwa kategorii: Tworzą sole z tlenkami zasadowymi. Koniec elementów należących do kategorii Kwasowy
- Nazwa kategorii: Zasadowy
- Nazwa kategorii: Reagują z kwasami tworząc sole.
- Nazwa kategorii: Tlenki litowców i berylowców reagują z wodą tworząc odpowiedni wodorotlenek. Koniec elementów należących do kategorii Zasadowy
- Nazwa kategorii: Amfoteryczny
- Nazwa kategorii: Reagują z kwasami i wodnymi roztworami wodorotlenków tworząc sole.
- Nazwa kategorii: Zazwyczaj nie reagują z wodą. Koniec elementów należących do kategorii Amfoteryczny
- Nazwa kategorii: Obojętny
- Nazwa kategorii: Nie reagują z kwasami, wodnymi roztworami wodorotlenków ani z wodą. Koniec elementów należących do kategorii Obojętny
- Elementy należące do kategorii Charakter chemiczny tlenków
- Elementy należące do kategorii Kwasowy
- Elementy należące do kategorii Zasadowy
- Elementy należące do kategorii Amfoteryczny
- Elementy należące do kategorii Obojętny
Wodorki
Wodorki to związki wodoru z innymi pierwiastkami. Ze względu na skład, wodorki możemy podzielić na:
wodorki niemetali – związki, w których wodór występuje na stopniu utlenienia;
wodorki metali – związki, w których wodór występuje na stopniu utlenienia.
R2BNIotMSNI6J1  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.R1NmXI1QAR7cC1 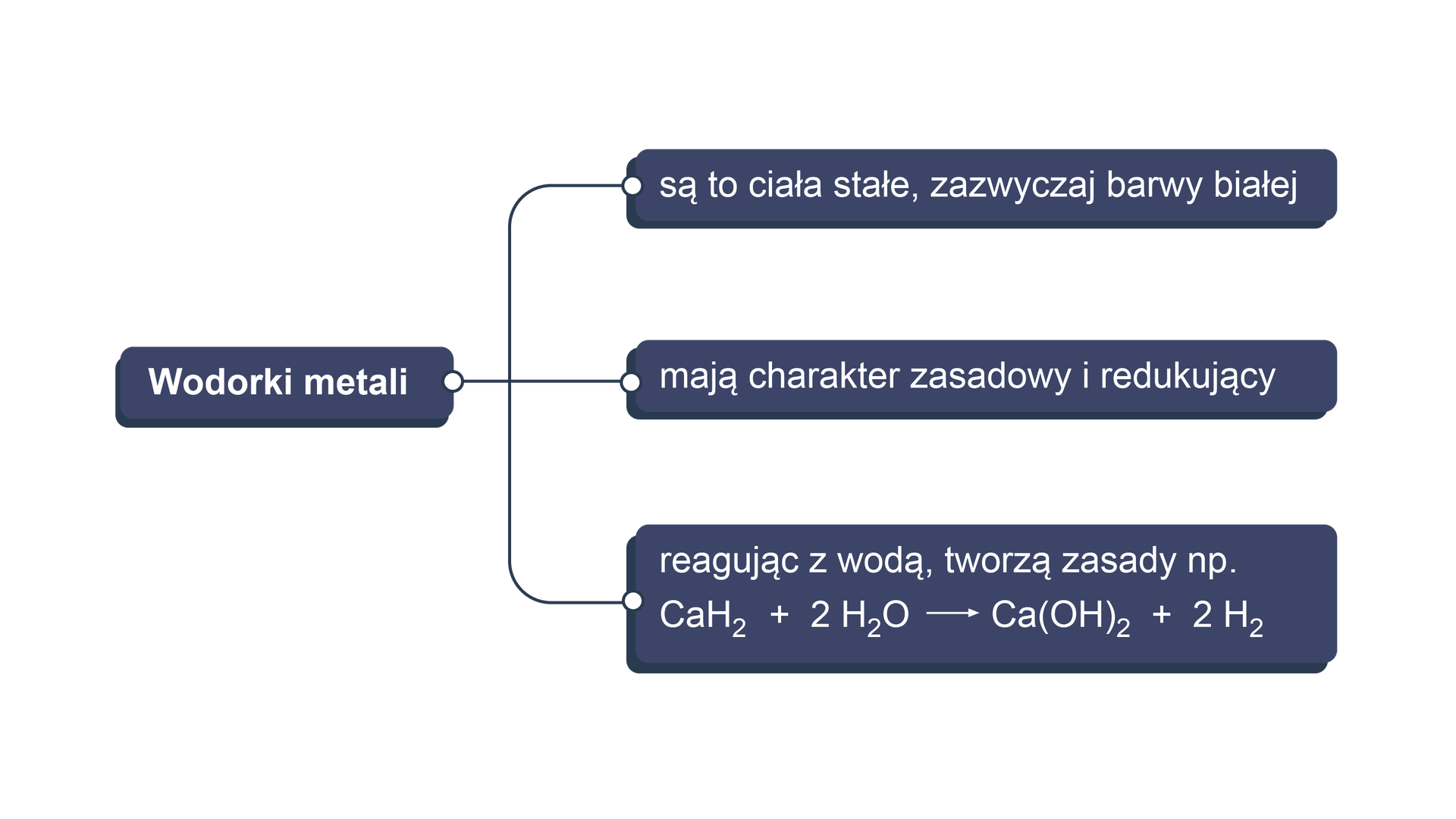 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Wodorotlenki
Wodorotlenki to związki chemiczne o budowie jonowej utworzone z kationów metalu () i anionów wodorotlenkowych (). Jony te przyciągają się w wyniku działania sił elektrostatycznych, tworząc sieć krystaliczną. Wodorotlenki nie tworzą więc cząsteczek i, jak większość związków o budowie jonowej, są substancjami o stałym stanie skupienia.
Przykładowo, sieć krystaliczna wodorotlenku sodu () zbudowana jest z kationów sodu () i anionów wodorotlenkowych ():

Nazwy wodorotlenków tworzymy przez dodanie do słowa „wodorotlenek” nazwy metalu tworzącego dany związek (w dopełniaczu), oraz – jeśli jest taka potrzeba – wartościowości metalu, jaką posiada w opisywanym wodorotlenku. Wartościowości nie podajemy w nazwach wodorotlenków metali i grupy układu okresowego oraz cynku i glinu (każdy ze wspomnianych metali, w związkach chemicznych przyjmuje tylko jedną wartościowość).
Dwie z laboratoryjnych metod otrzymywania wodorotlenków opisano na poniższym schemacie:

Metale aktywne (a więc metale i grupy układu okresowego, z wyjątkiem berylu), w większości reagują z wodą już w temperaturze pokojowej. Wyjątkiem jest magnez, który w widoczny sposób reaguje z wodą dopiero po ogrzaniu układu.
Opisanymi na schemacie metodami otrzymuje się na ogół wodorotlenki metali aktywnych dobrze rozpuszczalne w wodzie (wyjątkami są wodorotlenek magnezu i wodorotlenek wapnia, które są w wodzie trudno rozpuszczalne). A powstający w naczyniu reakcyjnym wodny roztwór wodorotlenku to zasada. Aby z tego roztworu otrzymać czysty wodorotlenek, można z niego odparować wodę.
Napisz (w formie cząsteczkowej) równania reakcji otrzymywania wodorotlenku potasu oraz wodorotlenku baru w reakcjach odpowiedniego metalu z wodą oraz odpowiedniego tlenku metalu z wodą. Nazwij reagenty każdej z reakcji.
Wybrane właściwości fizykochemiczne wodorotlenków (w temperaturze pokojowej) przedstawiono na poniższym schemacie:
Wodorotlenki rozpuszczalne w wodzie ulegają w niej procesowi dysocjacji elektrolitycznej. W procesie tym, z sieci krystalicznej odpowiedniego wodorotlenku, uwalniane są kationy odpowiedniego metalu oraz aniony wodorotlenkowe. Schemat procesu dysocjacji elektrolitycznej wodorotlenków można zapisać jako:
Np.
Np.

Kwasy
Kwasy to związki chemiczne, których cząsteczki są zbudowane z przynajmniej jednego atomu wodoru i reszty kwasowej. Wśród kwasów nieorganicznych wyróżniamy kwasy tlenowe i beztlenowe.
Wzór ogólny kwasów ma postać:
gdzie:
H – symbol atomu wodoru;
R – reszta kwasowa:
w cząsteczkach kwasów tlenowych zbudowana z atomów tlenu i atomu (a czasem atomów) pierwiastka innego niż tlen i wodór - najczęściej atomu niemetalu;
w cząsteczkach kwasów beztlenowych zbudowana z atomów niemetalu innego niż tlen i wodór;
n – indeks stechiometryczny określający liczbę atomów wodoru w cząsteczce kwasu (równy wartościowości reszty kwasowej).
Zasady nazewnictwa kwasów nieorganicznych przedstawiono na poniższym schemacie.

Metody otrzymywania kwasów nieorganicznych uzależnione są od tego, czy kwas, który chcemy otrzymać, jest kwasem tlenowym, czy beztlenowym. Wybrane metody otrzymywania kwasów opisano na poniższym schemacie.

Wybrane właściwości fizykochemiczne kwasów (w temperaturze pokojowej) przedstawiono na poniższym schemacie.
Kwasy rozpuszczalne w wodzie ulegają w niej procesowi dysocjacji elektrolitycznej. W ten sposób powstają kationy wodoru (a dokładniej – kationy oksoniowe) oraz aniony odpowiednich reszt kwasowych. Uproszczony schemat procesu dysocjacji elektrolitycznej kwasów można zapisać jako:
Jednak w rzeczywistości w roztworze wodnym nie znajdują się kationy wodoru, a tzw. kationy oksoniowe (), utworzone przez przyłączenie cząsteczki wody do kationu wodoru. Schemat procesu dysocjacji elektrolitycznej kwasów z uwzględnieniem jonów oksoniowych ma postać:
Przykładowo – uproszczony zapis procesu dysocjacji elektrolitycznej kwasu azotowego ma postać:
a z uwzględnieniem jonów oksoniowych:

Sole
Sole to związki, które w stanie stałym zbudowane są z kationów metalu (z wyjątkiem jonu ) i anionów reszty kwasowej , np.:

— oznacza liczbę kationów metalu
— oznacza liczbę anionów reszt kwasowych
Sposób klasyfikacji soli przedstawia grafika poniżej:

Istnieje wiele sposobów otrzymania soli obojętnych, które zebrano w poniższej tabeli.
Typ reakcji | Przykłady równań reakcji |
|---|---|
kwas + zasada | |
metal + kwas | |
tlenek zasadowy lub amfoteryczny + kwas | |
tlenek kwasowy + zasada | |
tlenek zasadowy + tlenek kwasowy | |
rozpuszczalna w wodzie sól + mocny kwas | |
rozpuszczalna w wodzie soli + mocna zasada | |
metal + niemetal | |
sól słabego kwasu + mocny kwas | |
rozpuszczalna w wodzie sól + rozpuszczalna w wodzie sól |
W tabeli poniżej zestawiono przykładowe sposoby otrzymywania hydroksosoli, wodorosoli i soli kompleksowych.
Typ reakcji | Przykłady równań reakcji |
|---|---|
kwas + zasada | |
metalu + kwas | |
rozpuszczalna w wodzie sól + rozpuszczalna w wodzie sól |
W ten sposób podsumowałeś/aś wiedzę z zakresu systematyki związków nieorganicznych. Aby ocenić, jak dobrze przyswoiłeś/aś ten materiał, przejdź do sekcji „Sprawdź, czego się nauczyłeś/aś”.