Przeczytaj
Niezwykłe odkrycie
Rosyjski chemik Vladimir Markovnikov w 1870 r. sformułował zasadę określającą kierunek reakcji addycji addycji do wiązania podwójnego typu węgiel−węgiel ().
Reguła ta – zwana regułą Markownikowa - mówi, że:
atom wodoru w reakcji addycji przyłącza się do atomu węgla związanego z większą liczbą atomów wodoru („bogatszego w wodór”).
Addycja chlorowodoru () do propenu, zgodna z regułą Markownikowa

O ile addycja chlorowodoru () i jodowodoru () do alkenów przebiega zgodnie z tą regułą, to większym problemem okazało się wyjaśnienie addycji bromowodoru () do danego alkenu. Naukowcy toczyli spór w tej sprawie przez wiele lat zakładając, że w reakcji powstają produkty, których struktura jest zgodna lub niezgodna z tą regułą. Inni zakładali również, że powstaje mieszanina produktów powstających w obu rozpatrywanych przypadkach.
Dopiero w 1933 r. dwaj amerykańscy naukowcy, Kharasch i Mayo, uporządkowali informacje dotyczące ścieżki reakcji z alkenami. Wykazali doświadczalnie, że na orientację tej reakcji wpływa wyłącznie obecność nadtlenkównadtlenków lub jej brak.
Kharasch i Mayo udwowodnili, że wykluczenie ze środowiska reakcji nadtlenków lub dodatek inhibitorówinhibitorów (np. hydrochinonu, tlenu lub difenyloaminy) powoduje przebieg reakcji addycji zgodnie z regułą Markownikowa, a więc zgodnie z mechanizmem addycji elektrofilowej. Jeśli jednak w mieszaninie są obecne nadtlenki, to proces przebiega rodnikoworodnikowo (przez karborodnikkarborodnik w stanie przejściowym), a orientacja przyłączenia cząsteczki jest niezgodna z regułą Markownikowa, co znane jest jako efekt nadtlenkowyefekt nadtlenkowy.
Wobec przeprowadzonych doświadczeń Kharasch i Mayo zaproponowali dwie odmienne drogi addycji bromowodoru do wiązania podwójnego.

Nadtlenki, które łamią wszelkie reguły

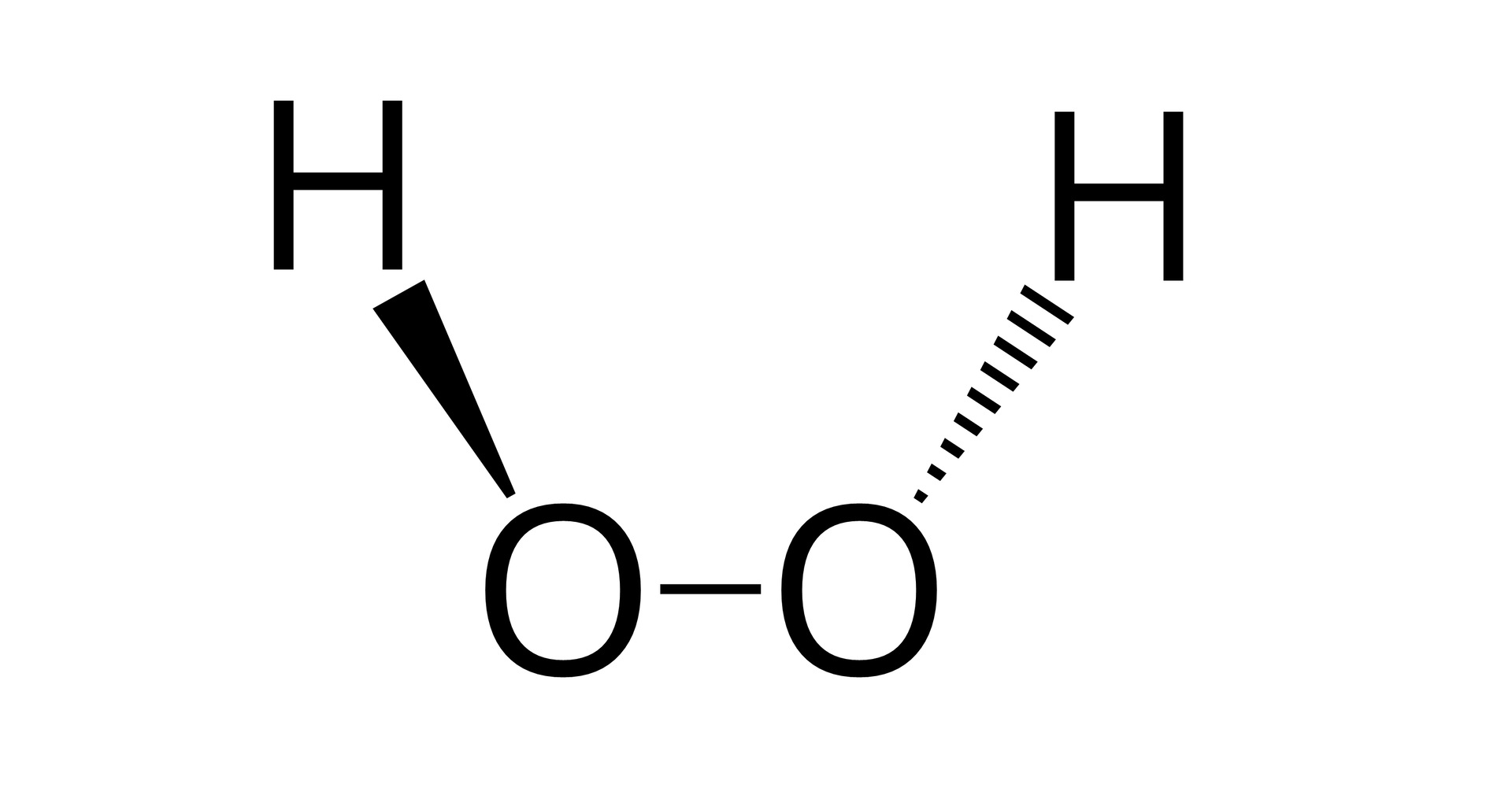
Nadtlenki to związki, które posiadają łatwo rozrywalne wiązanie pomiędzy atomami tlenu (mostek tlenowy).
W reakcjach addycji elektrofilowej, wg mechanizmu rodnikowego, najczęściej biorą udział:
Skąd w środowisku reakcji biorą się nadtlenki?
Największych ich źródłem są zanieczyszczenia związków organicznych, z których wytworzyły się na skutek działania tlenu na te związki. Niektóre nadtlenki są jednak celowo dodawane do środowiska reakcji, by uzyskać produkty otrzymywane przeciwnie do reguły Markownikowa.
Mechanizm reakcji addycji bromowodoru do alkenów inicjowanej nadtlenkami
Główną cechę mechanizmu rodnikowego stanowi fakt, że w reakcji produktem przejściowym jest wolny rodnik (karborodnik), a nie karbokationkarbokation.
Reakcja przebiega łańcuchowo i składa się z kilku etapów:
„Obecność lub brak obecności nadtlenków nie wywiera wpływu na addycję chlorowodoru, jodowodoru, kwasu siarkowego(VI) czy też wody do wiązania podwójnego. Wynika to z faktu, że etap propagacji wymaga dostarczenia energii do układu, stąd też zachodzi tak wolno, że nie tworzy się właściwy produkt.”
Źródło: Robert T. Morrison, Robert N. Boyd, Chemia organiczna, t. 1, Państwowe Wydawnictwo Naukowe, Warszawa 1985, s. 237.
Inne reakcje addycji wolnorodnikowej
Zgodnie z mechanizmem addycji rodnikowej, z alkenami (w obecności nadtlenków) reaguje również tetrachorometan (). Mechanizm tej reakcji można przedstawić w następujący sposób:

Słownik
(łac. additio „dodawanie”) reakcja przyłączania, reakcja chemiczna polegająca na przyłączaniu atomów lub grup atomów z utworzeniem cząsteczki jednego produktu (adduktu)
(łac. carbo „węgiel”, gr. katiṓn „idący w dół”) jon karboniowy, kation org., w którym dodatni ładunek wywołany deficytem elektronów jest zlokalizowany na atomie węgla
(łac. carbo „węgiel”) rodnik, w którym niesparowany elektron jest zlokalizowany na atomie węgla
związek chemiczny zawierający jon nadtlenkowy albo mostek tlenowy -, w którym atom tlenu występuje na stopniu utlenienia –I
(łac. inhibeo „wstrzymuję”) substancja, która, dodana w niewielkiej ilości do układu reagującego, powoduje zmniejszenie szybkości lub niekiedy całkowite zatrzymanie reakcji chemicznej
odmienna orientacja reakcji addycji spowodowana obecnością nadtlenków
indywiduum zbudowane z jednego lub powiązanych ze sobą atomów, z niesparowanym elektronem na powłoce walencyjnej jednego z atomów
Bibliografia
Encyklopedia PWN
Majewski W., Mechanizmy reakcji organicznych, Lublin 2012.
Morrison R. T., Boyd R. N., Chemia organiczna, tłum. W. Antkowiak i in., Warszawa 1985, t. 1‑2.
Vollhardt P., Schore N. E., Organic Chemistry structure and function, New York 2007, wyd. 6.