Przeczytaj
Istota i lokalizacja fosforylacji oksydacyjnej
Ilość energii potrzebna mężczyźnie ważącemu 70 kg i prowadzącemu tryb życia o umiarkowanej intensywności to aż 8400 kJ (2000 kcal) dziennie. Dostarczenie tak dużej porcji energii wymaga 83 kg ATP. Jednakże w organizmie człowieka w danym momencie ilość ATP wynosi zaledwie 250 g. Na szczęście różnica między ogólnie wymaganą ilością ATP a tą, którą dysponujemy w danym momencie, nie jest problemem, ponieważ ADP jest ponownie wykorzystywany do syntezy ATP. Każda cząsteczka ATP jest odzyskiwana około 300 razy dziennie, dzięki procesowi fosforylacji oksydacyjnejfosforylacji oksydacyjnej.
Fosforylacja oksydacyjna u organizmów eukariotycznych zachodzi w wewnętrznej błonie mitochondrialnej, natomiast u prokariontów – w ich błonie komórkowej.
Wytworzenie ATP na drodze fosforylacji oksydacyjnej jest reakcją egzoenergetyczną, którą można zapisać w postaci następującego równania:
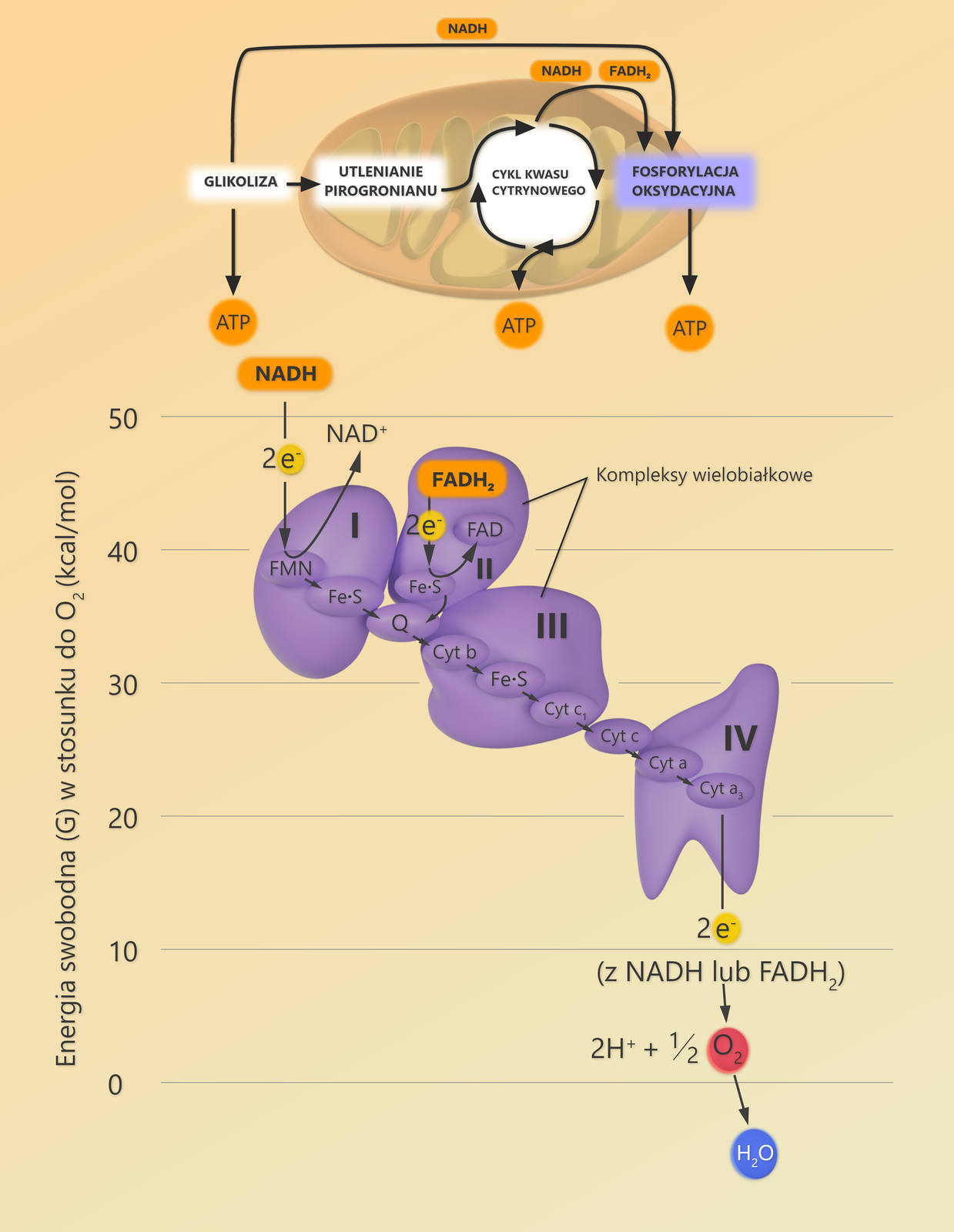
W błonie wewnętrznej mitochondriów znajdują się zespoły (kompleksy) związków chemicznych uszeregowanych zgodnie ze wzrastającym potencjałem oksydoredukcyjnym i coraz większą elektroujemnością. Związki te tworzą łańcuch oddechowyłańcuch oddechowy. Potencjał oksydoredukcyjny, nazywany też potencjałem redoks, to zdolność danego związku chemicznego do przyjmowania i oddawania elektronów. W łańcuchu oddechowym elektrony są transportowane od związków bardziej zredukowanych do tych o większym stopniu utlenienia, by ostatecznie dotrzeć do cząsteczki tlenu o największej elektroujemności.
NADH i , czyli zredukowane formy uniwersalnych przenośników protonów i elektronówuniwersalnych przenośników protonów i elektronów, otrzymywane podczas glikolizyglikolizy, reakcji pomostowejreakcji pomostowej oraz cyklu Krebsacyklu Krebsa, są utleniane przez składniki łańcucha oddechowego. Elektrony pochodzące z NADH i są przenoszone przez zakotwiczone w błonie wewnętrznej mitochondrium składniki łańcucha oddechowego, uszeregowane zgodnie ze wzrastającą elektroujemnością.
Transport elektronów w łańcuchu kończy się, gdy zostaną one przekazane na tlen – cząsteczkę o największej elektroujemności.
W wyniku takiego uporządkowanego przepływu elektronów wzdłuż błony wewnętrznej mitochondriów, uwolniona zostaje energia, która wykorzystana jest do przepompowania protonów (jonów HIndeks górny ++) w poprzek tej błony – z matriks mitochondrium do przestrzeni międzybłonowej (perimitochondrialnej).
W wyniku tego procesu dochodzi do kumulacji jonów HIndeks górny ++ w przestrzeni międzybłonowej. Łańcuch oddechowy umożliwia więc wytworzenie gradientu stężeń protonów, których energia jest następnie wykorzystana do syntezy ATP.
Składniki łańcucha oddechowego
Wewnętrzna błona mitochondrialna tworzy fałdy – grzebienie mitochondrialne. Znacznie zwiększają one powierzchnię, na której znajdują się składniki łańcucha oddechowego.
W skład łańcucha oddechowego wchodzą cztery kompleksy białkowe. Są to trzy pompy protonowe o nazwach: oksydoreduktaza NADH‑Q (kompleks I), nazywana dehydrogenazą NADH, oksydoreduktaza Q–cytochrom c (kompleks III) i oksydaza cytochromu c (oksydaza cytochromowa, kompleks IV), oraz wielki kompleks białkowy reduktaza bursztynian–Q (kompleks II), który jest bezpośrednio związany z cyklem Krebsa. Połączone kompleksy I, III i IV tworzą kompleks wielkocząsteczkowy (supramolekularny) – respirasom. Ułatwia on szybkie przenoszenie elektronów ze zredukowanych substratów, a także zapobiega uwalnianiu pośrednich form reakcji.
Elektrony są transportowane pomiędzy danymi kompleksami przez dwa specjalne nośniki elektronów: koenzym Q, nazywany również ubichinonemubichinonem, oraz cytochrom c. W transporcie elektronów w łańcuchu oddechowym można wyróżnić cztery etapy.
Synteza ATP
W 1961 r. brytyjski biochemik Peter Mitchell wysunął tzw. hipotezę chemiosmotyczną, mówiącą, że transport elektronów i synteza ATP są ze sobą sprzężone. Dzieje się tak dzięki utworzonemu w poprzek wewnętrznej błony mitochondrialnej gradientowi protonowemu. Przenoszenie elektronów wzdłuż łańcucha oddechowego prowadzi do pompowania protonów ze strony matriks na stronę cytoplazmatyczną wewnętrznej błony mitochondrialnej. Stężenie HIndeks górny ++ w matriks maleje, rośnie zaś w przestrzeni międzybłonowej, co prowadzi do powstania gradientu elektrochemicznego. Wówczas protony z powrotem przepływają do matriks, dzięki czemu ich stężenie w poprzek błony zostaje wyrównane. Taki przepływ protonów napędza syntezę ATP przez syntazę ATP (kompleks V). Efekt korzystnego energetycznie nierównomiernego rozłożenia protonów nazywa się siłą protonomotoryczną. Ma ona dwie składowe: gradient elektryczny i chemiczny. Hipoteza Mitchella została potwierdzona eksperymentalnie.
Początkowo hipoteza chemiosmotyczna Mitchella nie została przyjęta zbyt entuzjastycznie. Jeden z naukowców zajmujących się syntazą ATP, Efraim Racker, wspominał, że część badaczy uważała Mitchella za „nadwornego błazna”, którego praca nie ma żadnego znaczenia. Obecnie jednak odkrycie zjawiska napędzania reakcji syntazy ATP przez gradient protonowy uznaje się za jedno z dwóch (obok poznania struktury DNA) najważniejszych odkryć biologicznych XX w. W 1978 r. Peter Mitchell został uhonorowany Nagrodą Nobla w dziedzinie chemii.
Więcej o syntezie ATP dowiesz się z e‑materiału pt. Sposoby syntezy ATP w komórce.
Znane wszystkim trucizny, takie jak cyjanekcyjanek czy tlenek węgla, działają szkodliwie na nasz organizm, hamując aktywność enzymu oksydazy cytochromu c. Prowadzi to do zatrzymania reakcji łańcucha oddechowego.
Słownik
sole kwasu cyjanowodorowego; ich niekorzystny wpływ na organizm wynika z wiązania się z atomami miedzi i żelaza, które wchodzą w skład enzymów łańcucha oddechowego
cykl kwasu cytrynowego, w którym substrat, jakim jest acetylokoenzym A, zostaje utleniony do COIndeks dolny 22 w wyniku wielu przemian biochemicznych
białka złożone, hemoproteiny, które dzięki odwracalnej zmianie stopnia utlenienia żelaza grupy hemowej (z FeIndeks górny 2+2+ na FeIndeks górny 3+3+) stanowią układ przenośników elektronów w łańcuchu oddechowym u roślin i zwierząt
grupa enzymów zdolna do odszczepienia atomów wodoru od związków organicznych
zdolność do wykonania pracy bez zmiany temperatury i ciśnienia układu
proces syntezy ATP w warunkach tlenowych z wykorzystaniem łańcucha oddechowego
(gr. glik – słodki; lysis – rozpuszczanie) szlak metaboliczny, w którym na skutek wielu reakcji biochemicznych z jednej cząsteczki glukozy powstają: dwie cząsteczki pirogronianu, dwie cząsteczki ATP, dwie cząsteczki NADH oraz cząsteczka wody
zespół enzymatycznych reakcji oksydacyjno‑redukcyjnych zachodzących w wewnętrznej błonie mitochondrium u organizmów eukariotycznych, natomiast u bakterii – w błonie plazmatycznej, katalizowany przez białkowe przenośniki elektronów zawierające: flawiny, centra żelazo‑siarkowe i hemy jako grupy prostetyczne
białko błonowe zdolne do transportowania protonów (HIndeks górny ++) wbrew ich gradientowi stężeń
oksydacyjna dekarboksylacja pirogronianu – reakcja odłączania dwutlenku węgla od cząsteczki pirogronianu z jego jednoczesną dehydrogenacją i przyłączeniem powstałej reszty acetylowej do koenzymu A, w wyniku czego tworzy się acetylokoenzym A
enzym katalizujący reakcję wytwarzania ATP z ADP i fosforanu nieorganicznego
chinon będący specjalnym nośnikiem elektronów; przenosi elektrony między odpowiednimi kompleksami w łańcuchu oddechowym
, czyli forma utleniona dinukleotydu nikotynoamidoadeninowego, oraz FAD, czyli forma utleniona nukleotydu flawinoadeninowego – związki organiczne, które są akceptorami protonów i elektronów