Przeczytaj
Alotropia siarki
Siarka jest pierwiastkiem chemicznym (S), który zajmuje miejsce pod względem rozpowszechnienia w skorupie ziemskiej, oraz niemetalem, znajdującym się w okresie i grupie układu okresowego pierwiastków (tlenowce).
Siarka w przyrodzie występuje zarówno w stanie rodzimymrodzimym, jak i pod postacią licznych minerałów, tzw. siarczków (piryt, cynober, blenda cynkowa) oraz siarczanów (gips, celestyn, anhydryt). Ponadto posiada wiele różnych odmian alotropowychalotropowych, z których najlepiej znane są siarka rombowasiarka rombowa i siarka jednoskośnasiarka jednoskośna. Alotropią nazywa się występowanie tego samego pierwiastka chemicznego w dwóch lub więcej formach. Właściwość występowania w licznych odmianach, w stanie stałym i ciekłym, jest związana ze zdolnością siarki elementarnejsiarki elementarnej do tworzenia cząsteczek o pierścieniowym lub łańcuchowym układzie atomów.

Na świecie istnieje wiele miejsc, w których ludzie zajmują się eksploatacją złóż siarki. Występują one m.in.: w Polsce, USA, na Ukrainie oraz Sycylii. Jednym z takich miejsc jest malowniczy wulkan Kawah Ijen, położony na wysokości ok. , we wschodniej części Jawy w Indonezji. Ze zboczy wulkanu wypływa siarka i zastyga na powietrzu. W nocy można zaobserwować niebieskie płomienie spalającego się pierwiastka. Mężczyźni zarabiający tam na życie wykonują jeden z trudniejszych zawodów świata. Wyłamują bowiem płaty skondensowanej siarki, umieszczają je w dwóch koszach połączonych pałąkiem, a następnie pokonując długą oraz niebezpieczną trasę po krawędzi krateru, zmierzają do punktu skupu. Ładunek, który noszą trzy razy dziennie, waży . Ze względu na trujące opary (nie stać ich niestety na odpowiednie maski ochronne) i trudne warunki pracy, ludzie trudzący się tym fachem żyją znacznie krócej.
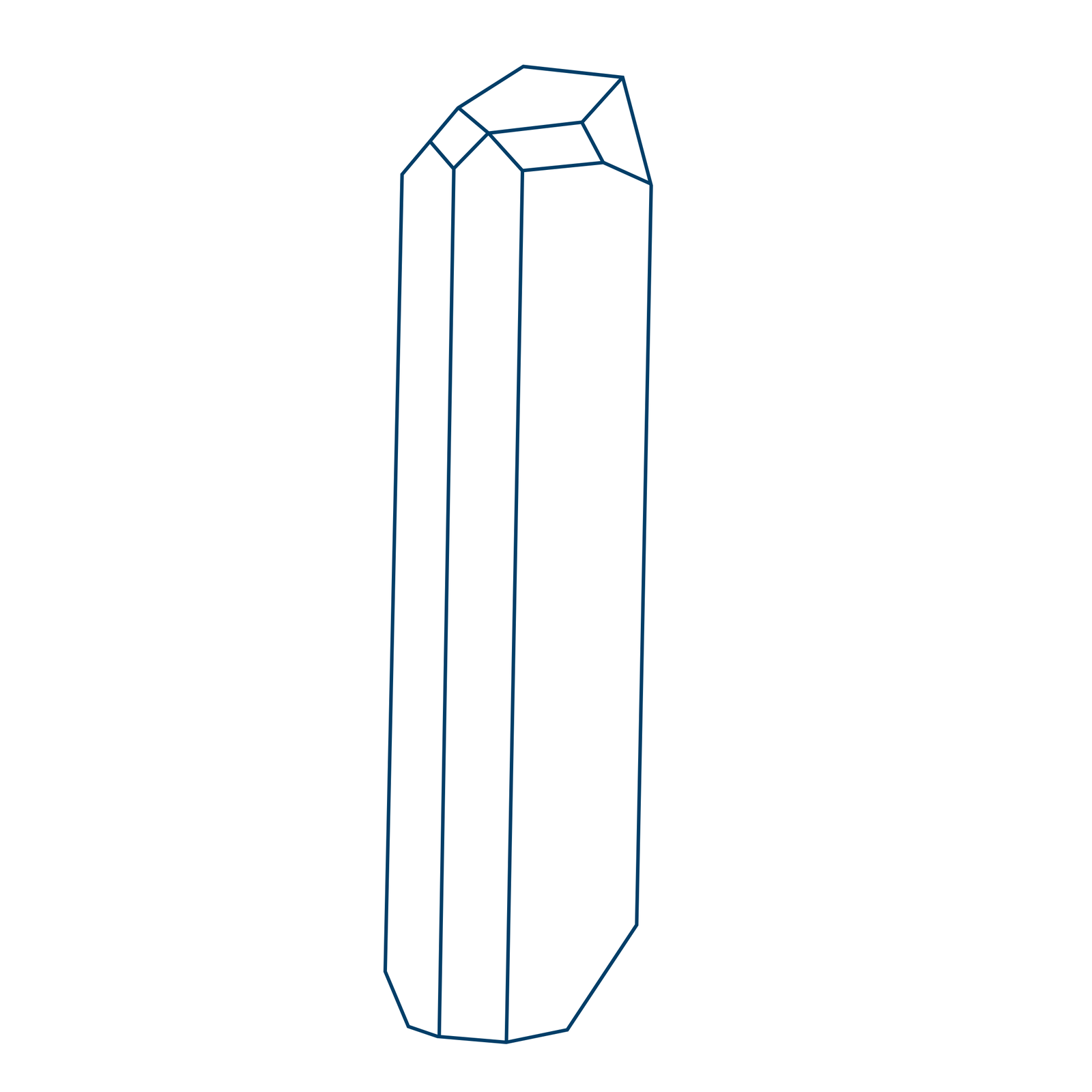
Siarka rombowa

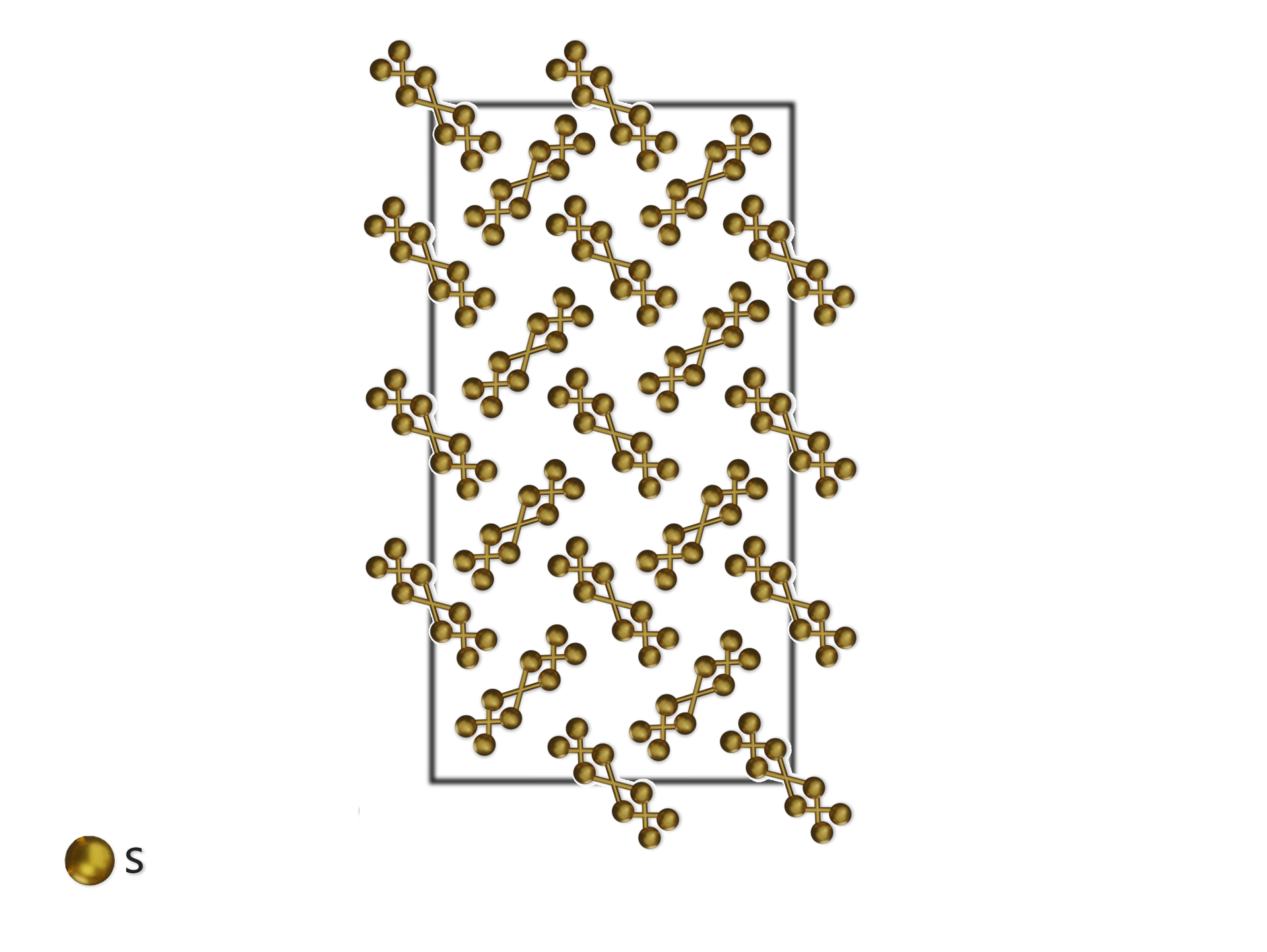
Siarka rombowa () jest jasnożółtą odmianą alotropową, trwałą w temperaturze pokojowej i występującą naturalnie w przyrodzie. Posiada strukturę zygzakowatego pierścienia (przypominającego kształtem koronę), złożoną z ośmiu atomów siarki . Wszystkie długości wiązań w pierścieniu wynoszą , kąty 107,8°, a kąty dwuściennekąty dwuścienne 98°.
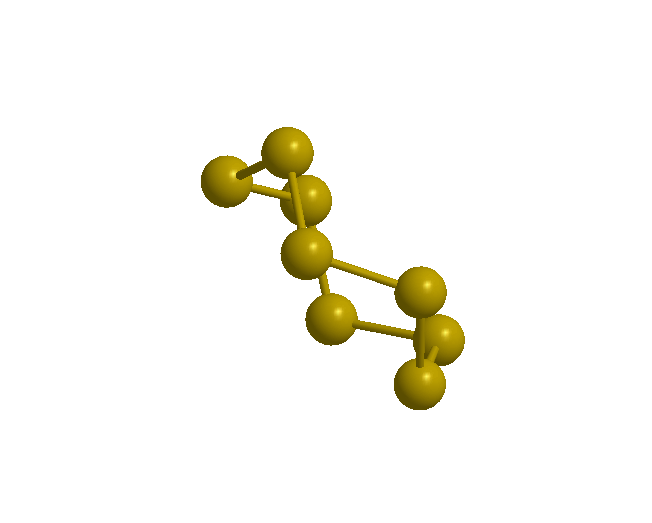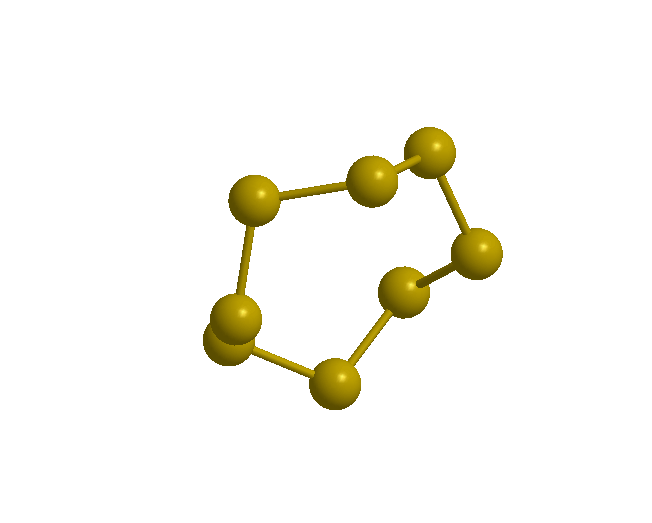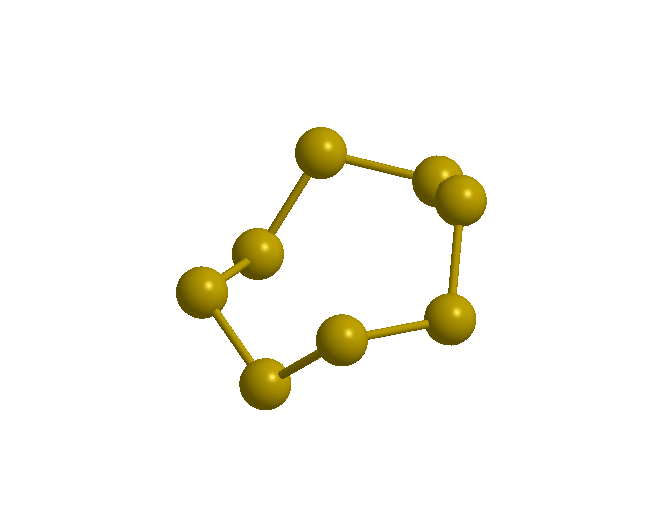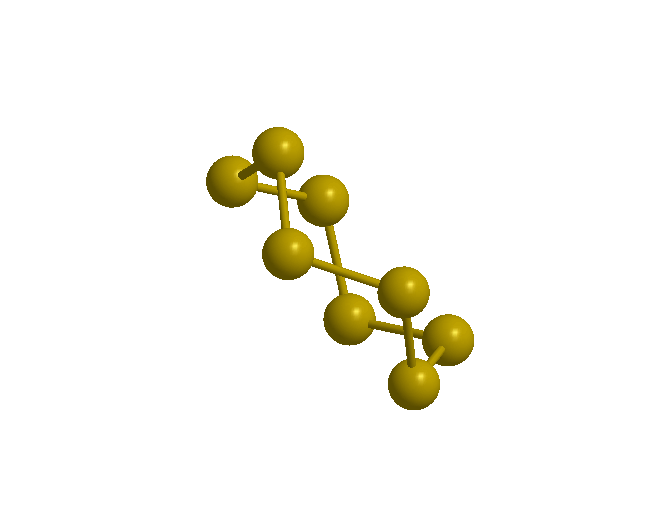
Forma ta jest nierozpuszczalna w wodzie, słabo rozpuszczalna w alkoholu i benzenie, za to lepiej rozpuszcza się w dwusiarczku węgla. Jest dobrym izolatorem elektrycznym i słabym przewodnikiem ciepła.
Siarka jednoskośna
Siarka jednoskośna () powstaje na skutek ogrzewania siarki rombowej w . Ta odmiana alotropowa topi się w temperaturze i posiada mniejszą gęstość niż siarka . Podobnie jak siarka rombowa, posiada strukturę zygzakowatego pierścienia, złożoną z ośmiu atomów siarki . Różni się tylko sposobem upakowania pierścieni w krysztale. Posiada analogiczną rozpuszczalność i właściwości jak siarka .
Inne odmiany alotropowe siarki
Analizując diagram fazowy siarki można wywnioskować, że podczas dostatecznie szybkiego ogrzewania (powyżej 368,8 K) siarki rombowej można od razu otrzymać stopioną siarkę (ciecz) bez produktu pośredniego w postaci siarki jednoskośnej i tym samym w przypadku dostatecznie szybkiego chłodzenia (poniżej 392,2 K) ciekłej siarki doprowadzić ją bezpośrednio do postaci siarki rombowej.
Siarka wrze w temperaturze 444,65°C (717,8 K) wydzielając pomarańczowe opary cząsteczek S8., 2. ŹÓŁTA CIECZ W wyniku dalszego ogrzewania żółta ciecz gęstnieje (konsystencja gęstego syropu) i ciemnieje. Powstaje ciekła siarka., 3. CIEKŁA SIARKA Powstała ciekła siarka składa się z cząsteczek cyklo-oktasiarki znajdujących się w równowadze z siarką łańcuchową (katena-oktasiarka).
Gdy w stanie równowagi w temperaturze 113,85°C (387 K) cztery procent cyklicznej siarki ulegnie przemianie w siarkę łańcuchową, obserwuje się tzw. naturalny punkt krzepnięcia siarki.
Dalsze ogrzewanie powoduje pękanie pierścieni oktasiarki i prowadzi do powstawania długich łańcuchowych struktur (katenacja) zawierających 105 jednostek S8. Tę siarkę nazywa się katena-polisiarką (Sµ)., 4. keta-polisiarka W maksymalnej dla niej temperaturze (ok. 166,85°C, czyli 440 K) przyjmuje ona barwę czerwonobrunatną i ma znacznie wyższą lepkość (2000‑krotność). Powyżej temperatury 196,85°C (470 K) następuje pękanie długich struktur katena-polisiarki.
Gwałtowne jej ochłodzenie w wodzie pozwala na otrzymanie bezpostaciowej brunatnej masy o konsystencji przypominającej kauczuk – tzw. siarka plastyczna.
Siarka µ jest nierozpuszczalna w dwusiarczku węgla., 5. SIARKA PLASTYCZNA
NIETRWAŁA Siarka plastyczna jest kolejnym przykładem nietrwałej odmiany alotropowej siarki, która po upływie kilku dni ulegnie przemianie w siarkę jednoskośną., 6. SIARKA JEDNOSKOŚNA Po upływie kilku dni siarka jednoskośna (Sβ) ulega przemianie w siarkę rombową. Reakcję tę możemy odwrócić ogrzewając siarkę rombową w temperaturze 95,6°C (368,75 K).
Innymi przykładami nietrwałych odmian alotropowych siarki są:
(cyklo-heksasiarka);
(cyklo-heptasiarka);
(cyklo-dekasiarka);
(cyklo-dodekasiarka);
(cyklo-oktadekasiarka);
(cyklo-ikozasiarka).
Wszystkie te formy charakteryzują się zmniejszoną trwałością termiczną i zwiększoną aktywnością chemiczną w porównaniu do cyklo-oktasiarki.
Występowanie trwałych odmian siarki w pewnych zakresach temperatur i ciśnienia oraz przemiany siarki rombowej w jednoskośną i/lub jednoskośnej w ciecz, można przedstawiać przy użyciu diagramu fazowegodiagramu fazowego.
Taki diagram ilustruje zależność istnienia faz układu w zależności od ciśnienia i temperatury. Obecne na tym wykresie linie graniczne opisują stany równowagi między odpowiednimi fazami, tzn.:
ciało stałe – gaz;
ciało stałe – ciecz;
gaz – ciecz.
Na wykresie występuje również punkt (punkt potrójny), który wyznacza warunki współistnienia trzech faz równocześnie. Ważne w tym aspekcie są również pojęcia ciśnienia krytycznego oraz temperatury krytycznej.
Analizując diagram fazowy siarki, można wywnioskować, że podczas dostatecznie szybkiego ogrzewania (powyżej ) siarki rombowej można od razu otrzymać stopioną siarkę (ciecz) bez produktu pośredniego w postaci siarki jednoskośnej, i tym samym, w przypadku dostatecznie szybkiego chłodzenia (poniżej ) ciekłej siarki, doprowadzić ją bezpośrednio do postaci siarki rombowej.
Wykres fazowy posiada krzywe, na których punkty podają warunki współistnienia różnych form siarki. Przykładowo:
krzywa AB podaje warunki współwystępowania siarki rombowej z parą;
krzywa BC podaje warunki współwystępowania siarki jednoskośnej z parą;
krzywa CD podaje warunki współwystępowania siarki ciekłej z parą.
Analogicznie, punkty, leżące na przecięciu krzywych, wyznaczają warunki, w których współistnieją trzy różne formy siarki. Przykładowo:
warunki, wyznaczone przez punkt B, sugerują współistnienie siarki rombowej, jednoskośnej oraz par siarki;
punkt F, wyznaczony przez krzywe równowag pozornych, powstałych z przedłużenia krzywych AB, CD (linia przerywane), świadczy o istnieniu nietrwałych faz: siarki rombowej, ciekłej oraz pary siarki. Wyznacza także warunki topnienia siarki rombowej.
Słownik
(gr. állos „obcy”, „inny”, trópos „sposób”, „postać”) występowanie tego samego pierwiastka chemicznego w dwóch lub więcej odmianach, znajdującego się w tym samym stanie skupienia
inaczej – wykres fazowy; krzywe opisujące równowagę termodynamiczną współistniejących ze sobą różnych faz układu; zawiera informacje na temat warunków współistnienia, w których zawarte są jednocześnie różne fazy układu
powstawanie wiązań chemicznych pomiędzy atomami tego samego pierwiastka
stan układu termodynamicznego, w którym makroskopowe przepływy (np. substancji, ciepła) i parametry układu (np. ciśnienie, temperatura, energia wewnętrzna) nie zmieniają się w czasie
minerał naturalnie występujący w przyrodzie
alotropowa, jasnożółta odmiana siarki, trwała w temperaturze pokojowej, nazywana siarką alfa (), złożona z ośmioatomowych () cząsteczek cyklo‑oktasiarki
alotropowa, jasnożółta odmiana siarki, nietrwała w temperaturze pokojowej, nazywana siarką beta (), złożona z ośmioatomowych () cząsteczek cyklo-oktasiarki, ułożonych inaczej w krysztale niż siarka rombowa
siarka w postaci pierwiastkowej
kąt utworzony przez dwie różne półpłaszczyzny o wspólnej krawędzi
Bibliografia
Bielański A., Podstawy chemii nieorganicznej, Warszawa 1994.
Encyklopedia PWN
Hejwowska S., Marcinkowski R., Chemia ogólna i nieorganiczna, Gdynia 2005.