Przeczytaj
Czym są metale?
(gr. muέtaualfalambdalambdaomicronnu „kopalnia”, „szyb”, „kamieniołom”) – pierwiastki chemiczne, w których występuje wiązanie metaliczne. W sieci krystalicznej metali występują niezwiązane elektrony (elektrony swobodne). Metale stanowią zdecydowaną większość pierwiastków w układzie okresowym pierwiastków (94 ze 118).
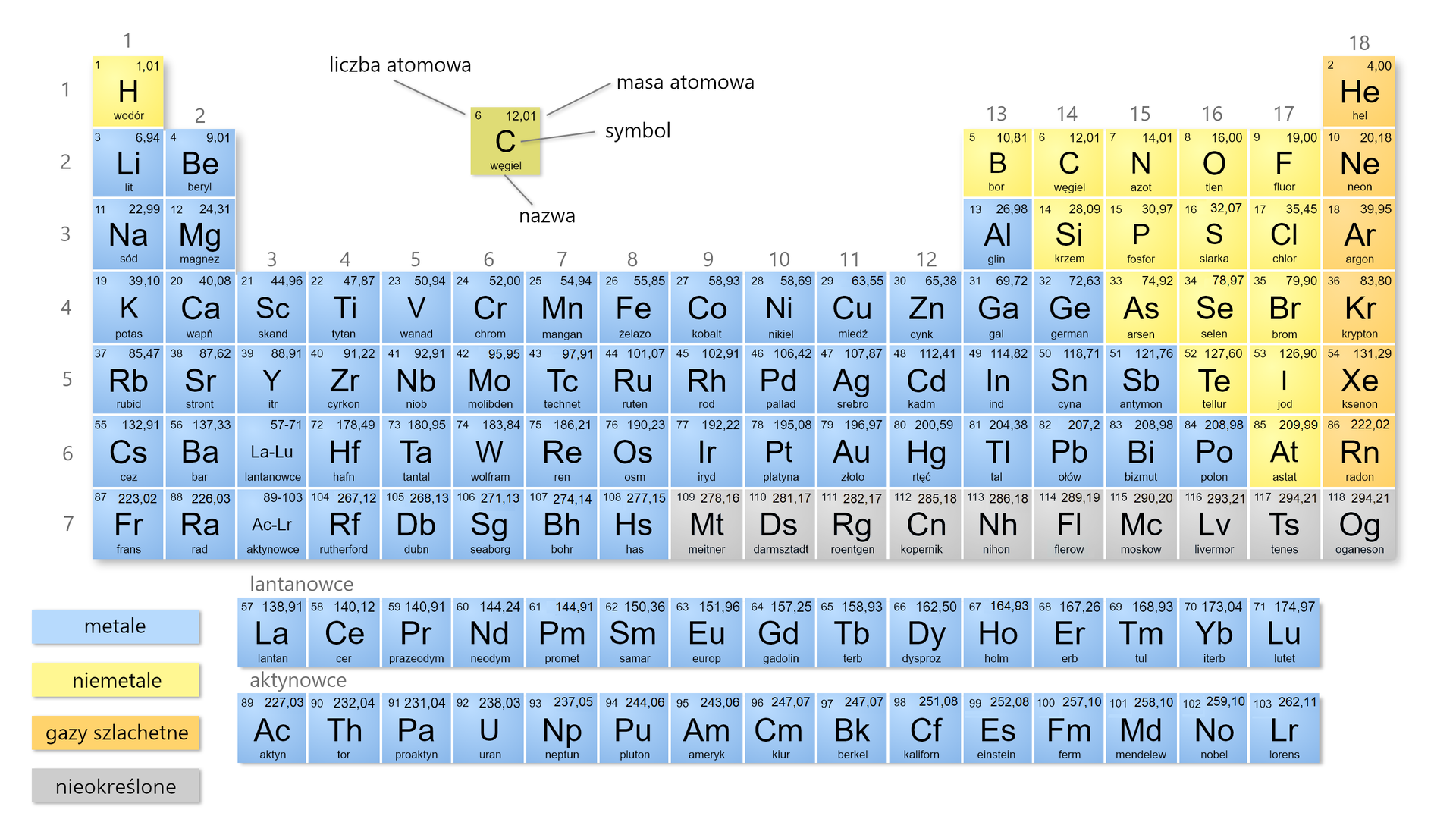
Pierwiastki chemiczne, należące do tej grupy, charakteryzują specyficzne właściwości:
-
Właściwości metali
-
Przewodzą prąd[br]elektryczny (dzięki[br]obecności wolnych[br]elektronów w sieci[br] krystalicznej)
-
Przewodzą ciepło
-
Posiadają połysk
-
Są ciągliwe i kowalne
-
Zastosowania metali w życiu codziennym
Metale jako przewodniki prądu elektrycznego
Ze względu na bardzo dobre właściwości przewodzące, metale wykorzystuje się w elektronice oraz przy produkcji różnego rodzaju kabli. Najczęściej w tym celu stosuje się metale 11 grupy układu okresowego – miedziowce. Miedź, srebro oraz złoto, ze względu na obecność elektronów o dużej ruchliwości, posiadają niezapełnioną podpowłokę s.
Konfiguracja powłoki walencyjnej miedziowców: ndIndeks górny 1010(n+1)sIndeks górny 11.

Metale jako źródło energii
Niektóre metale mogą być źródłem energii. Do takich należy chociażby uran. Jest to radioaktywny pierwiastek, którego rozpadowi towarzyszy powstanie dużej ilości energii, która później jest wykorzystywana do generowania pary wodnej. Ta z kolei, napędzając turbiny, generuje prąd elektryczny. Jeden gram uranu może dostarczyć około 2,010Indeks górny 1010 J energii, co odpowiada spaleniu 1,5 t węgla. W tym procesie wykorzystuje się izotopizotop uranu . Naturalnie występuje on w uranie tylko w 0,7%. W reaktorach jądrowych zachodzi odpowiednia reakcja:

Rozszczepienie, czyli rozpad jądra atomu uranu następuje na skutek zderzenia z neutronami. W wyniku tej reakcji powstają dwa mniejsze jądra: atomów baru () i kryptonu () oraz 3 neutrony, które mogą rozszczepiać kolejne jądra atomów uranu.
Mimo niskiego kosztu energii jądrowej, pojawia się problem ze składowaniem jej radioaktywnych odpadów, powstałych w trakcie tego procesu. Mają one bardzo długi okres połowicznego rozpadu, przez co będą nam towarzyszyć jeszcze przez wiele lat. Takie odpady muszą być magazynowane w taki sposób, aby nie nastąpił ich wyciek do środowiska.
Metale jako materiały konstrukcyjne
Ze względu na swoją trwałość, kowalność i ciągliwość są wykorzystywane w budownictwie. Już w starożytności metale oraz ich stopy były wykorzystywane do konstrukcji np. sieci wodociągowych w starożytnym Rzymie czy do odlewania figur bogów i mitologicznych postaci. Z metali wykonuje się również obudowy samochodów czy pokrycia dachów. Odpowiednio dobrane są odporne na korozję, a ponadto są stosunkowo tanie i łatwe w obróbce.
-

Licencja: domena publiczna [online], dostępny w internecie: www.pixabay.com
Wieża Eiffla jest wykonana praktycznie całkowicie z metali. -

Licencja: domena publiczna [online], dostępny w internecie: www.pixabay.com
Rzeźby wykonane z metali
Metale jako katalizatory reakcji chemicznych
Wszystkie współczesne samochody spalinowe posiadają katalizatorykatalizatory samochodowe (reaktory katalityczne). Pełnią one bardzo istotną rolę, a mianowicie przekształcają szkodliwe dla środowiska związki chemiczne na takie, które są mniej szkodliwe lub przynajmniej neutralne, np.:
W katalizatorach samochodowych możemy odnaleźć metale, takie jak platyna czy pallad. Dzięki wysokiej trwałości tych metali, mogą służyć przez dłuższy czas swoim właścicielom, a po upływie pewnego czasu da się je w odpowiedni sposób zregenerować lub poddawać recyklingowirecyklingowi.
Katalizatory metaliczne możemy odnaleźć również przy innych ważnych procesach, jak np. uwodornianie nienasyconych kwasów tłuszczowych pochodzenia roślinnego (utwardzanie tłuszczów) przy użyciu katalizatorów niklowych. Innym przykładem może być reakcja syntezy amoniaku z pierwiastków, zachodząca na metalicznym żelazie pełniącym funkcję katalizatora.
We wszystkich powyższych reakcjach mamy do czynienia z katalizą heterogeniczną, co oznacza, że katalizator jest w innej fazie aniżeli pozostałe reagenty.
Podsumowanie
Metale możemy odnaleźć w praktycznie każdej dziedzinie życia. Wszystkie urządzenia elektroniczne mają metaliczne podzespoły. Wiele sprzętów użytku codziennego również wykonana jest z wielu rodzajów metali. Tory kolejowe, które umożliwiają nam transport pomiędzy miastami, także są wykonane z kilku stopów. Rozejrzyj się dookoła, a na pewno znajdziesz kolejnych jeszcze kilka przykładów metali wokół siebie.
Słownik
jądro tego samego pierwiastka, które posiada tę samą liczbę atomową, ale różną liczbę masową
substancja przyspieszająca przebieg reakcji chemicznej, która tym samym nie zużywa się w jej trakcie
przekształcanie odpadów w nowe materiały i przedmioty
elektrony znajdujące się na ostatniej zewnętrznej powłoce
Bibliografia
Atkins, P., Jones L., Laverman L., Chemical Principles, 7th Edition, New York 2016.
Bielański A., Podstawy chemii nieorganicznej, t. 2, Warszawa 2012.
Greenwood N. N., Earnshaw A., Chemistry of the Elements, Second Edition, Oksford 1997.
Kaspar J., Fornasiero P., Hickey N., Automotive Catalytic Converters: Current Status and Some Perspectives, „Catalysis Today” 2003, t. 77, nr 4, s. 419–449.