Przeczytaj
Translacja
TranslacjaTranslacja to proces biosyntezy białek na matrycy mRNA powstającego w jądrze komórkowym. Wynikiem translacji jest „przetłumaczenie” informacji genetycznej zawartej w DNA na sekwencję aminokwasów w białku (peptydzie).
Proces translacji przebiega zgodnie z centralnym dogmatem biologii molekularnej, który zakłada przepływ informacji genetycznej z DNA przez RNA do białka.
Proces translacji katalizowany jest przez rybosomy, które zlokalizowane są w cytoplazmie lub na błonach siateczki endoplazmatycznej szorstkiej. Do prawidłowego przebiegu translacji oprócz rybosomów niezbędne są:
mRNA – matrycowe RNA, na podstawie którego odczytywana jest informacja o sekwencji aminokwasów w łańcuchu polipeptydowym;
aminokwasy białkowe – 20 różnych aminokwasów wchodzących w skład białek;
tRNA – transportujący/transferowy RNA, czyli cząsteczki RNA, które mają za zadanie wiązanie wolnych aminokwasów w cytoplazmie i ich transport do rybosomów;
czynniki inicjacji, elongacji i terminacji translacji – białka lub kompleksy białkowe odpowiedzialne za procesy translacji na każdym z jej etapów;
GTPGTP – źródło energii.
Trzy etapy translacji
Wyrodrębnia się trzy etapy translacji: inicjację, elongację i terminację.
Inicjacja (rozpoczęcie translacji)
Pierwszym z etapów translacji jest inicjacja, czyli złożenie maszynerii translacyjnej oraz rozpoznanie kodonukodonu AUG (kodon START) na nici mRNA.
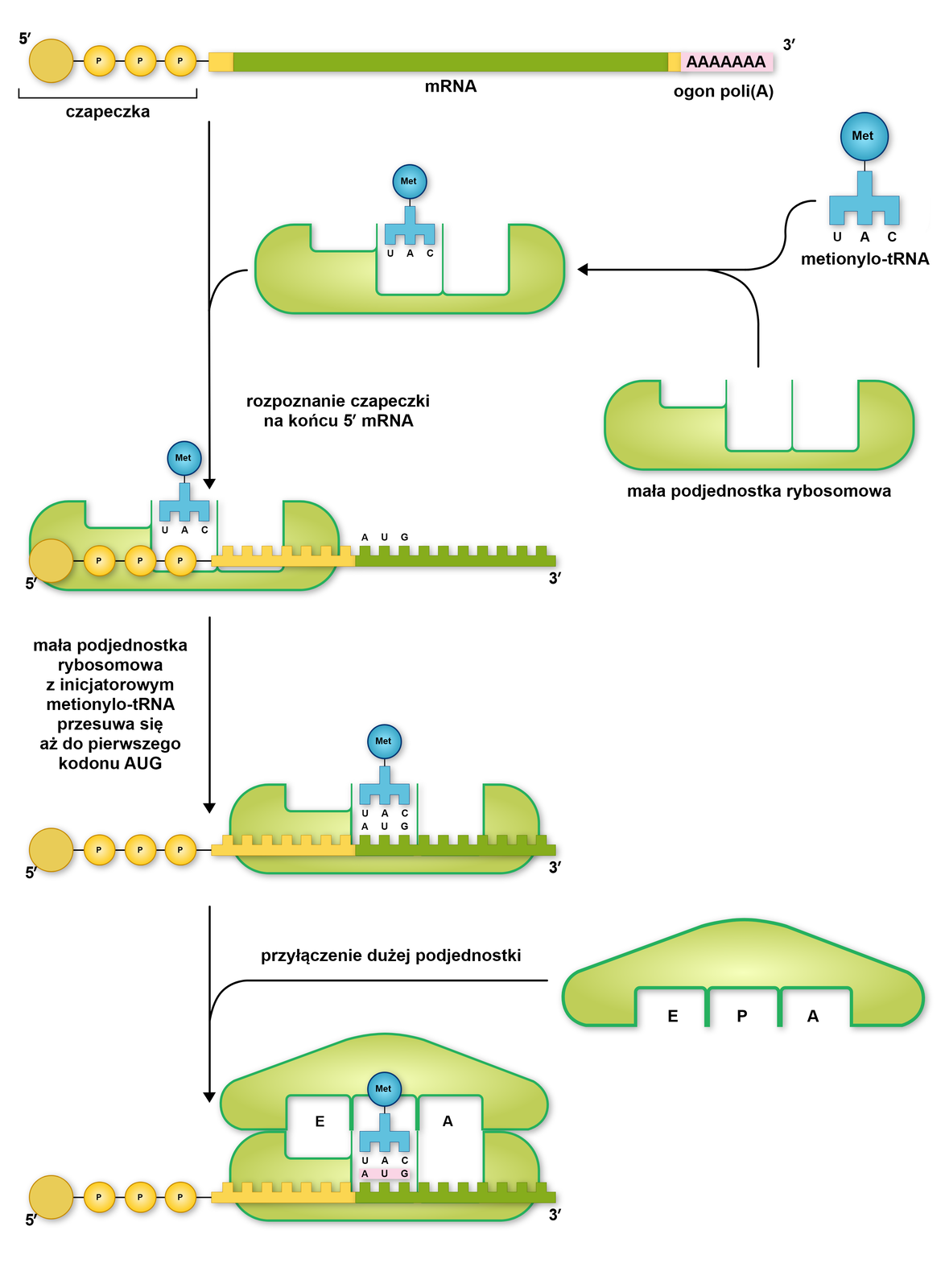
U eukariontów mniejsza podjednostka rybosomu łączy się najpierw z inicjatorowym metionylo‑tRNA, a następnie z czapeczką. Czapeczka jest strukturą na końcu 5′ mRNA, która stanowi miejsce wiązania rybosomu. Po przyłączeniu małej podjednostki rybosomu przesuwa się ona po sekwencji mRNA, aż natrafi na kodon AUG.
Kodon AUG znajduje się w obrębie sekwencji Kozaksekwencji Kozak, będącej miejscem inicjacji translacji.
Sekwencja Kozak to sekwencja nukleotydowa ACCAUGG, która występuje w mRNA eukariontów. Jest ona rozpoznawana przez rybosom jako miejsce, od którego mRNA jest przepisywany na kolejność aminokwasów w łańcuchu polipeptydowym w procesie translacji.
Sekwencja Kozak została nazwana na cześć amerykańskiej biochemiczki Marilyn Kozak, która zidentyfikowała ją w połowie lat 80 XX wieku.
Kiedy mała podjednostka rybosomu natrafi na kodon AUG, następuje przyłączenie dużej podjednostki rybosomu.
W procesie inicjacji translacji ważny udział pełnią białka lub kompleksy białkowe należące do czynników inicjacji translacji, oznaczanych jako eIFeIF.
Czynnik inicjacji translacji | Funkcja |
|---|---|
eIF1, eIF1A, eIF3 | Biorą udział w zapobieganiu połączeniu się małej podjednostki rybosomu z dużą podjednostką. Czynniki te wiążą się z małą podjednostką rybosomu (40S) oraz mRNA, umożliwiając utrzymanie struktury przestrzennej regionu rybosomu odpowiedzialnego za wiązanie mRNA. Dzięki temu możliwe jest skanowanie mRNA w poszukiwaniu kodonu START. |
eIF4F | Bierze udział w przyłączeniu rybosomu do czapeczki na końcu 5′ mRNA. |
eIF2 | Wchodzi w skład kompleksu zawierającego inicjatorowe metionylo‑tRNA oraz GTPGTP. Odnajduje kodon AUG, który inicjuje translację. |
Elongacja (wydłużanie łańcucha peptydowego)
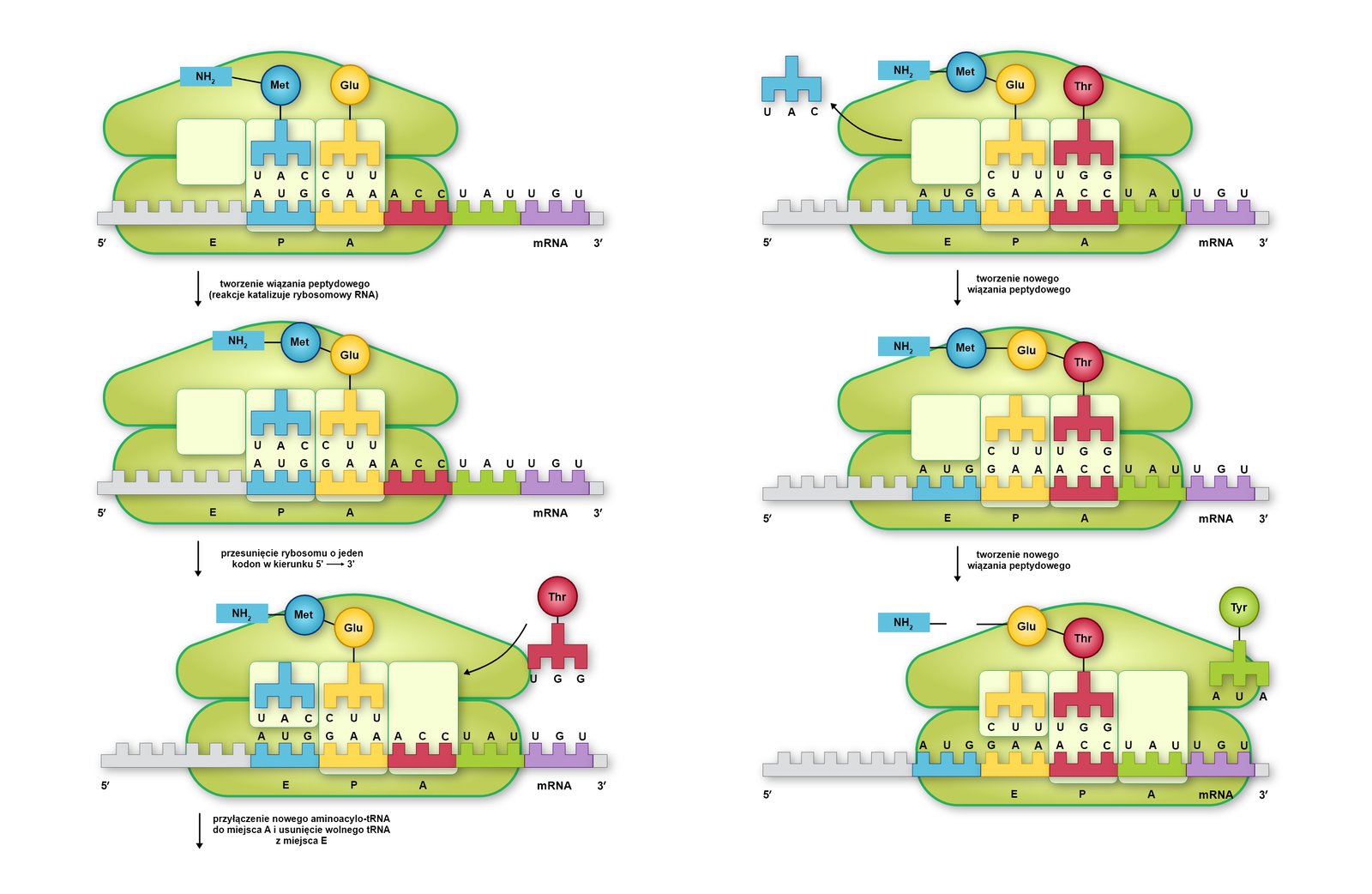
Elongacja to najbardziej dynamiczny etap procesu translacji i wiąże się z wydłużaniem sekwencji łańcucha peptydowego. Cząsteczka tRNA z przyłączoną metioniną znajdują się w miejscu P rybosomu. W miejscu A przyłącza się następna cząsteczka tRNA z przyłączonym aminokwasem, której antykodonantykodon odpowiada kolejnemu kodonowi w mRNA. Między metioniną a nowym aminokwasem tworzy się wiązanie peptydowe, metionina odłącza się od tRNA, a rybosom przesuwa o trzy nukleotydy (o kodon). W miejscu P znajduje się teraz nowo przyłączony tRNA, z którym związany jest łańcuch dwóch aminokwasów. Cząsteczka tRNA, która jako pierwsza przyłączyła się do mRNA, zostaje przesunięta do miejsca E, przez które opuszcza rybosom. Do uwolnionego miejsca A przyłącza się kolejna cząsteczka aminoacylo‑tRNA i cały proces przebiega według poprzedniego schematu aż do końca translacji.
Organizmy eukariotyczne mają dwa główne czynniki elongacji oznaczane jako eEFeEF.
Czynnik elongacji | Funkcja |
|---|---|
eEF1 | Wiązanie aminoacylo‑tRNA do struktury rybosomu, co umożliwia tworzenie wiązań między kolejnymi aminokwasami. |
eEF2 | Odpowiada za przesunięcie nici mRNA o jeden kodon po dołączeniu aminokwasu do tworzonego łańcucha peptydowego. Powoduje zmiany konformacyjne w obrębie rybosomu, które wymagają nakładu energii z GTP. |
Terminacja (zakończenie translacji)
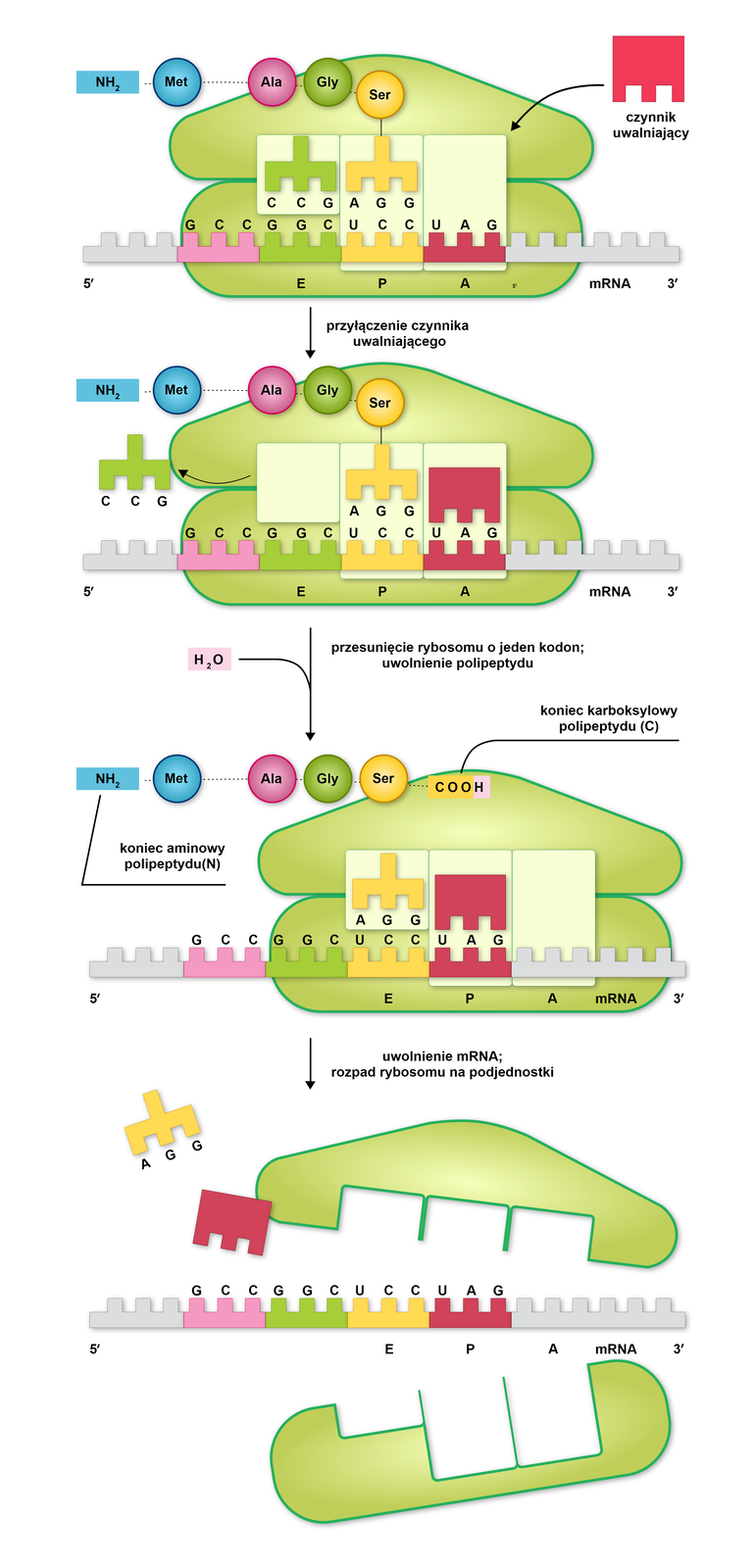
Terminacja to ostatni etap syntezy polipeptydu na rybosomach, który rozpoczyna się w momencie rozpoznania w sekwencji mRNA kodonu STOP. Ważną rolę w tym procesie odgrywa czynnik uwalniający oznaczany jako eRFeRF.
Kiedy miejsce A natrafi na kodon STOP (UAA, UAG, UGA), zamiast aminoacylo‑tRNA przyłącza się do niego białko zwane czynnikiem uwalniającym eRF1.
Czynnik uwalniający | Funkcja |
|---|---|
eRF1 | Czynnik ten powoduje hydrolizę wiązania estrowego między powstałym polipeptydem a miejscem P rybosomu. Tutaj kończy się translacja – odłącza się utworzony polipeptyd i rozpada kompleks translacyjny. |
eRF3 | Stymulacja aktywności eRF1 w obecności GTP. |
Potranslacyjne modyfikacje białek
W trakcie translacji łańcuch polipeptydowy jest zwijany i modyfikowany chemicznie, dzięki czemu białko osiąga odpowiednią strukturę drugorzędową i trzeciorzędową. Zwijanie białka warunkowane jest sekwencją aminokwasów i tworzeniem się wiązań pomiędzy łańcuchami bocznymi aminokwasów. Jeżeli dojrzałe białko składa się z kilku łańcuchów polipeptydowych, odpowiednie z nich są łączone, dzięki czemu białko osiąga strukturę czwartorzędową.
Nowo syntezowane białka nie zawsze tuż po powstaniu są białkami funkcjonalnymi, dlatego wymagają dodatkowych modyfikacji, aby mogły pełnić swoje funkcje w komórce. Modyfikacje potranslacyjne wpływają na stabilność, aktywność, właściwości fizyczne i właściwości chemiczne białek. Dzięki modyfikacjom potranslacyjnym białka mogą pełnić funkcje strukturalne i regulatorowe oraz możliwe jest ich sortowanie i kierowanie do odpowiednich miejsc w komórce lub poza nią.
Niektóre aminokwasy mogą być modyfikowane chemicznie, czyli przez przyłączenie do nich cząsteczek niebiałkowych np. cukrów, tłuszczów i grup fosforanowych.
Najczęściej spotykaną reakcją regulatorową jest fosforylacja łańcuchów bocznych aminokwasów. Dołączenie przez kinazy grupy fosforanowej do białka może doprowadzić do zmiany kształtu białka, przyczyniając się na przykład do odsłonięcia bądź zamaskowania centrum aktywnego. Wiele etapów ekspresji genów i szlaków przekazywania sygnałów powiązanych jest z potranslacyjną modyfikacją białek przez fosforylowanie.
Zdarza się, że konieczne jest wycięcie pewnej liczby aminokwasów z łańcucha polipeptydowego, np. wycięcie pierwszego aminokwasu – metioniony. Ponadto łańcuchy polipeptydowe mogą być cięte po syntezie na mniejsze fragmenty i dopiero w takiej formie są aktywne. Takiej modyfikacji ulegają m.in. insuliny i kaspazykaspazy.
Aminokwasy mogą być także modyfikowane poprzez przyłączenie innych białek. Przykładem jest ubikwitynacja, czyli przyłączenie ubikwityny do białka docelowego, która związana jest z procesem ich degradacji.
Białka mogą być modyfikowane wielokrotnie na różny sposób. Więcej na ten temat w e‑materiale Modyfikacje potranslacyjne białek.
Znaczenie translacji
Translacja odgrywa istotną rolę we wszystkich procesach komórkowych, ze względu na zaangażowanie białek w niemal każdą funkcję komórki, od budowy, poprzez transport, do reakcji metabolicznych. Mutacje w genach białek zaangażowanych w proces translacji powodują często ogromne zmiany w funkcjonowaniu organizmu, mogą prowadzić nawet do śmierci.
Zmiany w sekwencji czynnika inicjacji eIF1A w jego regionie N‑końca skorelowano z niekontrolowaną proliferacją komórek oraz zmianami nowotworowymi.
Mutacja w genie czynnika elongacji eEF2 powiązano z ataksją rdzeniowo‑móżdżkową. Z kolei zmiana w genie kodującym czynnik uwalniający u bakterii powodowała zatrzymanie podziałów komórkowych.
Translacja jest także jednym z poziomów regulacji ekspresji genów. Wszystkie te cechy dowodzą, iż translacja jest bardzo ważnym procesem w komórkach i pozwala na ich prawidłowe funkcjonowanie.
Słownik
trzy kolejne nukleotydy w sekwencji tRNA odpowiedzialne za rozpoznanie komplementarnej (zgodnie z komplementarnością zasad azotowych) sekwencji znajdującej się w kodonie w mRNA
(ang. eukaryotic elongation factor – eukariotyczny czynnik elongacji) białko uczestniczące w elongacji translacji u eukariontów
(ang. eukaryotic initiation factor – eukariotyczny czynnik inicjacji) białko uczestniczące w inicjacji translacji u eukariontów
(ang. eukaryotic release factor – eukariotyczny czynnik uwalniający) białko uczestniczące w terminacji translacji u eukariontów
guanozyno‑5′-trifosforan; organiczny związek chemiczny pełniący funkcję przenośnika energii w komórce
grupa enzymów, których celem jest zniszczenie białek strukturalnych i enzymatycznych w trakcie procesu apoptozy komórki
sekwencja trzech nukleotydów w łańcuchu DNA lub mRNA kodująca pojedynczy aminokwas w białku
sekwencja nukleotydowa w obrębie mRNA eukariontów, zawierająca kodon START; fragment mRNA rozpoznawany przez rybosom jako miejsce inicjacji translacji
drugi etap ekspresji genu, podczas którego – na podstawie informacji zapisanej w nici mRNA – jest syntetyzowany polipeptyd