Przeczytaj
Otrzymywanie soli w wyniku reakcji wodorotlenków z tlenkami
Reakcję otrzymywania soli w wyniku oddziaływania wodorotlenków z tlenkami można przedstawić równaniem:
Reakcja wodnego roztworu wodorotlenku z tlenkami kwasowymi
Tlenki kwasowe to tlenki, które reagują z zasadami, a nie reagują z kwasami. Można zaliczyć do nich: tlenek węgla(IV) , tlenek siarki(IV) , tlenek siarki(VI) , tlenek azotu(IV) , tlenek fosforu(V) . Poniżej przedstawiono doświadczenie reakcji wodorotlenku z tlenkiem kwasowym.
Problem badawczy: Czy tlenek kwasowy będzie reagował z wodnym roztworem wodorotlenku tworząc sól?
Hipoteza: Tlenek kwasowy będzie reagował z wodnym roztworem wodorotlenku tworząc sól.
Sprzęt i odczynniki:
probówki, szklana rurka, mała łyżeczka, pipeta;
odczynniki: wodny roztwór wodorotlenku sodu, gazowy tlenek węgla(IV), suchy lódsuchy lód, alkoholowy roztwór fenoloftaleiny.
Wykonanie:
Umieść w probówce 2 roztworu wodorotlenku sodu oraz dodaj dwie krople alkoholowego roztworu fenoloftaleiny.
Za pomocą szklanej rurki wdmuchuj tlenek węgla(IV) lub za pomocą łyżeczki dodawaj małymi porcjami drobny suchy lód.
Obserwuj zawartość probówki.
Schemat doświadczenia:

Równania reakcji:
Zapis cząsteczkowy równania reakcji:
Zapis jonowy równania reakcji:Zapis jonowy równania reakcji:
Zapis jonowy skrócony:Zapis jonowy skrócony:
Przy zapisie równań reakcji jonowych należy pamiętać, że tlenki nie dysocjujądysocjują na jony.
Obserwacje:
Po dodaniu gazowego tlenku węgla(IV) do roztworu wodorotlenku sodu, który zawiera fenoloftaleinę, następuje zmiana intensywności barwy roztworu.
Wnioski:
Tlenek reaguje z wodorotlenkiem. Powstaje sól – węglan sodu oraz woda.
Podsumowanie:
Zmiana intensywności barwy roztworu jest związana z tym, że wodny roztwór powstałej soli – węglanu sodu – ma odczyn zasadowy, a więc nie dochodzi do odbarwienia, za to wartość ulega obniżeniu w stosunku do wartości wyjściowej.
Tę reakcję można także zauważyć obserwując butelkę, w której znajduje się roztwór wodorotlenku sodu. Gdy na zewnętrznych jej ściankach znajdują się niewielkie ilości wodorotlenku sodu, reaguje on z tlenkiem węgla(IV) z powietrza. Wówczas na ściance można zauważyć biały nalot pochodzący od stałego węglanu sodu (po odparowaniu wody).
Reakcja wodnego roztworu wodorotlenku z tlenkami amfoterycznymi
Tlenki amfoteryczneTlenki amfoteryczne to tlenki, które reagują zarówno z kwasami, jak i zasadami. Do tlenków amfoterycznych można zaliczyć m.in. tlenek glinu , tlenek cynku . Poniżej przedstawiono doświadczenie wodorotlenku z tlenkiem amfoterycznym.
Problem badawczy: Czy tlenek amfoteryczny będzie reagował z wodnym roztworem wodorotlenku tworząc związek typu soli?
Hipoteza: Tlenek amfoteryczny będzie reagował z wodnym roztworem wodorotlenku tworząc związek typu soli.
Sprzęt i odczynniki:
probówki, mała łyżeczka, pipeta;
substancje: wodny roztwór wodorotlenku sodu, tlenek glinu.
Wykonanie:
Umieść w probówce 2 roztworu wodorotlenku sodu.
Za pomocą łyżeczki dodawaj małymi porcjami tlenek glinu.
Obserwuj zawartość probówki.
Schemat doświadczenia:
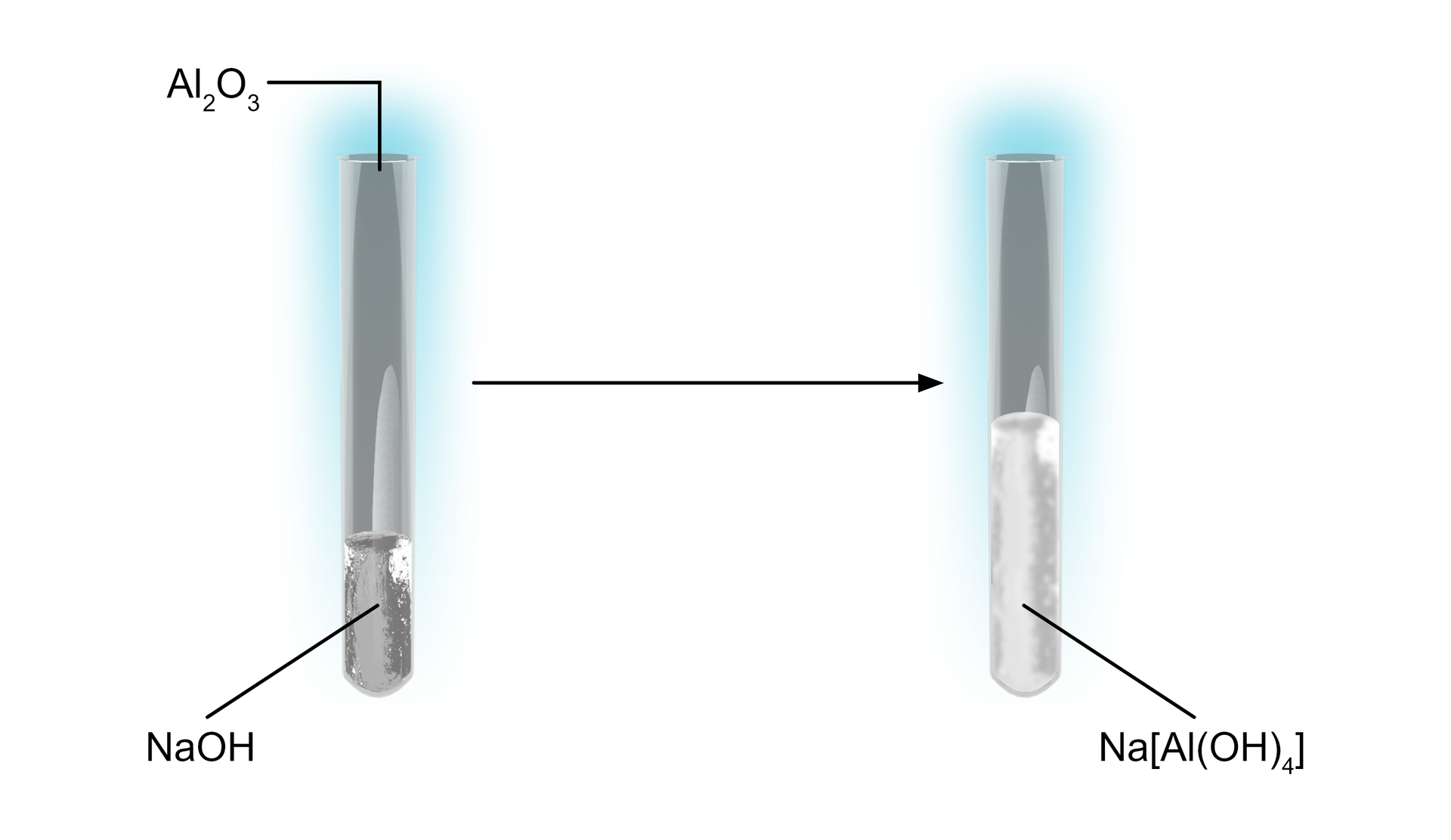
Równania reakcji:
Zapis cząsteczkowy równania reakcji:
Zapis jonowy równania reakcji:
Zapis jonowy skrócony:
Oczywiście zapis równań reakcji, w których powstaje heksahydroksoglinian sodu, jest jak najbardziej poprawny i równoznaczny z powyższym.
Obserwacje:
Po dodaniu do wodorotlenku sodu stałego tlenku glinu, tlenek roztworzył się.
Wnioski:
Powstał związek kompleksowy – tetrahydroksoglinian sodu – związek typu soli.
Podsumowanie:
Doświadczenie to wykazało, że wodne roztwory wodorotlenków reagują z tlenkami amfoterycznymi, w wyniku czego nie powstaje sól i woda, a jedynie sól jako związek kompleksowy.
Do otrzymania soli w wyniku reakcji z zasadami, a więc wodnymi roztworami wodorotlenków, możemy użyć tlenków kwasowych – wtedy równanie reakcji zapiszemy zgodnie ze schematem przedstawionym na początku lekcji. Tlenki zasadowe i obojętne nie będą reagowały z zasadami, a tlenki amfoteryczne wchodzą w reakcje z zasadami dając związki koordynacyjne.
Słownik
(gr. amphoteros „dwustronny”) zdolność związku chemicznego do reakcji zarówno z kwasami, jak i z zasadami
rozpad substancji chemicznej na jony dodatnie i ujemne pod wpływem rozpuszczalnika (na przykład wody)
tlenek węgla(IV) () w stanie stałym
zapis reakcji chemicznej zachodzącej w roztworze wodnym, przedstawiający substraty i produkty rozpuszczalne w wodzie w postaci jonów
zapis reakcji chemicznej zachodzącej w roztworze wodnym, gdzie przedstawione są jedynie substancje i jony, które biorą udział w reakcji
Bibliografia
Pac B., Zegar A., Podstawy klasyfikacji związków nieorganicznych w teorii i zadaniach, Kraków 2020.
Pac B., Zegar A., Reakcje w roztworach wodnych w teorii i zadaniach, Kraków 2020.