Przeczytaj
Cechy materii pozwalające na odróżnienie jednej substancji od drugiej nazywane są właściwościami. W chemii do opisu substancji używane są właściwości chemiczne i fizyczne.
to cechy nie związane ze zmianą składu chemicznego danej substancji. Należą do nich m.in.: gęstość, kolor, twardość, temperatury topnienia i wrzenia oraz przewodność elektryczna.
Ogólna charakterystyka żelaza
W tym rozdziale opisane zostaną właściwości fizyczne żelaza. Od czasów starożytnych żelazożelazo było wykorzystywane przez ludzi. Cała epoka w dziejach ludzkości nazwana została na jego cześć - epoką żelaza. Najstarsze wyroby z kutego żelaza pochodzą z XV i XIV wieku p.n.e. Zatem było i jest ono po dzień dzisiejszy metalem o znaczeniu strategicznym w przemyśle, a nawet w medycynie. Zajmuje ono czwarte miejsce pod względem rozpowszechnienia w skorupie ziemskiej. Szacuje się, że ok 5,6% Ziemi to właśnie żelazo, jednak znaczna jego część ulokowana jest w metalicznym jądrze naszej planety.
W przyrodzie można je spotkać w stanie rodzimym niezwykle rzadko, bowiem najczęściej występuje w postaci minerałów, tj.: magnetyt (), hematyt (), limonit (HIndeks dolny 22O), syderyt () oraz piryt ().
Żelazo (Fe, liczba atomowa 26) to metal występujący w bloku d, VIII grupie i 4 okresie układu okresowego pierwiastków chemicznych. Jego masa atomowa wynosi 55,845(2)u i posiada on 25 izotopów, z czego cztery są izotopami trwałymi. Żelazo chemicznie czyste to lśniący i srebrzystobiały metal, którego twardość wynosi 4 w skali MohsaMohsa. Jest ono kowalne i ciągliwe, a jego gęstość wynosi 7,86 .
Właściwości fizyczne żelaza
Właściwości fizyczne żelaza | |
Gęstość | 7,86 |
Temperatura topnienia | 1538,85°C |
Temperatura wrzenia | 2861°C |
Twardość w skali Mohsa | 4 |
Ciepło parowania | 349,6 |
Ciepło topnienia | 13,8 |
Ciśnienie pary nasyconej | 7,05 Pa (1808 K) |
Ciepło właściwe | 449 |
Konduktywność | 9,9310Indeks górny 66 |
Przewodność ciepła | 80,2 |
Układ krystalograficzny | Regularny przestrzennie centrowany - w temperaturze pokojowej |

W celu zwiększenia twardości tegoż metalu otrzymuje się jego stopy z innymi pierwiastkami. Najpopularniejszym z nich jest stal będąca stopem żelaza z węglem (max. 2,11%) i innymi pierwiastkami. Najczystszym stopem żelaza jest żelazo kute, ponieważ zawiera najmniejszą ilość domieszek innych pierwiastków, które nie przekraczają 0,5%. Takie żelazo ze względu na odporność na rozciąganie oraz duży udźwig znajduje zastosowanie w produkcji: mostów, rur, dachów, bojlerów, a nawet konstrukcji obiektów architektonicznych, np. wieży Eiffla.
Odmiany alotropowe żelaza
- Nazwa kategorii: Odmiany alotropowe żelaza
- Nazwa kategorii: Odmiana α‑Fe
- Nazwa kategorii: Odmiana γ‑Fe
- Nazwa kategorii: Odmiana δ‑Fe Koniec elementów należących do kategorii Odmiany alotropowe żelaza
- Elementy należące do kategorii Odmiany alotropowe żelaza
Odmiana alfa‑Fe
Jest trwała do temperatury 1179 K (905,85ºC). Tworzy ona sieć krystalicznąsieć krystaliczną - regularną, przestrzennie centrowaną. Odmiana ta posiada właściwości ferromagnetyczneferromagnetyczne i wykazuje je do temperatury 1041K (767,85ºC - temperatura CurieCurie), powyżej tej temperatury jest paramagnetykiem.
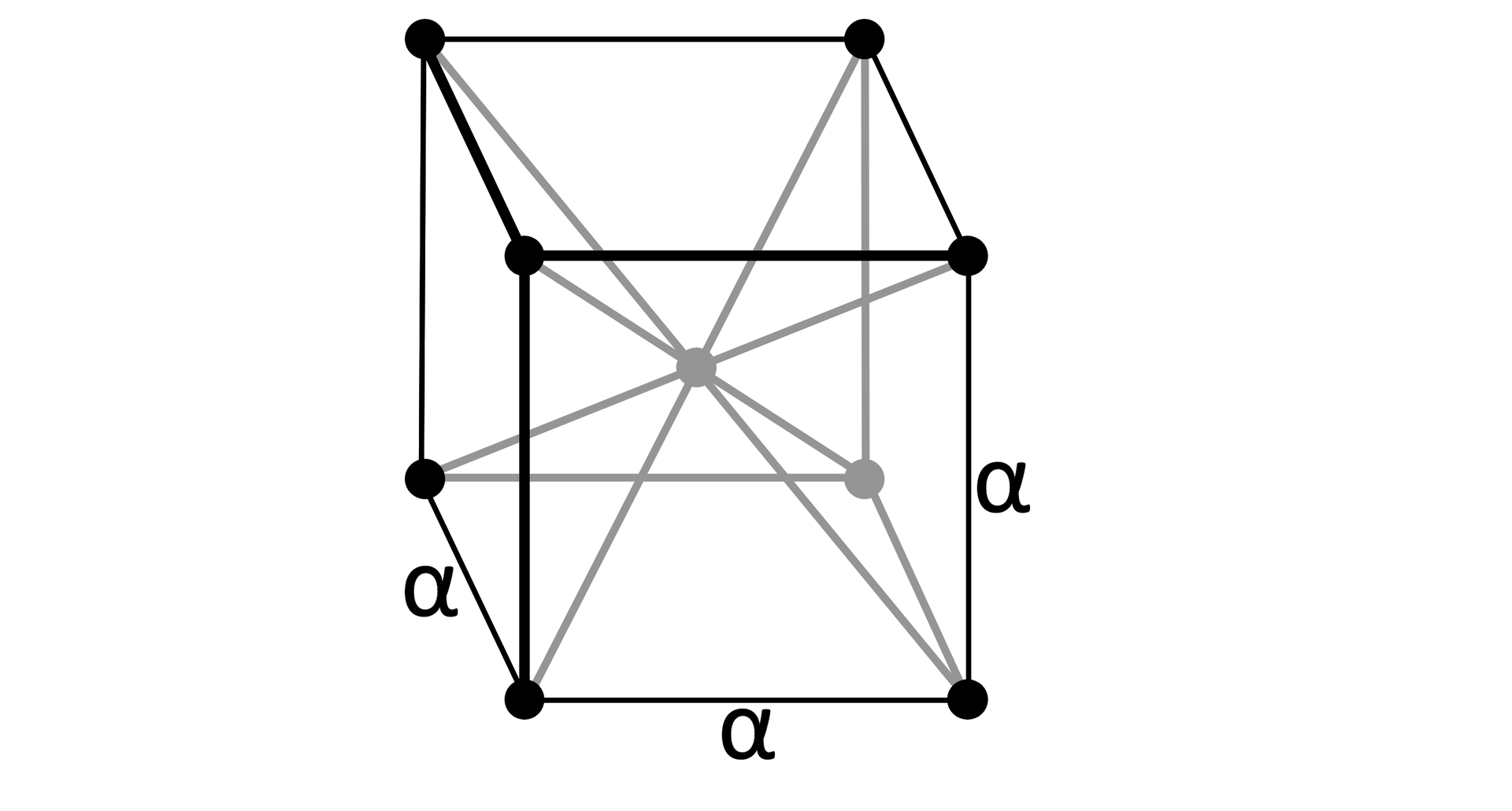
Odmiana gamma‑Fe
Jest to odmiana trwała w zakresie temperatur od 1179 K - 1674 K (905,85ºC - 1400,85ºC). Tworzy ona sieć krystaliczną regularną, płasko centrowaną.

Odmiana delta‑Fe
Jest to odmiana trwała w zakresie temperatur od 1674 K - 181 2K (1400,85ºC - 1538,85ºC). Tworzy ona sieć krystaliczną regularną, przestrzennie centrowaną.
Schemat przemian fazowychprzemian fazowych żelaza wygląda następująco:

Żelazo w meteorytach

Żelazo niezwykle rzadko i w niewielkich ilościach można spotkać w postaci rodzimej, np. w skałach bazaltowych (np. na Grenlandii). Jak wiadomo, w obecnych czasach żelazo pozyskuje się z innych minerałów zawierających żelazo, w wyniku redukcji rud tlenkowych koksem w wielkich piecach, a więc poprzez zastosowanie metod chemicznych i odpowiedniej obróbki tych złóż. Powstaje pytanie, w jaki sposób nastała epoka żelaza? Wiadomo, że w czasach starożytnych nie znano sposobów pozyskiwania żelaza. Skąd więc ono pochodziło? Żelazo w czasach prehistorycznych było głównie pochodzenia meteorytowego. Meteoryty bowiem są fragmentami skał, odłupanymi od macierzystych ciał w wyniku katastrofalnych zderzeń ciał niebieskich w kosmosie. Większość z nich posiada budowę ziarnistą i składa się z kamiennych kuleczek, między którymi występuje m.in. żelazo rodzime - w czystej postaci.
Słownik
(łac. ferrum „żelazo”) symbol Fe jest to pierwiastek chemiczny, należący do metali przejściowych. Jego masa atomowa wynosi 26. W układzie okresowym pierwiastków chemicznych leży w VIII grupie i w 4 okresie
jest to temperatura, powyżej której substancja będąca ferromagnetykiem traci swoje właściwości magnetyczne i staje się paramagnetykiem. Ma to związek ze zmianą fazy danego ciała stałego. Nazwa ta została nadana na cześć francuskiego fizyka Pierre'a Curie (męża Marii Skłodowskiej-Curie)
jest to pojęcie matematyczne, które oznacza powtarzające się w przestrzeni upakowanie drobin
(łac. ferrum „żelazo”, magneticus „magnetyczny”) ciało, które posiada własności ferromagnetyczne, czyli wykazuje spontaniczne namagnesowanie. Takie ciało jest kryształem, który posiada obszary stałego namagnesowania, zwane domenami magnetycznymi; ułożone są one w sposób chaotyczny
jest to proces termodynamiczny polegający na przejściu substancji z jednej fazy w inną, np. parowanie, krystalizacja, przemiana alotropowa
jest to skala twardości minerałów
ilość energii, jaką należy dostarczyć do jednostki masy danej substancji, aby zmienić jej stan skupienia w gazowy w stałej temperaturze i ciśnieniu
ilość energii potrzebnej do jednostki masy danej substancji stałej, aby zmienić jej stan skupienia w ciekły przy stałym ciśnieniu
ciśnienie, przy którym w określonej temperaturze gaz jest w stanie równowagi z cieczą
ciepło potrzebne do zmiany temperatury ciała w jednostkowej masie o jedną jednostkę
przewodność elektryczna właściwa, przewodnictwo elektryczne właściwe – wielkość fizyczna charakteryzująca przewodnictwo elektryczne przewodnika jednorodnego o oporze właściwym 1 oma na metr
Bibliografia
Bielański A., Podstawy chemii nieorganicznej, Warszawa 1994.
Encyklopedia PWN
Hejwowska S., Marcinkowski R., Równowagi i procesy jonowe, Gdynia 2005.
Pilski A. S., Meteoryty, online: http://www.ptmet.org.pl/meteoryty/, dostęp: 19.05.2021.




