Przeczytaj
Wpływ ciśnienia i temperatury na rozpuszczalność gazów w cieczy
RozpuszczalnośćRozpuszczalność to zdolność substancji do tworzenia z innymi substancjami roztworówroztworów jednorodnych.
Miarą rozpuszczalności jest maks. ilość substancji chemicznej, rozpuszczająca się w rozpuszczalnika w danych warunkach (temperatury i ciśnienia) tak, aby otrzymać roztwór nasycony.
Na proces rozpuszczania w cieczy zawsze mają wpływ siły międzycząsteczkowe, jednak w przeciwieństwie do ciał stałych i cieczy, w czasie rozpuszczania gazów jedynym czynnikiem energetycznym, który wpływa na rozpuszczalność, są oddziaływania substancja rozpuszczona‑rozpuszczalnik. Nie istnieją zaś oddziaływania substancja rozpuszczona‑substancja rozpuszczona, ponieważ atomy (lub cząsteczki) gazu są daleko od siebie zlokalizowane i nie doświadczają istotnych interakcji ze sobą.
Od jakich czynników zależy rozpuszczalność gazów w wodzie?
Rodzaj substancji i rozpuszczalnika
„Podobne rozpuszcza się w podobnym”. Rozpuszczalność tlenu w wodzie jest ok. trzy razy większa niż helu, co jest spowodowane występowaniem większych sił dyspersyjnych między cząsteczkami wody, a większymi od atomów helu cząsteczkami tlenu. Natomiast polarne cząsteczki chloroformu () mają stukrotnie większą rozpuszczalność od cząsteczek tlenu, ponieważ ulegają przyciąganiu z cząsteczkami wody na skutek oddziaływań typu dipol‑dipol.dipol‑dipol.
Temperatura
Rozpuszczalność gazów maleje wraz ze wzrostem temperatury.
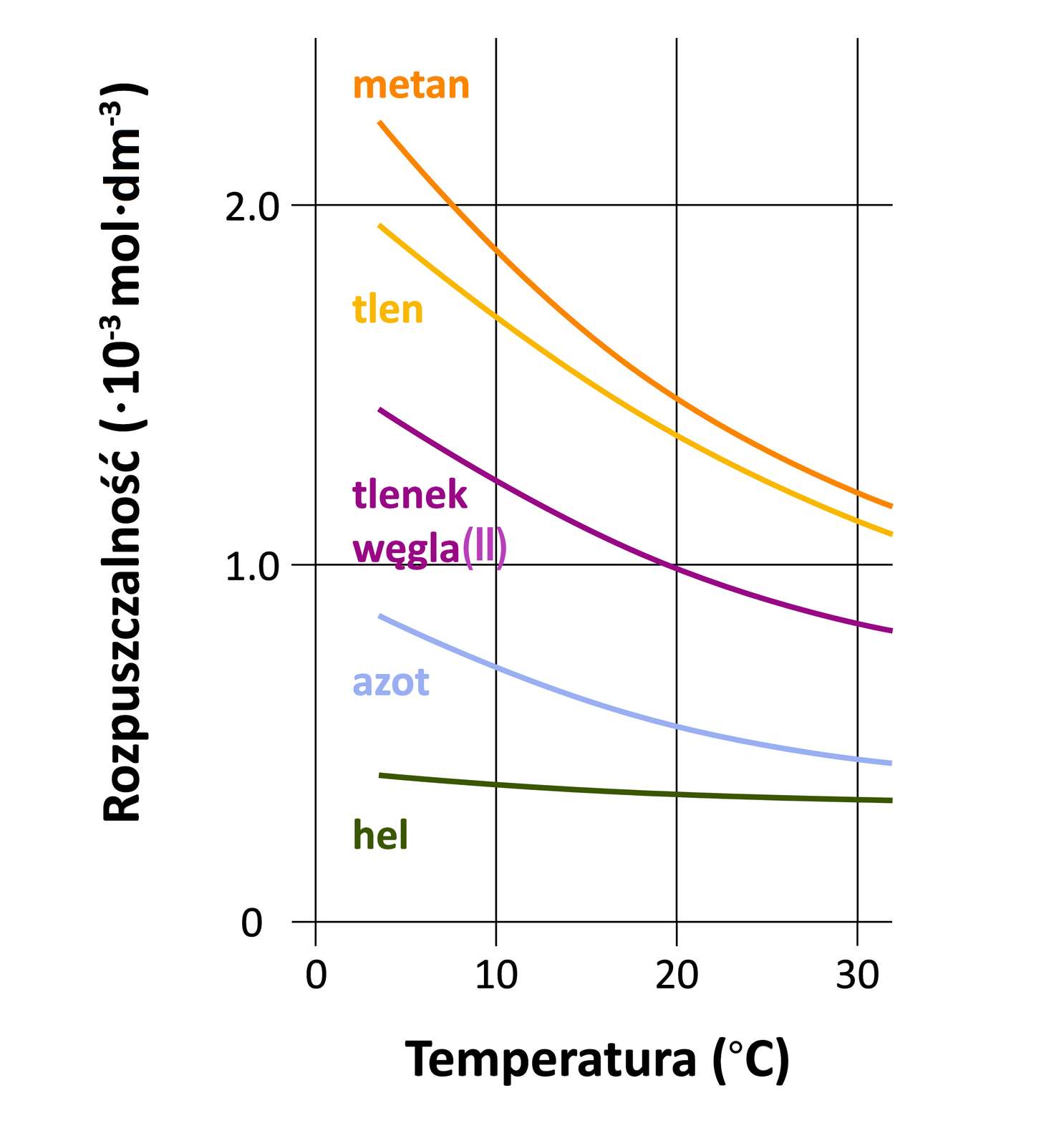

Odwrotna zależność rozpuszczalności gazów od temperatury ma duży wpływ na środowisko naturalne. Gdy temperatura wody w rzece, jeziorze lub strumieniu wzrasta, rozpuszczalność zawartego w niej tlenu maleje. Taka sytuacja może mieć poważne konsekwencje dla właściwego funkcjonowania ekosystemów wodnych i w najgorszych przypadkach może prowadzić do wymierania ryb na dużą skalę.
Ciśnienie
Rozpuszczalność gazów zależy od ciśnienia i rośnie wraz z jego wzrostem.
Analizując poniższy wykres, można zauważyć prawdziwość powyższego stwierdzenia. I chociaż zwiększenie ciśnienia powoduje wzrost rozpuszczalności gazów, to wpływ ten dla różnych typów gazów jest zróżnicowany. Na poniższym wykresie można zauważyć, że jest on bardzo duży dla tlenku węgla(), ale już dla samego tlenu nie powoduje tak znaczących zmian w rozpuszczalności.
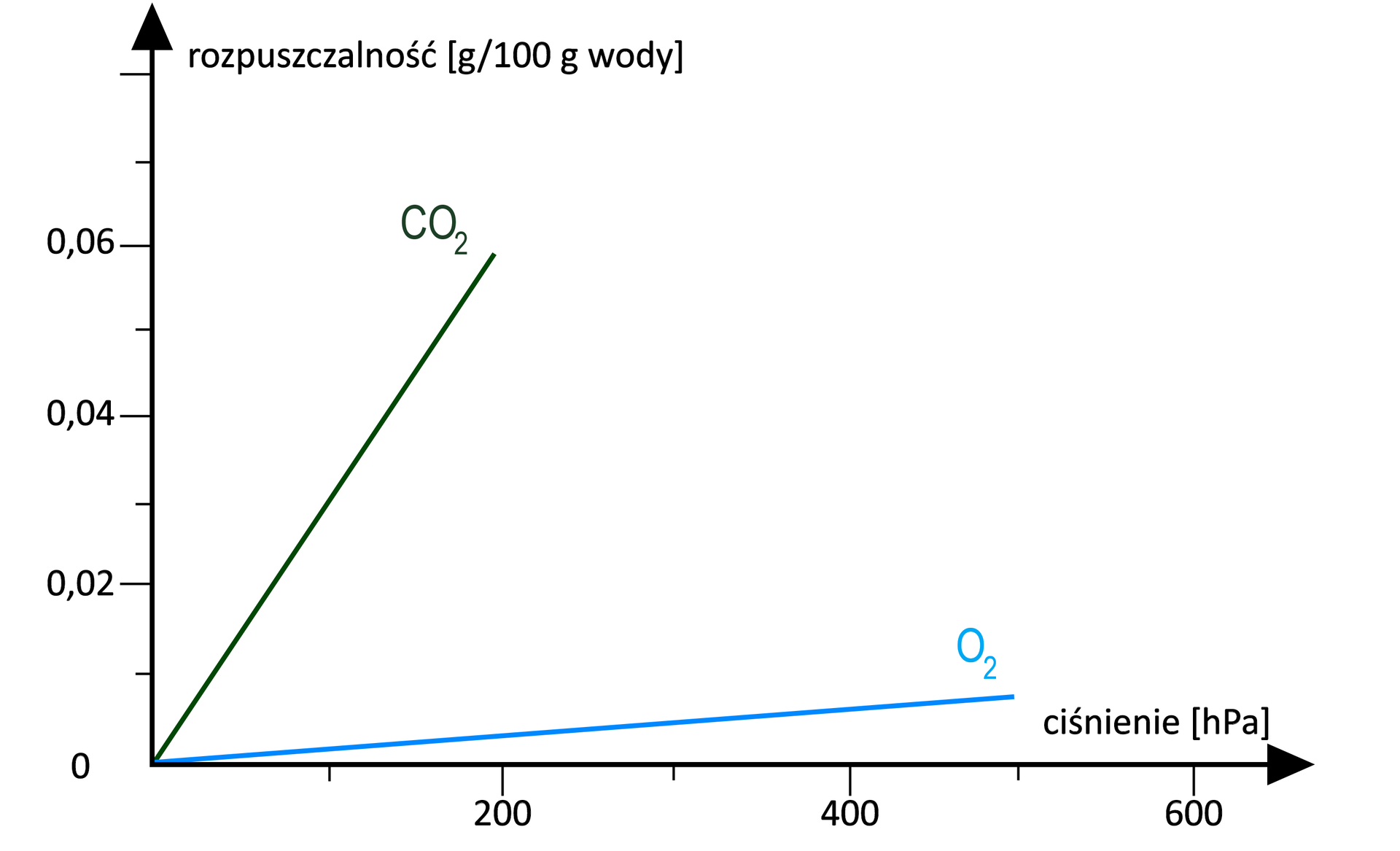

Przykładem właściwie ilustrującym to zjawisko są napoje gazowane. Proces nasycania napojów tlenkiem węgla() polega na działaniu na nie gazowym tlenkiem węgla() o stosunkowo wysokim ciśnieniu, a następnie uszczelnieniu pojemnika z napojem. Po otwarciu butelki, można usłyszeć charakterystyczny dźwięk „syknięcia” – wówczas maleje ciśnienie, a tym samym rozpuszczalność, dlatego obserwuje się uwalnianie części rozpuszczonego dwutlenku węgla z roztworu. Początkowo roztwór jest nasycony tlenkiem węgla(), pod stosunkowo wysokim ciśnieniem, jednak po otwarciu butelki po pewnym czasie dojdzie do wyrównania zawartości tlenku węgla() zgodnie z jego rozpuszczalnością.
Efektywność rozpuszczania gazu w wodzie pod danym ciśnieniem jest odwrotnie proporcjonalna do zmian temperatury:
podwyższenie temperatury – powoduje zmniejszenie ilości gazu w mieszaninie;
obniżenie temperatury – powoduje zwiększenie ilości gazu w mieszaninie.
Efektywność rozpuszczania gazu w wodzie w danej temperaturze jest wprost proporcjonalna do zmian ciśnienia:
zwiększenie ciśnienia – powoduje zwiększenie ilości gazu w mieszaninie;
zmniejszenie ciśnienia – powoduje zmniejszenie ilości gazu w mieszaninie.

Gazy mogą tworzyć roztwory przesycone i nie jest to tylko sztucznie generowane przez producentów napojów gazowanych, lecz może również występować naturalnie w odpowiednich warunkach ciśnienia i temperatury. Przesycenie wody tlenkiem węgla() nad jeziorem Nyos w Kamerunie sierpnia roku było przyczyną śmierci osób i wielu tysięcy sztuk bydła, antylop oraz gryzoni w promieniu - kilometrów od jeziora. Do tragedii doszło wskutek gwałtownego wydzielania się tlenku węgla(), nagromadzonego w pokładach geologicznych pod powierzchnią zbiornika wodnego. Woda na dnie jeziora Nyos była przesycona tlenkiem węgla(), ze względu na aktywność wulkaniczną (pod jeziorem). W wyniku ogrzewania, z wód jeziora, uwolnionych zostało ok. miliona ton . Ten bezbarwny gaz, o gęstości większej od gęstości powietrza, spłynął po zboczu góry do dwóch sąsiadujących dolin, dusząc ich mieszkańców.
Słownik
oznacza jednorodną mieszaninę dwóch lub więcej substancji; najczęściej jeden ze składników tej mieszaniny występuje w większej ilości i wówczas nazywany jest rozpuszczalnikiem, a więc substancją służącą do rozpuszczania innych składników (substancji rozpuszczonych)
zdolność substancji do tworzenia z innymi substancjami roztworów jednorodnych
rodzaj sił międzycząsteczkowych (sił van der Waalsa) typu dipol indukowany‑dipol indukowany, który występuje między cząsteczkami każdego rodzaju; mające szczególne znaczenie dla związków niepolarnych i nieposiadających trwałego momentu dipolowego (jak np. , , i ) oraz w gazach szlachetnych
rodzaj oddziaływań międzycząsteczkowych – sił van der Waalsa – które występują między cząsteczkami posiadającymi trwałe momenty dipolowe; cząsteczki takie posiadają w jednych miejscu nadmiar ładunku ujemnego, a w innym jego niedomiar; oddziałują ze sobą podobnie jak jony, jednak oddziaływanie to jest słabsze
Bibliografia
Encyklopedia PWN
Czynniki wpływające na szybkość rozpuszczania się w wodzie, Platforma edukacyjna Ministerstwa Edukacji i Nauki, online: https://epodreczniki.pl/a/czynniki-wplywajace-na-szybkosc-rozpuszczania-sie-substancji-w-wodzie/DYNLy4Koc, dostęp: 28.01.2021.
Hejwowska S., Marcinkowski R., Chemia ogólna i niorganiczna, Gdynia 2005.