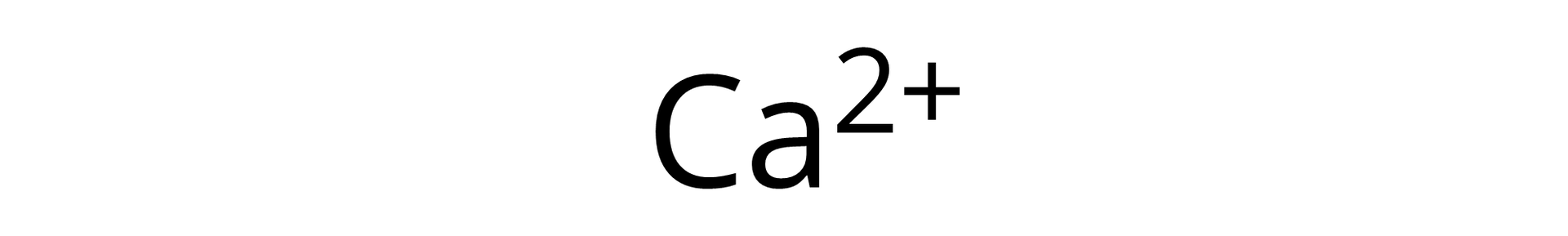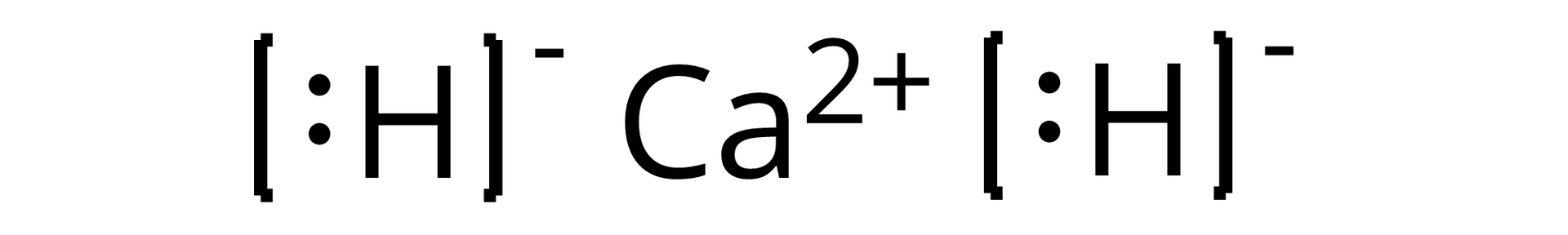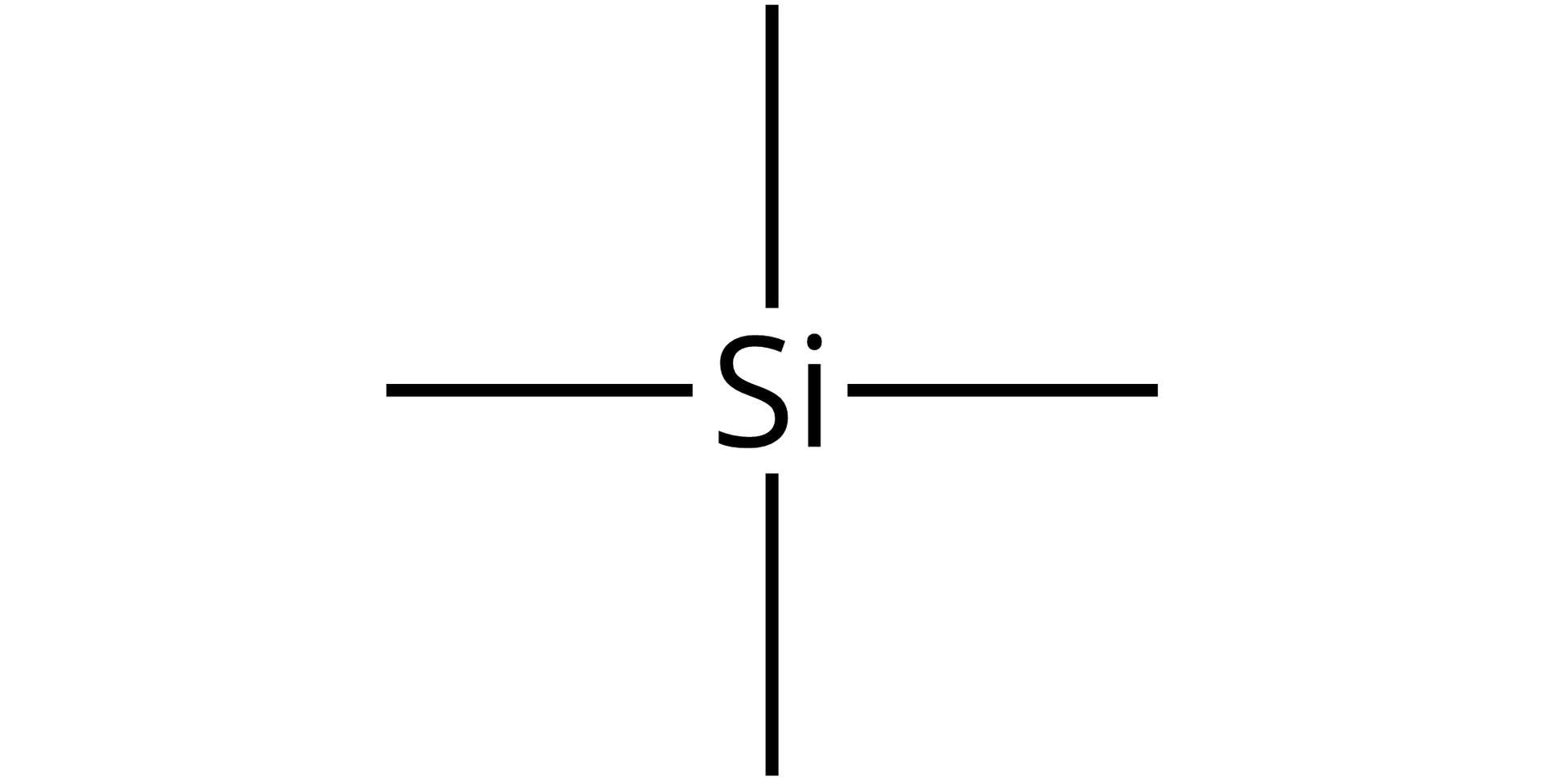Przeczytaj
Klasyfikacja wodorków
Początek istnienia Wszechświata, na skutek Wielkiego Wybuchu, spowodował powstanie wodoru. Pierwiastek ten jest najczęściej spotykanym pierwiastkiem we Wszechświecie i tworzy on binarne (dwuskładnikowe) wodorki niemalże ze wszystkimi pierwiastkami bloku i bloku , z wyjątkiem gazów szlachetnych oraz indu i talu.

Budowa oraz charakter tych związków wynika bezpośrednio z rodzaju pierwiastków, jakie tworzą je z wodorem.
Wodorki jonowe (typu soli)
I tak, silnie elektrododatnie pierwiastki grupy i tworzą z wodorem związki typu soli, gdzie atomy są ze sobą połączone wiązaniem jonowym (wyjątek stanowi beryl oraz magnez, dla których wiązania z atomami wodoru wykazują charakter raczej kowalencyjny), w których wodór występuje na stopniu utlenienia. Przykładem takiego związku jest – wodorek potasu.
Wodorki metaliczne
Drugi typ związków to wodorkiwodorki metaliczne, które tworzone są z wodoru i pierwiastków z bloku (np. – wodorek miedzi()).
Wodorki kowalencyjne
Trzeci i ostatni typ wodorków tworzony jest z pierwiastkami znajdującymi się w bloku . Są to związki kowalencyjne (cząsteczkowe), do których należą: amoniak, wodorki tlenowców (np. ) i fluorowców (np. ), a także metan.
Rysowanie wzorów strukturalnych wodorków
Wzory sumaryczne wodorków tworzy się poprzez umieszczenie symbolu wodoru na drugim miejscu dla wodorków pierwiastków z grup – lub na pierwszym miejscu dla wodorków pierwiastków z grup i Takie wzory pozwalają na ustalenie składu pierwiastkowego wodorków, lecz nie dostarczają one informacji na temat przestrzennego ułożenia atomów i ich wzajemnych połączeń. Informacje te można uzyskać ze wzorów strukturalnychwzorów strukturalnych, które ukazują, w jaki sposób atomy połączone są w cząsteczce związku. Do wyznaczenia wzoru sumarycznego wodorków ważne jest ustalenie, z jakim typem związku mamy do czynienia i jaki jest stopień utlenieniastopień utlenienia pierwiastka macierzystego, który go tworzy:
gdzie:
– oznacza atom metalu lub niemetalu grup , , oraz metale bloku i bloku ;
– oznacza jon wodorowy;
– oznacza stopień utlenienia atomu metalu.
– oznacza atom niemetalu grupy , ;
– oznacza atom wodoru;
– oznacza stopień utlenienia atomu niemetalu.
We wzorach strukturalnych, do narysowania wiązań kowalencyjnych pomiędzy atomami posługujemy się kreskami (które łączą dwa atomy pierwiastków), jedna kreska oznacza jedno wiązanie. Dla związków jonowych, do narysowania ich struktur wykorzystujemy wzory Lewisa. Powstaje pytanie: jak narysować wzory strukturalne dla wodorków?
Dla wodorków, tworzących związki jonowe, wzory strukturalne wyglądają w sposób następujący:

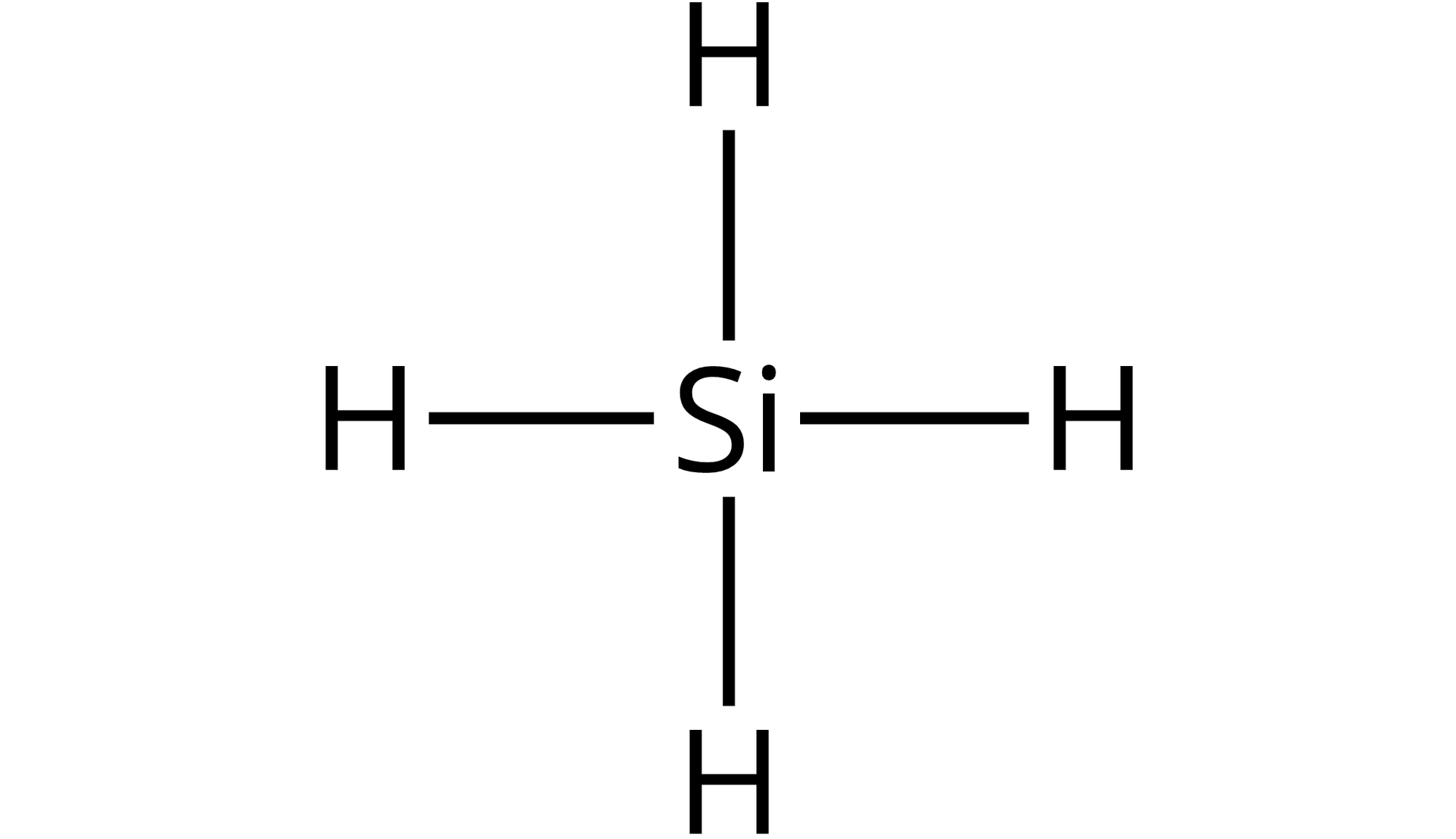
Jeśli chcemy narysować wzory strukturalne dla wodorków bloku , należy wykorzystać w tym celu kreski oznaczające wiązanie wytworzone pomiędzy atomem wodoru a atomem drugiego pierwiastka w cząsteczce. Przykładowy wzór wygląda następująco:
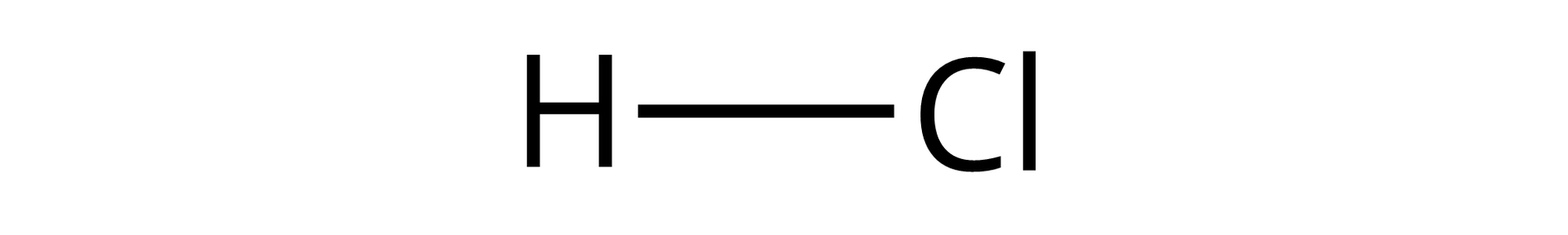
W przypadku wodorków metali przejściowych, wiązania między wodorem a metalami mogą wykazywać charakter metaliczny, gdyż w kryształach tych związków jony wodoru są nieregularnie rozmieszczone między jonami metalu. Co więcej, stosunek atomów obu pierwiastków nie zawsze jest stechiometryczny, jak np. dla wodorku palladu, opisywanego wzorem , gdzie oznacza liczbę dziesiętną mniejszą od .
Nazwa systematyczna wodorku (nazwa dopuszczalna) | Wzór wodorku | Stopień utlenienia pierwiastka macierzystego |
|---|---|---|
wodorek litu | ||
wodorek sodu | ||
wodorek potasu | ||
wodorek rubidu | ||
wodorek wapnia | ||
wodorek strontu | ||
wodorek miedzi() | ||
wodorek chromu() | ||
wodorek skandu() | ||
metan | ||
silan (krzemowodór) | ||
arsan (arsenowodór) | ||
azan (amoniak) | ||
sulfan (siarkowodór) | ||
fluorowodór |
Narysuj wzór strukturalny wodorku wapnia.
Narysuj wzór strukturalny .
Słownik
liczba dodatnich lub ujemnych ładunków elementarnych, jakie można przypisać atomom pierwiastka danego związku chemicznego, gdyby wszystkie wiązania utworzone przez atom były jonowe
inaczej nazywany wzorem kreskowym, pozwala na określenie poszczególnych połączeń, składu jakościowego i ilościowego w danym związku chemicznym
jest to dwuskładnikowy związek, powstały w wyniku połączenia wodoru z innymi pierwiastkami chemicznymi, jego wzór ogólny to ( – atom pierwiastka macierzystego, należący do bloku , lub grup , , i bloku , – wartościowość tego pierwiastka) lub ( – atom pierwiastka macierzystego, należący do grup lub bloku , – wartościowość tego pierwiastka)
Bibliografia
Encyklopedia PWN
Atkins P., Jones L., Chemia ogólna, Cząsteczki, materia, reakcje, Warszawa 2016.
Bielański A., Podstawy Chemii nieorganicznej, t. 2, Warszawa 1994.