Przeczytaj
Mydło to pojęcie w języku polskim, które posiada wiele znaczeń. Określeniem tym nazywa się nie tylko środek do mycia i prania, ale również jedną z kostek domino lub jeden ze znaczników linii na materiale.
Mydła (z chemicznego punktu widzenia) to sole wyższych kwasów karboksylowych (o długich łańcuchach węglowodorowych). Posiadają budowę jonową. W ich skład wchodzą aniony reszt kwasowych pochodzących od wyższych kwasów karboksylowych oraz kationy metalu lub kationy amonu .
Gdy mówimy o wyższych kwasach karboksylowych, w tym wypadku najczęściej myślimy o:
kwasie heksadekanowym (palmitynowym) , ;
kwasie oktadekanowym (stearynowym) , ;
kwasie oktadec––enowym (oleinowym),
, .
Gdy mówimy o kationach metalu, najczęściej myślimy o kationach sodu, potasu, ale mogą to być również kationy litu, magnezu oraz glinu.
Budowa mydeł jako substancji amfifilowych
Anion posiada właściwości amfifiloweamfifilowe, wynikające z jego specyficznej budowy. Znajdują się w niej bowiem dwa fragmenty o odmiennej naturze, co sprawia, że wykazują one różne powinowactwo do substancji polarnych i niepolarnych. Przyjrzyjmy się bliżej budowie tego anionu, który składa się:
z części hydrofilowejhydrofilowej, która „lubi” wodę, tzw. polarnejpolarnej „głowy”;
z części hydrofobowejhydrofobowej, która „nie lubi” wody, tzw. niepolarnego „ogona”.
Na niepolarny „ogon” składa się węglowodorowy łańcuch. Polarną „głowę” tworzy grupa .

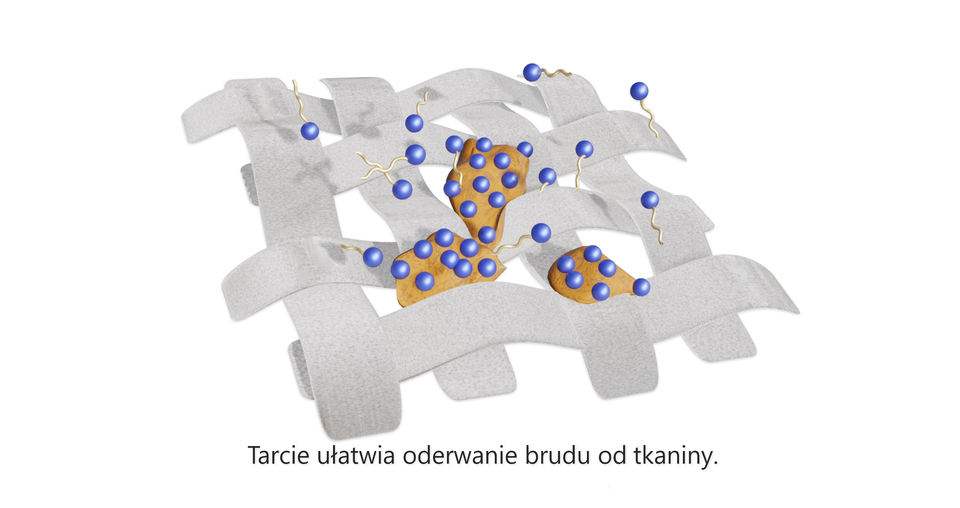
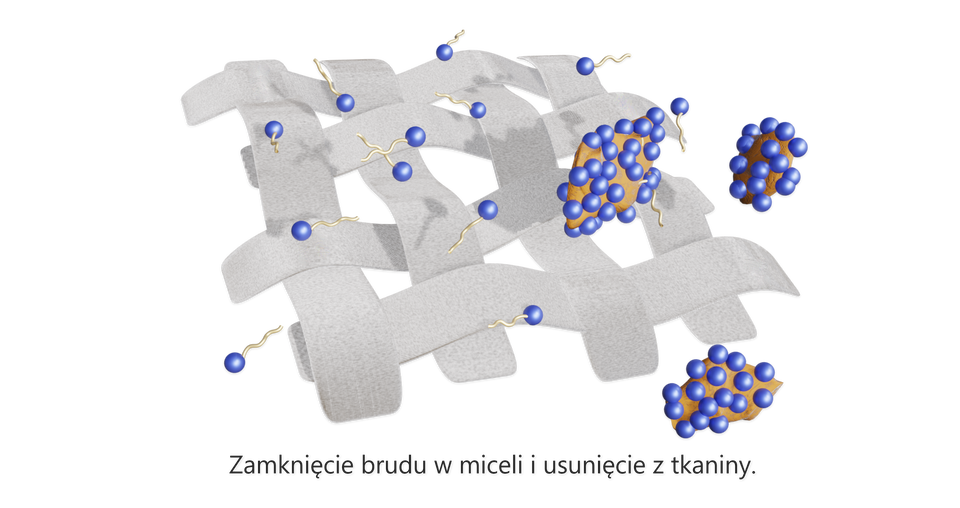
Substancja o tego typu budowie nosi nazwę (anionowo) powierzchniowo czynnej. Dodana do wody, powoduje obniżenie napięcia powierzchniowego i umożliwia lepsze wnikanie cząsteczek wody, nawet w najmniejsze szczeliny czy zagłębienia. Taka budowa umożliwia także usuwanie brudu oraz sprawia, że aniony te mogą działać jak emulgator.
Klasyfikacja mydeł
Mydła możemy podzielić m.in. ze względu na ich rozpuszczalność w wodzie i ich stan skupienia.
- Nazwa kategorii: mydła{color=#BCAAA4}
- Nazwa kategorii: rozpuszczalność [br]w wodzie{color=#E57373}
- Nazwa kategorii: rozpuszczalne{color=#EF9A9A}
- Nazwa kategorii: sodowe{color=#D7CCC8}
- Nazwa kategorii: potasowe{color=#D7CCC8}
- Nazwa kategorii: amonowe{color=#D7CCC8} Koniec elementów należących do kategorii rozpuszczalne{color=#EF9A9A}
- Nazwa kategorii: nierozpuszczalne{color=#EF9A9A}
- Nazwa kategorii: magnezowe{color=#D7CCC8}
- Nazwa kategorii: wapniowe{color=#D7CCC8}
- Nazwa kategorii: glinowe{color=#D7CCC8}
- Nazwa kategorii: litowe{color=#D7CCC8} Koniec elementów należących do kategorii nierozpuszczalne{color=#EF9A9A}
- Nazwa kategorii: stan[br] skupienia{color=#E57373}
- Nazwa kategorii: ciekłe{color=#EF9A9A}
- Nazwa kategorii: magnezowe{color=#D7CCC8} Koniec elementów należących do kategorii ciekłe{color=#EF9A9A}
- Nazwa kategorii: stałe{color=#EF9A9A}
- Nazwa kategorii: miękkie{color=#D7CCC8}
- Nazwa kategorii: potasowe{color=#FFCDD2}
- Nazwa kategorii: glinowe{color=#FFCDD2} Koniec elementów należących do kategorii miękkie{color=#D7CCC8}
- Nazwa kategorii: twarde{color=#D7CCC8}
- Nazwa kategorii: sodowe{color=#FFCDD2}
- Nazwa kategorii: wapniowe{color=#FFCDD2} Koniec elementów należących do kategorii twarde{color=#D7CCC8}
- Nazwa kategorii: kationy [br]metalu{color=#E57373}
- Nazwa kategorii: grupa{color=#EF9A9A}
- Nazwa kategorii: kationy [br]potasu{color=#D7CCC8}
- Nazwa kategorii: kationy [br]sodu{color=#D7CCC8}
- Nazwa kategorii: kationy [br]litu{color=#D7CCC8} Koniec elementów należących do kategorii grupa{color=#EF9A9A}
- Nazwa kategorii: grupa{color=#EF9A9A}
- Nazwa kategorii: kationy [br]wapnia{color=#D7CCC8}
- Nazwa kategorii: kationy [br]magnezu{color=#D7CCC8}
- Nazwa kategorii: metale [br]ciężkie{color=#D7CCC8} Koniec elementów należących do kategorii grupa{color=#EF9A9A}
- Nazwa kategorii: zastosowanie w procesie [br]produkcji i dodatki [br]uszlachetniające{color=#E57373}
- Nazwa kategorii: szare [br](bez [br]dodatków){color=#EF9A9A}
- Nazwa kategorii: półtoaletowe{color=#EF9A9A}
- Nazwa kategorii: toaletowe{color=#EF9A9A}
- Nazwa kategorii: toaletowe [br]dla dzieci{color=#EF9A9A} Koniec elementów należących do kategorii zastosowanie w procesie [br]produkcji i dodatki [br]uszlachetniające{color=#E57373}
- Elementy należące do kategorii mydła
- Elementy należące do kategorii rozpuszczalność [br]w wodzie
- Elementy należące do kategorii rozpuszczalne
- Elementy należące do kategorii nierozpuszczalne
- Elementy należące do kategorii stan[br] skupienia
- Elementy należące do kategorii ciekłe
- Elementy należące do kategorii stałe
- Elementy należące do kategorii miękkie
- Elementy należące do kategorii twarde
- Elementy należące do kategorii kationy [br]metalu
- Elementy należące do kategorii grupa
- Elementy należące do kategorii grupa
- Elementy należące do kategorii zastosowanie w procesie [br]produkcji i dodatki [br]uszlachetniające
Hydroliza mydeł
Mydła rozpuszczalne w wodzie (sodowe, potasowe i amonowe) nadają roztworowi wodnemu odczyn zasadowy. Jest on konsekwencją reakcji hydrolizy anionowej, której – ze względu na swoją budowę – ulegają mydła.
Przykładem może być dysocjacja i hydroliza rozpuszczalnego w wodzie mydła sodowego, heksadekanianu (palmitynianu) sodu: .
Dysocjacja elektrolityczna
Kation sodu pochodzi od mocnej zasady, wodorotlenku sodu, dlatego nie ulega reakcji hydrolizy. Anion heksadekanianowy pochodzi od słabego kwasu heksadekanowego (palmitynowego), dlatego ulega reakcji hydrolizy anionowej.
Hydroliza anionowa
W wyniku reakcji hydrolizy anionowej powstaje słaby kwas heksadekanowy oraz anion wodorotlenkowy, który odpowiada za zasadowy odczyn roztworu.


Syndet jest preparatem myjącym, który zawiera detergenty syntetyczne. W porównaniu z mydłem, w mniejszym stopniu powoduje przesuszanie naskórka. Po rozpuszczeniu w wodzie powoduje, że powstały roztwór ma lekko kwasowy odczyn, nie zawiera mydła. Wymyślony został dla żołnierzy z armii amerykańskiej, żeby mogli zadbać o higienę w każdych okolicznościach, nawet korzystając z wody morskiej, w której syndet doskonale się pieni.
Słownik
właściwość substancji, polegająca na zdolności jej cząsteczek (lub jej fragmentów) do oddziaływania z rozpuszczalnikami polarnymi, głównie z wodą bądź grupami polarnymi innych związków; cecha makroskopowa materiałów, obrazująca ich zdolność do zwilżania wodą
(gr. hydro „woda”, phobos „strach”) właściwość substancji, polegająca na niezdolności jej cząsteczek (lub jej fragmentów) do oddziaływania z rozpuszczalnikami polarnymi, głównie z wodą bądź grupami polarnymi innych cząsteczek; cecha makroskopowa materiałów obrazująca ich brak zdolności do zwilżania przez wodę
cząsteczka biegunowa, cząsteczka dipolowa, dipol, cząsteczka utworzona z atomów o różnej elektroujemności, w której nastąpiło rozdzielenie ładunku dodatniego i ujemnego
właściwość substancji polegająca na zdolności jej cząsteczek do silnego oddziaływania zarówno z cząsteczkami rozpuszczalników polarnych (np. wody), jak i niepolarnych (np. węglowodorów)
wielkość termodynamiczna, określająca zdolność układu substancji do przereagowania w określonym kierunku w danych warunkach
(łac. mica „okruszyna”) ułożony na kształt kuli zespół cząsteczek związku powierzchniowo czynnego (surfaktantu) lub jonów w roztworze; posiadają działanie solubilizujące, które umożliwia substancji nierozpuszczalnej w wodzie wprowadzenie do fazy wodnej
Bibliografia
Encyklopedia PWN
Falarz A., Mataczyńska G., Towaroznawstwo wybranych artykułów spożywczych i nieżywnościowych, Warszawa 1997.
Mastalerz P., Podręcznik chemii organicznej, Warszawa 1998.
McMurry J., Chemia organiczna, t. 5, Warszawa 2000.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 4, Warszawa 1997.
Reusch W., Virtual Textbook of Organic Chemistry, 2019.
Sikora T., Giemza M., Obsługa klienta: elementy towaroznawstwa : podręcznik – liceum o profilu usługowo–gospodarczym, Warszawa 2003.
Soaps and detergents, 2020, online: Soaps and Detergents - https://chem.libretexts.org/Bookshelves/Organic_Chemistry/Supplemental_Modules_(Organic_Chemistry)/Lipids/Properties_and_Classification_of_Lipids/Soaps_and_Detergents (dostęp: 17.06.2021)