Przeczytaj
Związki chromu i manganu na różnych stopniach utlenienia
Na początek zastanów się, jakie są możliwe stopnie utlenieniautlenienia manganu i chromu w związkach. Chrom i mangan są metalami – mogą oddawać elektrony. Przeanalizuj konfiguracje elektronowe tych pierwiastków.
Mangan
Chrom
Mangan i chrom są pierwiastkami występującymi w związkach na różnych stopniach utlenienia, w dodatku różnią się barwą. Związki tych pierwiastków na najwyższym stopniu utlenienia, czyli manganu(VII) oraz chromu(VI), są silnymi utleniaczami. W jaki sposób przebiegają reakcje utleniania i redukcji związków manganu i chromu?
Reakcje utlenienia i redukcji związków manganu
Reakcje utlenienia i redukcji związków chromu
Reakcja dichromianu(VI) potasu z azotanem(III) potasu
Reakcja dichromianudichromianu(VI) potasu z azotanem(III) potasu w środowisku kwasu siarkowego(VI) przebiega zgodnie z równaniem:

Zakwaszone związki dichromianów(VI) są często stosowane w laboratorium jako odczynniki utleniające.
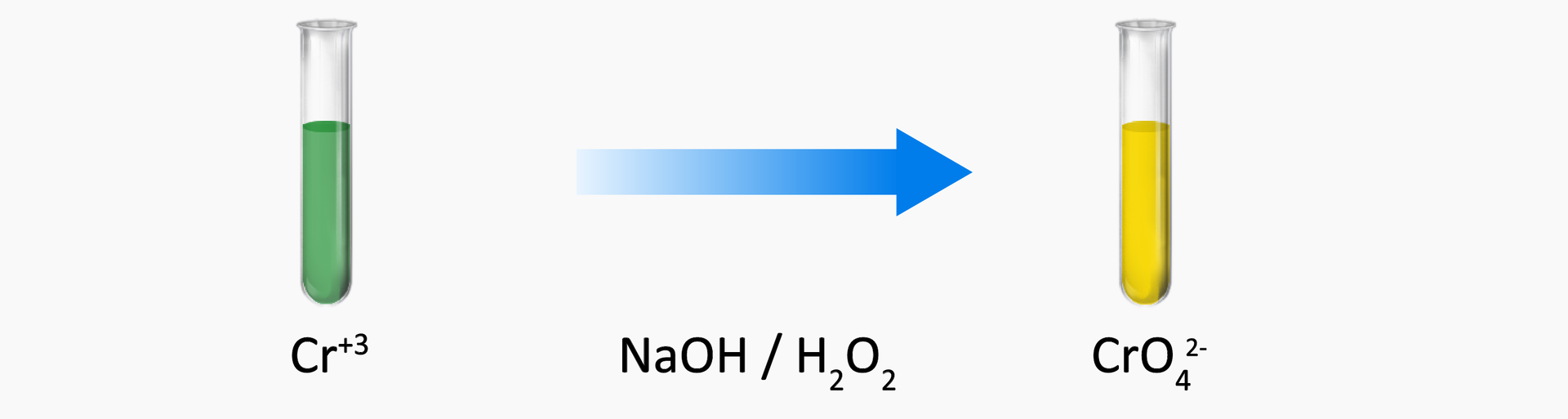
Utlenianie jonów chromu(III) nadtlenkiem wodoru
Utlenianie jonów chromu(III) nadtlenkiem wodoru w środowisku wodorotlenku sodu przebiega zgodnie z równaniem:
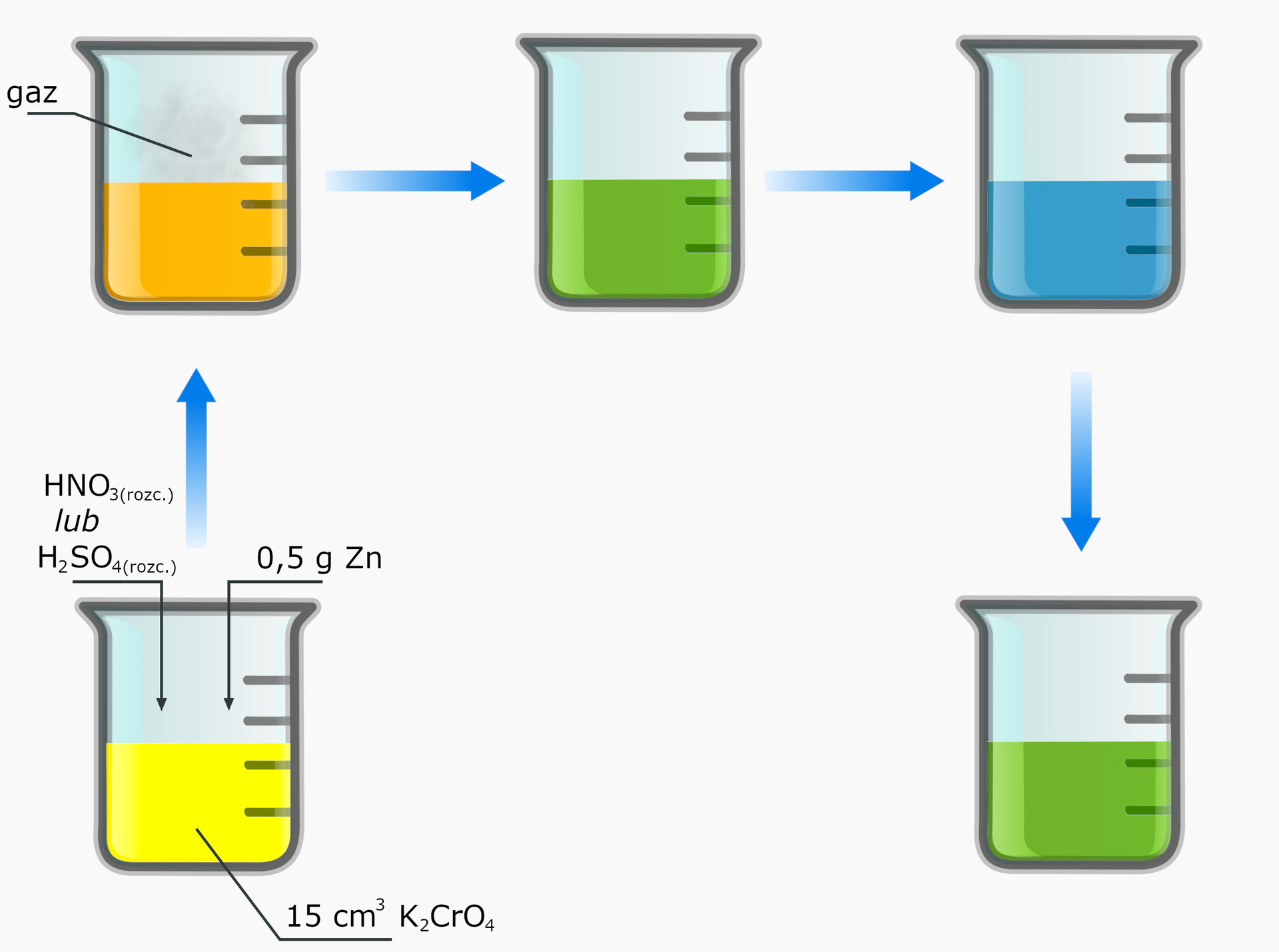
Redukcja chromianu(VI) potasu cynkiem
, Wykonanie: 1. Do probówki nalej 15 cm3 tego roztworu chromianu(VI) potasu.
2. Dodaj niewielką ilość (ok. 0,5 g) pyłu cynkowego.
3. Mieszaninę zakwaś rozcieńczonym roztworem kwasu siarkowego(VI) lub kwasu azotowego(V).
4. Obserwuj zmiany.
W 1774 r. szwedzki aptekarz Karl Wilhelm Scheele także uzyskał chlor ze związku manganu, lecz poprzez ogrzewanie tlenku manganu(IV) z kwasem solnym. Nie został jednak uznany za odkrywcę chloru, ponieważ jego produkt był mieszaniną chloru z powietrzem.
Słownik
reakcja, podczas której atom, jon lub cząsteczka reduktora traci elektrony. Podczas tego procesu stopień utlenienia atomu wzrasta
reakcja, podczas której atom, jon lub cząsteczka utleniacza zyskuje elektrony. Podczas tego procesu stopień utlenienia atomu maleje
reakcja, podczas której zachodzi wymiana elektronów pomiędzy reduktorem i utleniaczem
teoretyczny ładunek, który wykazywałby atom, gdyby wszystkie utworzone przez niego wiązania miały charakter jonowy
sól istniejącego tylko w roztworach wodnych mocnego kwasu; substancja krystaliczyna, rozpuszczalna w wodzie; jej roztwory mają barwę intensywnie różowofioletową; stosowana jako środek utleniający
sole kwasu chromowego(VI) zawierają anion , a dichromowego(VI) – anion ; stosowane jako środek utleniający
Bibliografia
Bielański A., Podstawy chemii nieorganicznej, Warszawa 1987, s. 871‑882, 890‑899.
Czerwiński A., Czerwińska A., Jelińska‑Kazimierczuk M., Kuśmierczyk K., Chemia 1. Podręcznik, Warszawa 2002, s. 297‑327.
Hassy R., Mrzigod A., Mrzigod J., Sułkowski, Chemia 2, Warszawa 2003, s. 326‑335.
Orlińska I., Mangan i jego związki, „Chemia w szkole” 2009, 2, s. 37‑41.