Przeczytaj
Co to są alkiny?
AlkinyAlkiny są węglowodorami, czyli związkami składającymi się z atomów węgla, które są zdolne do tworzenia czterech wiązań, oraz z wodoru. Ze względu na występowanie wiązania potrójnego są związkami bardzo reaktywnymi. W skład wiązania wielokrotnego wchodzi jedno mocne typu ϭ oraz dwa słabe typu pi. Dzięki temu alkiny są podatne na reakcje addycjiaddycji. Jedną z nich jest addycja chloru i bromu. Alkiny reagują z bromem lub chlorem, dając odpowiednie nasycone lub nienasycone halogenopochodne. W przypadku nadmiaru fluorowca otrzymuje się tetrahalogenopochodną alkanu. Natomiast w przypadku niedomiaru – dihalogenopochodną alkenu.
Ogólne równanie reakcji addycji bromu i chloru do cząsteczek alkinów można zapisać w następujący sposób:
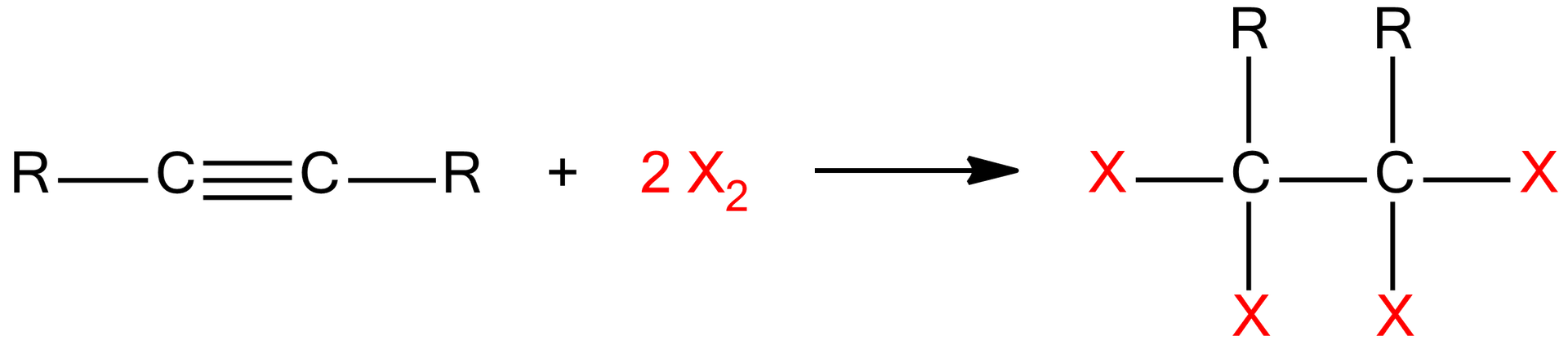
Reakcja ta zachodzi stopniowo poprzez pośredni produkt – halogenopochodną alkenu. Równanie reakcji addycji fluorowca do cząsteczek alkinów można zatem zapisać w postaci dwóch reakcji chemicznych (dwóch etapów) w następujący sposób:
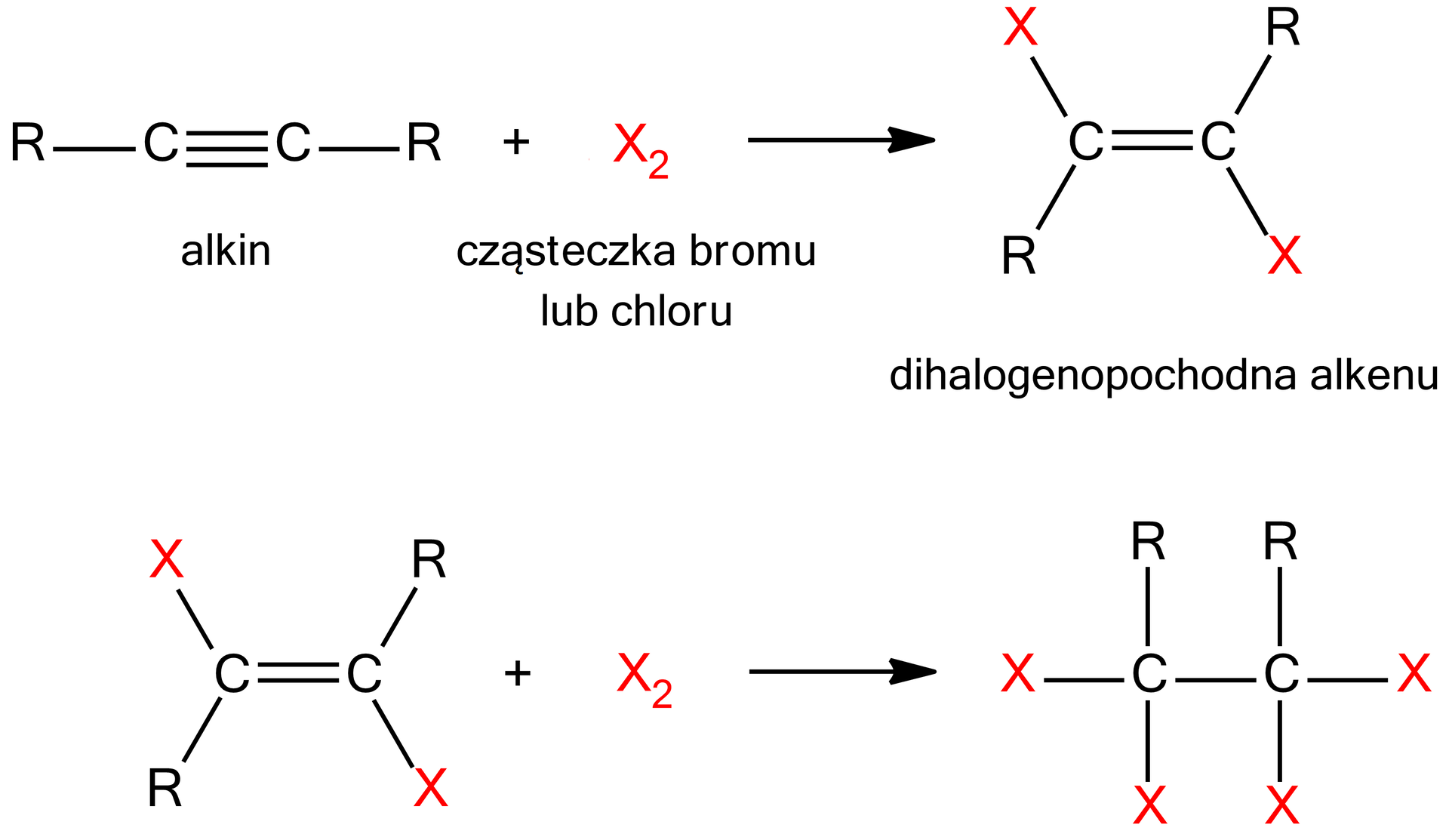
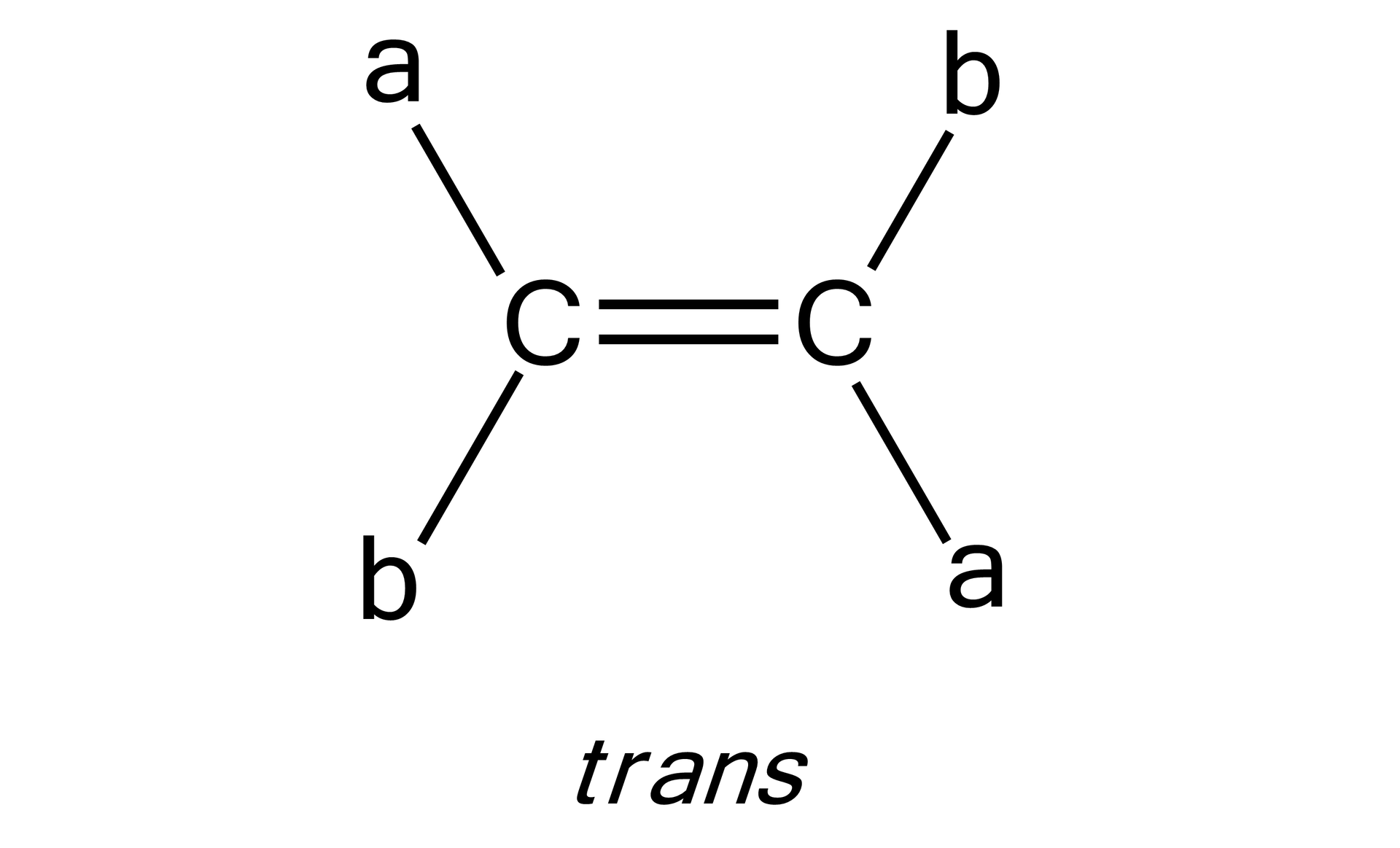
Tworzący się produkt pośredni ma zazwyczaj konfigurację transkonfigurację trans, ze względu na duży promień zarówno bromu, jak i chloru.
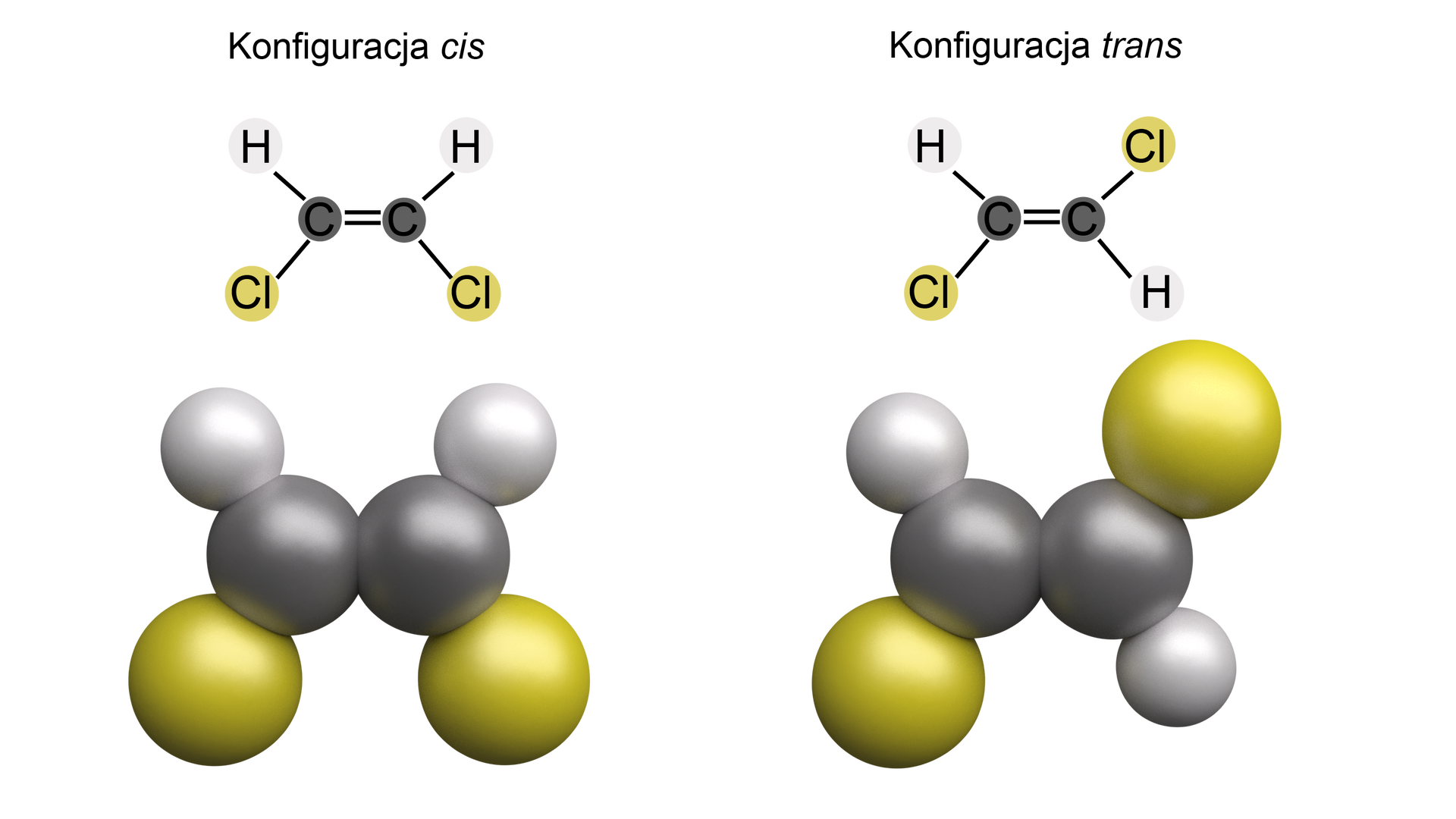
Jaki jest mechanizm reakcji addycji fluorowców do alkinów?
W związku z tym, że w alkinie występują dwa wiązania pi, to wokół atomów węgla wiązania potrójnego występuje pewna gęstość elektronowa. Kiedy cząsteczka zbliża się do cząsteczki alkinu, wiązanie kowalencyjne niespolaryzowane pomiędzy atomami chloru ulega polaryzacji. Wówczas na jednym atomie chloru tworzy się cząstkowy ładunek dodatni, a na drugim – cząstkowy ładunek ujemny. Para elektronów pi alkinu atakuje dodatni biegun cząsteczki chloru, zrywając jednocześnie wiązanie i odpychając jon chlorkowy, który zabiera oba elektrony tego wiązania. ElektrofilElektrofil, czyli , przyłącza się do alkinu, dzięki czemu powstaje karbokation, czyli kation organiczny, w którym atom węgla ma deficyt elektronów. W ten sposób tworzy się na nim ładunek dodatni (1). Jest to zatem atak elektrofilowy. Powstały karbokation to karbokation winylowy – produkt przejściowy, który w dalszej kolejności reaguje z anionem chlorkowym. Para elektronowa jonu chlorkowego atakuje pośredni karbokation, przez co powstaje nowe wiązanie i tworzy się obojętny produkt addycji. Nastąpił więc atak nukleofilowy (czynnika nukleofilowego). Ten etap daje nam dichlorowy produkt addycji, posiadający elektrony pi wiązania podwójnego (2). W związku z tym możliwa jest kolejna addycja cząsteczek chloru w ten sam, analogiczny sposób. Elektrony wiązania pi oddziałują na cząsteczkę chloru, wywołując polaryzację wiązania i przyłączenie odczynnika elektrofilowego do jednego z atomów węgla. Tworzy się wówczas karbokation alkilowyalkilowy (3), do którego przyłącza się anion chlorkowy, dając chlorek alkilowy ,czyli produkt całkowitej addycji chloru do alkinu (4). W takim razie addycja chloru i bromu zachodzi zgodnie z mechanizmem elektrofilowym, ponieważ jako pierwszy następuje atak elektrofilowy.
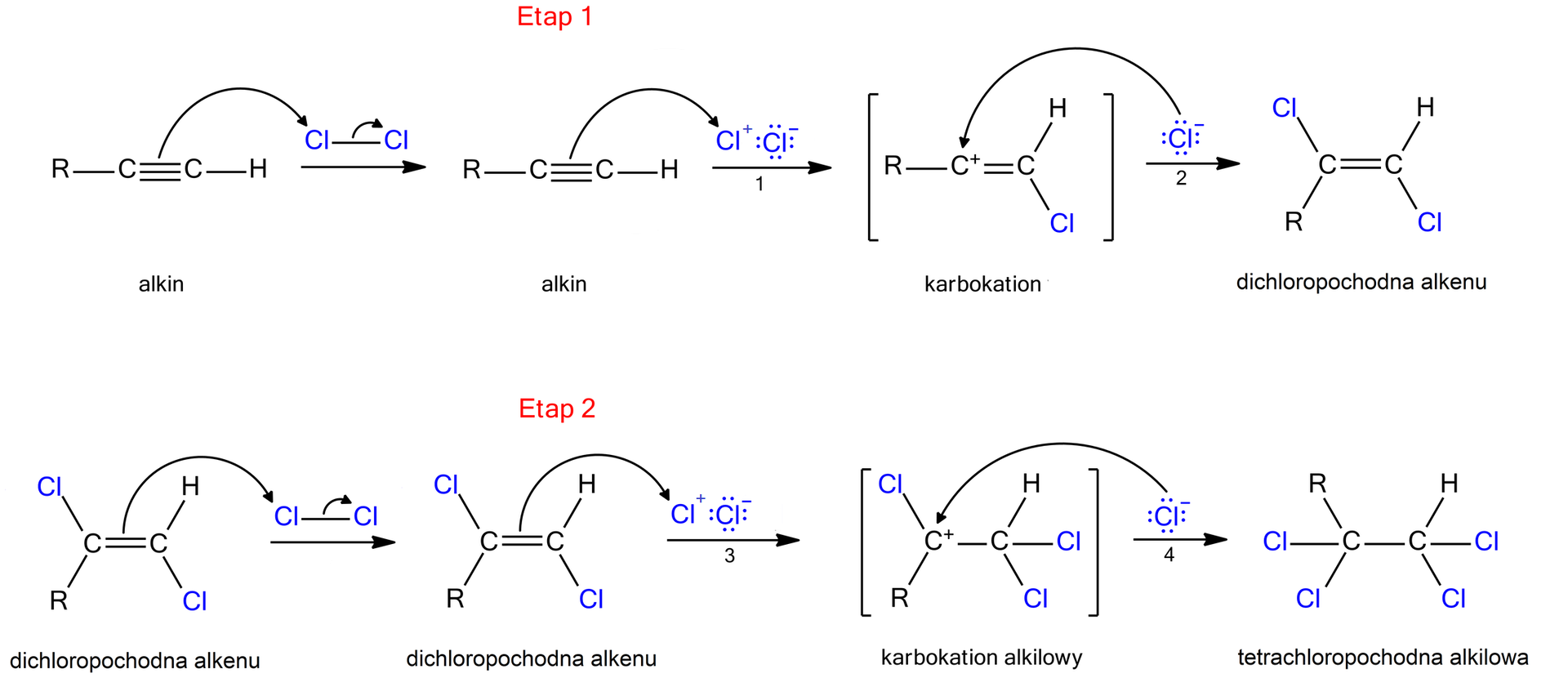
R oznacza dowolna grupę węglowodorową lub atom wodoru
Pamiętaj, że addycja bromu do alkinu stanowi prostą metodą laboratoryjną, potwierdzającą obecność wiązań wielokrotnych. Do próbki badanego związku dodaje się brom rozpuszczony w rozpuszczalniku organicznym (np. tetrachlorometanie ). Odbarwienie pomarańczowo‑brunatnego roztworu świadczy o tym, że próbkę stanowi alkin (lub alken). Jest to więc szybka metoda na odróżnienie węglowodorów nasyconych od nienasyconych.

Co z pozostałymi fluorowcami?
Fluor jest bardzo reaktywny, dlatego w warunkach laboratoryjnych przeprowadzenie reakcji addycji fluoru jest trudne. Jod natomiast nie reaguje z większością węglowodorów nienasyconych. Dlaczego? Wynika to z niekorzystnego efektu energetycznego: wiązanie jest po prostu słabe. Energia potrzebna do rozerwania wiązań oraz przewyższa energię tworzenia wiązań . Wniosek jest jeden – reakcja jest niekorzystna energetycznie.
Słownik
alifatyczne węglowodory nienasycone o wzorze ogólnym , których cząsteczki zawierają jedno wiązanie potrójne między atomami węgla
reakcja addycji, czyli łączenia, w której związek posiadający niedomiar elektronów (elektrofil) przyłącza się do związku chemicznego posiadającego nadmiar elektronów bez powstawania produktów ubocznych
indywiduum chemiczne obdarzone ładunkiem dodatnim (w reakcji bromowania jest to , w reakcji nitrowania , w reakcji chlorowania , w reakcji metylowania itd.)
dział chemii; nauka o budowie przestrzennej cząsteczek związków chemicznych i przestrzennym przebiegu reakcji chemicznych
jedna z możliwości rozmieszczenia atomów lub grup atomów wokół wiązania podwójnego w izomerii geometrycznej; konfiguracja trans oznacza rozmieszczenie po dwóch stronach wiązania podwójnego tych samym atomów lub grup atomów w różnych kierunkach
grupa organiczna wywodząca się z cząsteczki węglowodoru alifatycznego, tworząca się w wyniku oderwania atomu wodoru od cząsteczki alkanu
Bibliografia
Encyklopedia PWN
McMurry J., Chemia organiczna, Warszawa 2000.
McMurry J., Chemia organiczna, Warszawa 2016.