Przeczytaj
Reakcje alkenów z wodą
Alkeny są związkami niepolarnymi i nie rozpuszczają się w wodzie. Co ciekawe, mimo że alkeny nie rozpuszczają się w wodzie, wykazano, że związki te reagują z wodą w środowisku kwasowym w podwyższonej temperaturze. Rolę katalizatorakatalizatora reakcji pełni mocny kwasmocny kwas (np. kwas siarkowy(VI)), a reakcja nazywana jest często hydratacją i przebiega zgodnie z mechanizmem addycjiaddycji elektrofilowej.

W jaki sposób alken przyłącza wodę?
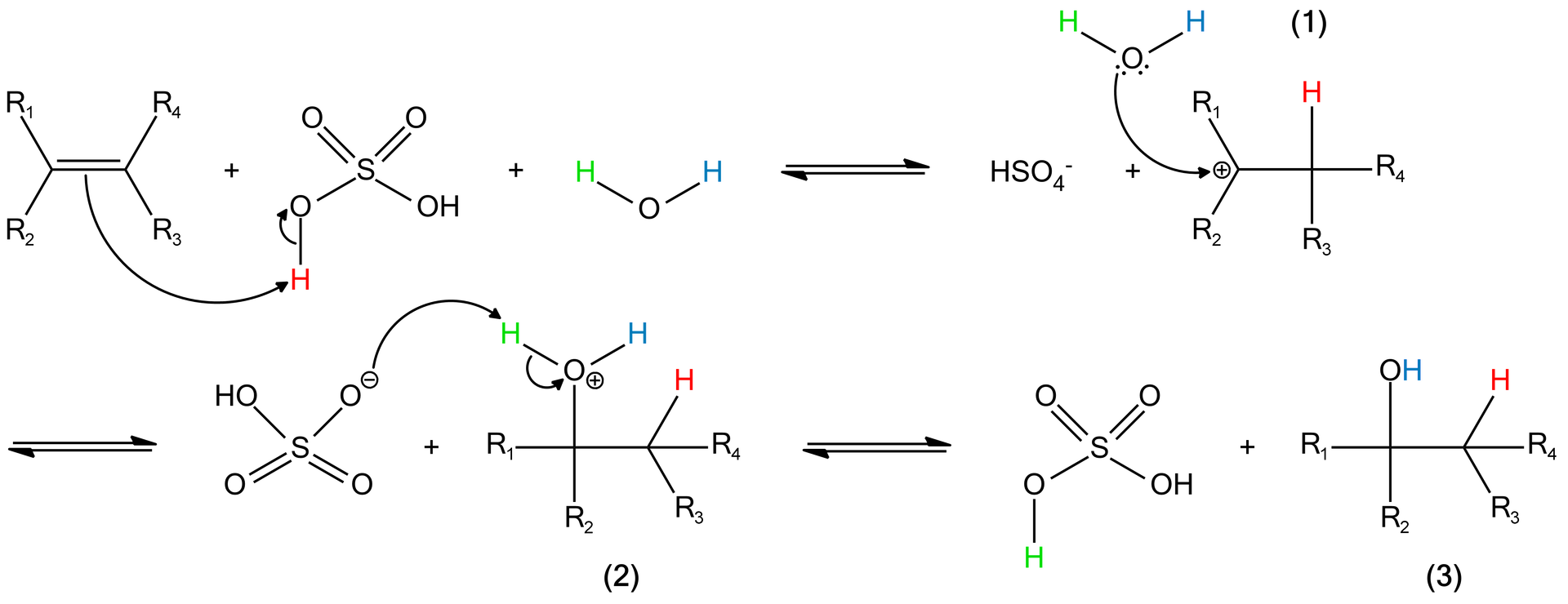
Uwaga: Należy pamiętać, że stabilność karbokationów rośnie z rzędowością, dlatego powstaje zawsze ten najstabilniejszy. Ilustracja przedstawia następującą zależność: trzeciorzędowy atom węgla (kation) łączy się z trzema grupami: u góry R1,a na dole symetrycznie: po lewej stronie z grupą R2, po prawej stronie z grupą R3. Pomiędzy tym wzorem a kolejnym jest znak większe od. Kolejny wzór: drugorzędowy atom węgla (kation) łączy się na górze z grupą R1, a na dole symetrycznie po lewej stronie z grupą R2, po prawej stronie z atomem wodoru. Jest większe od wzór: pierwszorzędowy atom węgla (kation) łączy się na górze z grupą R1, a na dole symetrycznie po lewej i po prawej stronie z atomem wodoru, większe od wzór: atom węgla (kation) łączy się z trzema atomami wodoru.Alkilowe karbokationy w malejącym porządku ich trwałości
Autor: GroMar Sp. z o.o. Licencja: CC BY-SA 3.0, Etap 3 W ostatniej fazie reakcji, anion pochodzący z rozpadu katalizatora odczepia proton z kationu oksoniowego (2), dzięki czemu powstaje elektroobojętny produkt, którym jest alkohol (3). Tym samym zostaje odtworzona cząsteczka katalizatora, jakim jest H2SO4.
Alkeny niesymetryczne i woda
W przypadku alkenów niesymetrycznychalkenów niesymetrycznych, takich jak np. propen, warto zastanowić się, w jaki sposób woda przyłącza się do wiązania podwójnego węgiel‑węgiel.

Okazuje się, że addycja cząsteczki wody do propenu, katalizowana kwasem siarkowym(VI), zachodzi zgodnie z regułą Markownikowaregułą Markownikowa. Reguła ta mówi, że atom wodoru w reakcji addycji przyłącza się do atomu węgla związanego z większą liczbą atomów wodoru („bogatszego w wodór”) i o możliwie najmniejszej rzędowości. Natomiast grupa przyłącza się do karbokationu stabilniejszego, czyli takiego, którego rzędowość jest możliwie największa. Oznacza to, że w przypadku propenu otrzymujemy propan‑2-ol zamiast propan‑1-olu.
Temperatura reakcji stanowi istotny element reakcji addycji wody do cząsteczek alkenów. Ciepło jest wykorzystywane do katalizowania uwodnienia alkenu. Wynika to z faktu, że reakcja przebiega w równowadze z odwodnieniem alkoholu. Dokładne temperatury są bardzo zmienne i zależą od rodzaju tworzonego produktu:
alkohol pierwszorzędowy: mniej niż 170ºC;
alkohol drugorzędowy: mniej niż 100ºC;
alkohol trzeciorzędowy: mniej niż 25ºC.
Źródło: www.chem.libretexts.org, data dostępu 10. 02. 2020 r.
Słownik
(łac. additio „dodawanie”) reakcja przyłączania, chem. reakcja chemiczna, polegająca na przyłączaniu atomów lub cząsteczek związku chemicznego z utworzeniem cząsteczki jednego produktu (adduktu)
elektrofil; cząsteczka lub grupa, w której występuje niedomiar elektronów i w odpowiednich warunkach jest w stanie je przyjąć, czyli być ich akceptorem
nukleofil; cząsteczka lub grupa, w której występuje nadmiar elektronów i w odpowiednich warunkach może być ich donorem
(łac. carbo „węgiel”, gr. katiṓn „idący w dół”) jon karboniowy, kation org., w którym dodatni ładunek wywołany deficytem elektronów jest zlokalizowany na atomie węgla
(gr. katálysis „rozłożenie”) substancja, która zwiększa szybkość, z jaką reakcja chemiczna osiąga stan równowagi, sama się jednak nie zużywa
alkeny, w których cząsteczkach na jednym węglu wiązania podwójnego są przyłączone inne podstawniki niż na drugim węglu wiązania podwójnego;
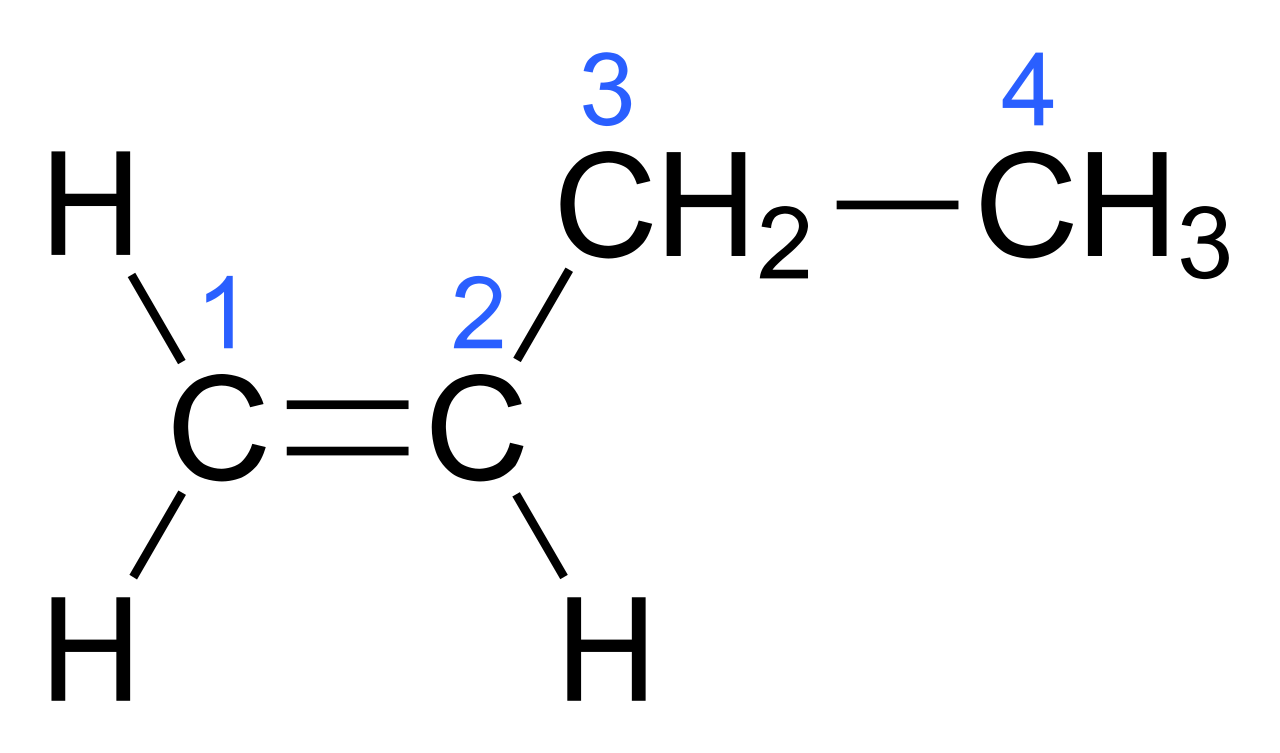
Przykładem jest but‑1-en, w którym do węgla 1 przyłączone są dwa atomy wodoru, a do węgla 2 grupa etylowa oraz atom wodoru.
kwasy, które w roztworach (przy dostatecznie dużym rozcieńczeniu) całkowicie dysocjują na jony, tj. ich stopień dysocjacji elektrolitycznej jest równy 1
reguła określająca przebieg reakcji addycji elektrofilowej do atomów węgla, połączonych podwójnym wiązaniem w cząsteczkach niesymetrycznych węglowodorów nienasyconych
Bibliografia
Encyklopedia PWN
Morrison R. T., Boyd R. N., Chemia organiczna. T. 1, Warszawa 2010.
Pazdro K., Zbiór zadań z chemii dla szkół ponadgimnazjalnych, Warszawa 2003.
Ryczkowski J., Kataliza i technologia chemiczna jako elementy postępu cywilizacyjnego, Wydział Chemii, Uniwersytet Marii Curie-Skłodowskiej w Lublinie.