Przeczytaj
Przyłączanie chloru lub bromu w roztworze wodnym i bezwodnym
AddycjaAddycja elektrofilielektrofili do alkenów jest użyteczną reakcją, ponieważ umożliwia syntezę wielu rodzajów związków. Warto w tym miejscu przyjrzeć się addycji chlorowców do alkenów i sprawdzić, jak warunki reakcji wpływają na rodzaj powstających produktów.
Jakie są produkty reakcji bromu z etenem w opisanych poniżej warunkach?


Reakcja w środowisku chloroformu ()
Reakcja w środowisku
W przypadku niesymetrycznych alkenów, grupa przyłącza się do atomu węgla, związanego atomem węgla o wyższej rzędowości, np.:

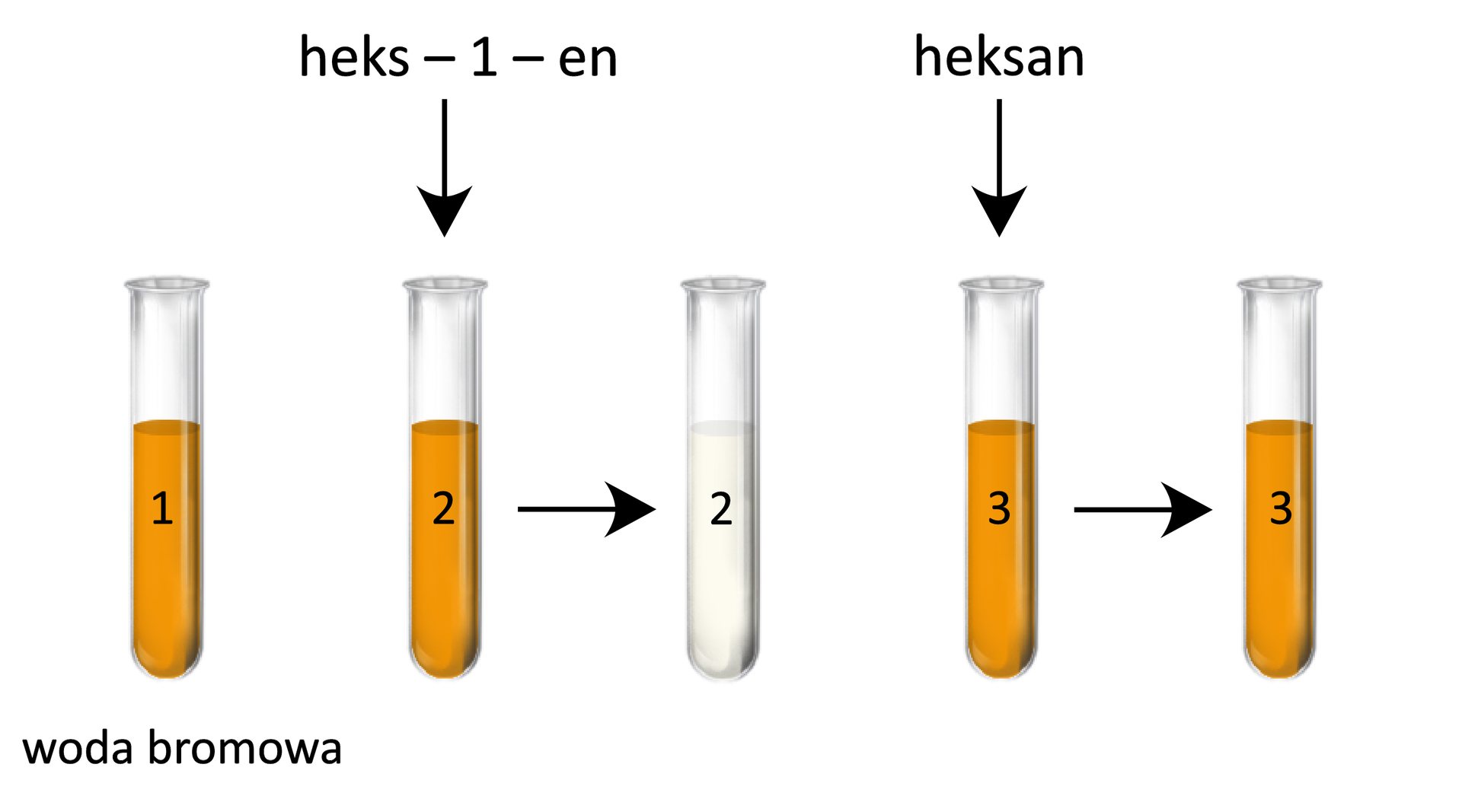
Wykorzystując zgromadzony sprzęt i odczynniki, wykonaj doświadczenie w laboratorium chemicznym, w którym zbadasz zachowanie heks--enu i heksanu wobec wody bromowejwody bromowej. Zaproponuj hipotezę oraz przedstaw schematyczny rysunek doświadczenia. W trakcie doświadczenia zanotuj obserwacje, a następnie zweryfikuj postawioną hipotezę i sformułuj wnioski. Zapisz sumaryczne równania reakcji (związki organiczne przedstaw wzorami półstrukturalnymi) i podaj nazwy produktów organicznych.
Słownik
(łac. additio „dodawanie”) reakcja chemiczna, polegająca na łączeniu się ze sobą atomów lub cząsteczek związków chemicznych (substratów) w cząsteczki jednego związku (produktu), tzw. adduktu
inaczej elektrofil; cząsteczka lub grupa atomów, która ze względu na niedomiar elektronów posiada ładunek dodatni; w odpowiednich warunkach elektrofil jest w stanie przyjąć elektrony, czyli być ich akceptorem
przesunięcie gęstości elektronowej wywołane różnymi czynnikami
inaczej nukleofil; cząsteczka lub grupa atomów, która ze względu na nadmiar elektronów posiada ladunek ujemny; w odpowiednich warunkach może oddać elektrony, czyli być ich donorem
(łac. carbo „węgiel”, gr. katiṓn „idący w dół”) jon karboniowy, kation organiczny, w którym dodatni ładunek, wywołany deficytem elektronów, jest zlokalizowany na atomie węgla
(łac. vicinus „sąsiadów”) związki zawierające dwie grupy funkcyjne przy sąsiednich atomach węgla
(gr. brṓmos „smród”) ok. nasycony roztwór bromu w wodzie o brunatnym zabarwieniu; zazwyczaj jest przechowywana w ciemnych butelkach, co zapobiega reakcjom rozkładu
nasycony roztwór chloru w wodzie; zazwyczaj jest przechowywana w ciemnych butelkach, co zapobiega reakcjom rozkładu
Bibliografia
Buza D., Sas W., Szczeciński P., Chemia organiczna, Warszawa 2006.
Dudek‑Różycki K., Płotek M. , Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków, 2020.
Dudek‑Różycki K., Płotek M. , Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Koziara A., Kociołek K., Zabrocki J., Zjawiony J., Zwierzak A., Zadania i ćwiczenia z chemii organicznej, Łódź 2007.
McMurry J., Chemia organiczna, cz. 2, Warszawa 2010.
Morrison R. T., Boyd R. N., Chemia organiczna, Warszawa 2010.
Pazdro K., Zbiór zadań z chemii dla szkół ponadgimnazjalnych, Warszawa 2003.