Przeczytaj
Wygląd i stan skupienia krzemu
Na podstawie fotografii przedstawiającej krzem, określ jego stan skupienia i barwę.
Na podstawie opisu fotografii przedstawiającej krzem, określ jego stan skupienia i barwę.

Położenie w układzie okresowym
Na podstawie układu okresowego określ symbol chemiczny krzemu, podaj jego średnią masę atomową oraz liczbę atomową. Oblicz także liczbę elektronów walencyjnych, odczytaj elektroujemność i zapisz podpowłokową skróconą (zaw. rdzeń gazu szlachetnego) konfigurację elektronową atomu krzemu w stanie podstawowym.
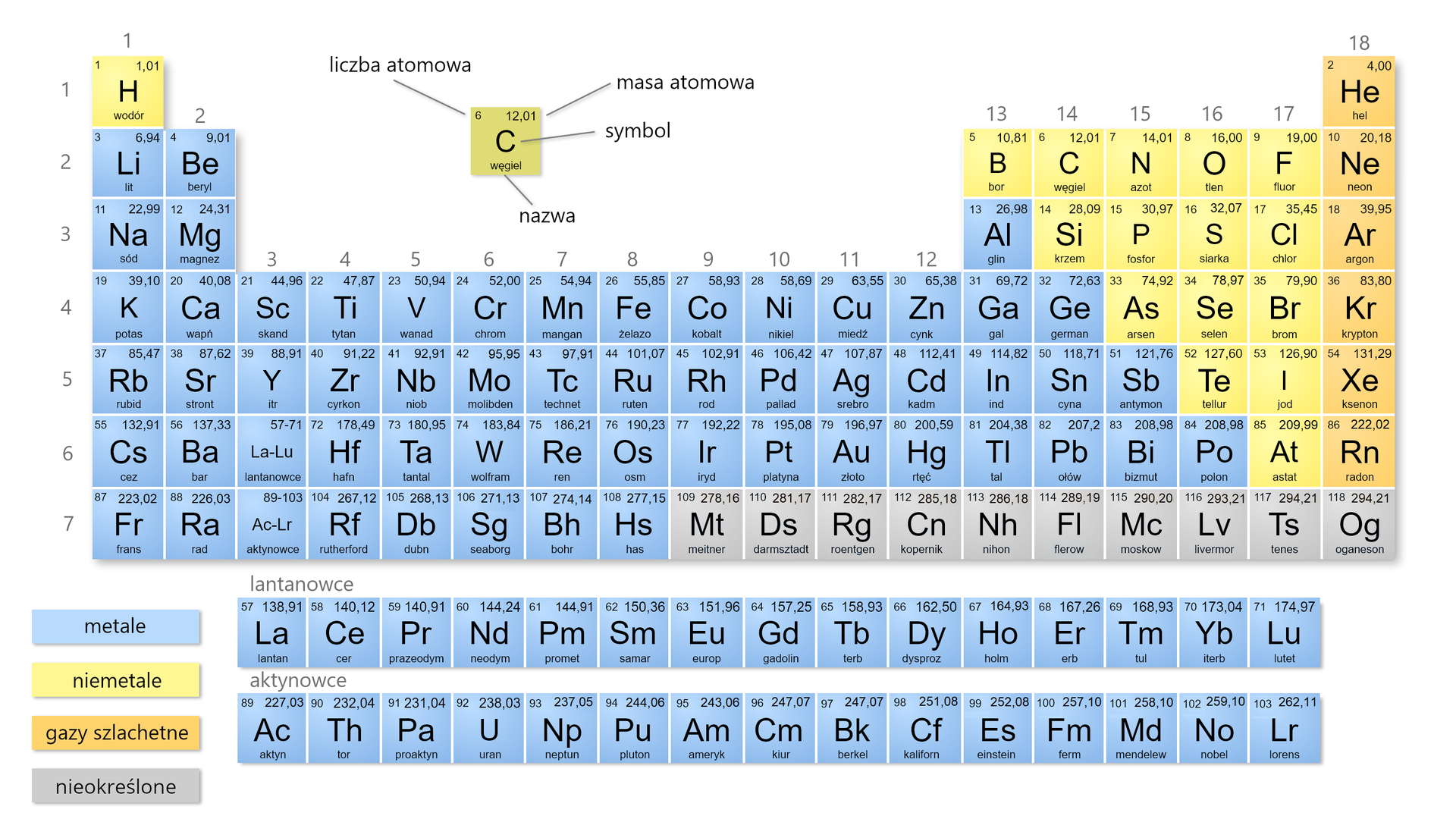
Symbol chemiczny: 1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaście.
Średnia masa atomowa: 1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaście u.
Liczba atomowa: 1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaście.
Liczba elektronów walencyjnych: 1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaście.
Elektroujemność: 1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaście.
Skrócona konfiguracja elektronowa: [1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaście]1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaścies indeks górny, dwa, koniec indeksu górnego1. X e, 2. dwadzieścia osiem przecinek zero dziewięć, 3. cztery, 4. S i, 5. K r, 6. S i O, 7. jeden przecinek osiem, 8. trzy, 9. trzy, 10. Ne, 11. czternaściep indeks górny, dwa, koniec indeksu górnego
Kryształ krzemu
W warunkach normalnych omawiany pierwiastek krystalizuje w odmianie krystalograficznej, charakterystycznej dla diamentu, czyli w układzie krystalograficznymukładzie krystalograficznym regularnym.

Kryształy krzemu są twarde (twardość w skali Mohsaskali Mohsa ), ale jednocześnie kruche. Charakteryzują się gęstością, wynoszącą , oraz temperaturą topnienia o wartości . Krzem występuje również w innych odmianach. Są one jednak trwałe tylko w warunkach wysokiego ciśnienia.
Izotopy krzemu
Występuje naturalnie w postaci trzech izotopówizotopów: izotopu krzemu o liczbie masowej , którego zawartość procentowa wynosi , izotopu krzemu o liczbie masowej oraz procentowej zawartości w przyrodzie równej , a także izotopu krzemu, który posiada liczbę masową równą , a zawartość procentową .
- Nazwa kategorii: Izotopy krzemu{color=#A90D4F}
- Nazwa kategorii: Si‑28 (92,23%){color=#E70C6A}
- Nazwa kategorii: Si‑29 (4,67%){color=#E70C6A}
- Nazwa kategorii: Si‑30 (3,10%){color=#E70C6A} Koniec elementów należących do kategorii Izotopy krzemu{color=#A90D4F}
- Elementy należące do kategorii Izotopy krzemu
Właściwości półprzewodnikowe
Krzem wykazuje właściwości półprzewodnikowe. Przewodnictwo elektryczne krzemu rośnie, gdy wzrasta temperatura lub przez wprowadzenie domieszek. Dzięki właściwościom półprzewodnikowym, wykorzystuje się go przy konstruowaniu tranzystorów.
Można przyjąć, że całkowicie czysty krzem zupełnie nie przewodzi prądu elektrycznego (przewodnictwo krzemu jest mniej więcej razy gorsze niż szkła), ale wystarczają już nadzwyczaj małe domieszki innych materiałów, które praktycznie zawsze w nim występują, aby przewodnictwo zwiększyło się zauważalnie.

Dolina krzemowa (ang. Silicon Valley)
To nazwa nadana północnej części Doliny Santa Clara. Od lat wieku region ten stanowi centrum amerykańskiego sektora zaawansowanych technologii.
Aktywność chemiczna
Krzem w warunkach normalnych jest mało aktywny chemicznie, ponieważ pokryty jest cienką warstewką tlenku krzemu().
Krzem spala się w powietrzu po silnym ogrzaniu:
Z fluorem reaguje już w warunkach normalnych, czego efektem jest widoczny płomień; z innymi fluorowcami krzem reaguje dopiero po ogrzaniu:
Metale ogrzewane z krzemem tworzą krzemki, np. , , , :
Krzem jest odporny na działanie kwasów, reaguje jedynie z mieszaniną kwasu azotowego() i fluorowodorowego:
Otrzymany kwas heksafluorokrzemowy po ogrzaniu rozkłada się na fluorowodór i tetrafluorek krzemu:
Słownik
powszechnie używana skala służąca do określania względnej twardości minerałów
każdy z atomów tego samego pierwiastka chemicznego, który ma jednakową liczbę protonów, lecz różne liczby neutronów
sześć rodzajów sieci przestrzennych różniących się kształtem i rozmiarami komórek elementarnych (wartościami stałych sieciowych) oraz symetrią
Bibliografia
Bielański A., Podstawy chemii nieorganicznej 2, Warszawa 2013.
Słownik PWN