Przeczytaj
Rzędowość
Jest to termin stosowany przy opisie budowy związku chemicznego, który określa stopień podstawienia atomu w cząsteczce. Najczęściej jest jednak używany w chemii organicznej, zwykle do wskazania liczby atomów lub grup organicznych, przyłączonych do danego atomu węgla (lub innego atomu np. azotu). Znajomość rzędowościrzędowości atomu węgla pozwala na scharakteryzowanie ogólnych właściwości związków i umożliwia przewidywanie przebiegu niektórych reakcji chemicznych. Niekiedy termin jest używany również w chemii nieorganicznej do opisu soli, pochodzących od kwasów wieloprotonowych.
Rzędowość związków organicznych
Rzędowość atomów węgla w węglowodorach
Rzędowość atomu węgla to w praktyce liczba atomów węgla bezpośrednio z nim połączonych. Czasem można spotkać „rzędowość” w odniesieniu do atomów wodoru, w tym znaczeniu, że atomy wodoru mają taką samą rzędowość jak atomy węgla, z którymi są związane. Określenie rzędowości atomów wodoru jest błędem i za taki należy uznawać wszelkie próby używania tego skrótu myślowego. Mało tego – pamiętaj, że rzędowość powinna być określana w praktyce tylko dla atomów węgla o tetraedrycznej hybrydyzacji orbitali walencyjnych. Do oznaczenia rzędowości mogą służyć cyfry rzymskie lub arabskie – te ostatnie z symbolem ().
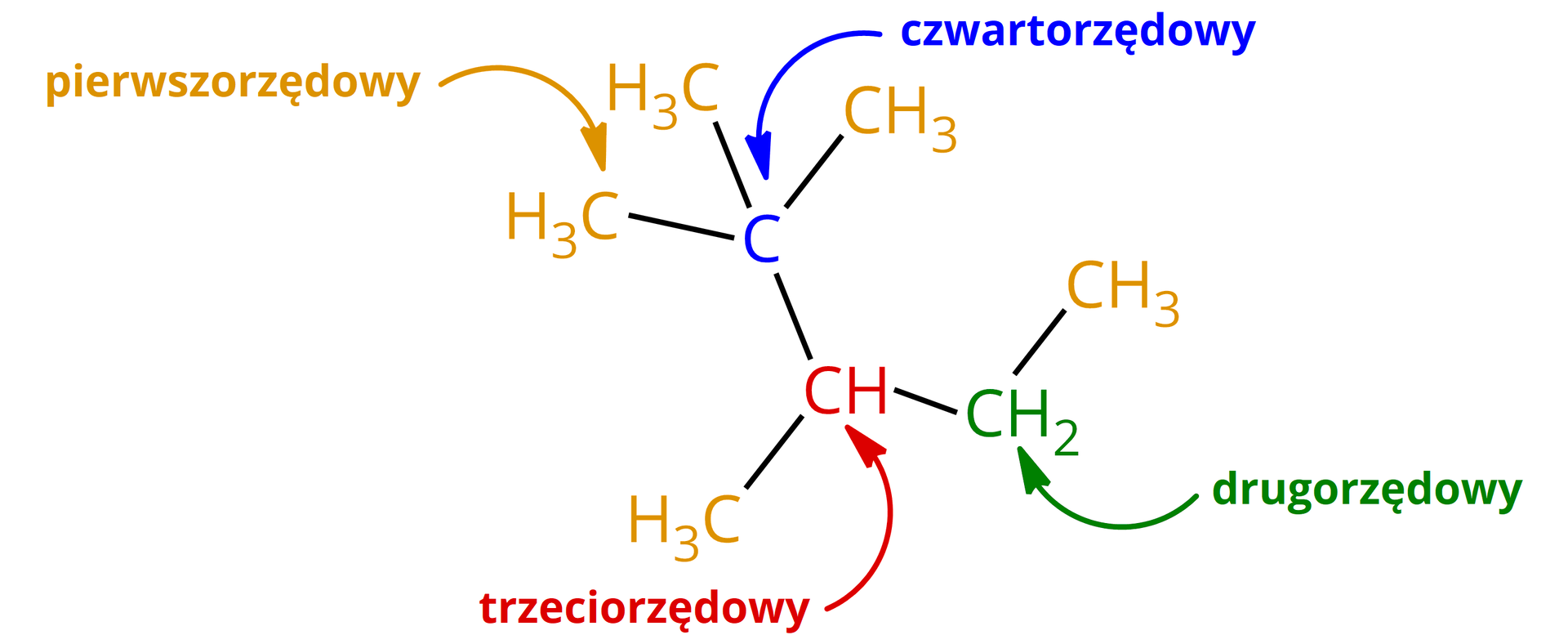
Wiemy już, jak wyznaczyć rzędowość atomów węgla węglowodorów alifatycznych, kiedy w cząsteczce związku znajduje się kilka atomów węgla. Tak jak to ma miejsce w przypadku metanu, w cząsteczce którego znajduje się jeden atom węgla, połączony z czterema atomami wodoru, co oznacza, że nie łączy się on z innym atomem węgla. Jest to jedyny taki przypadek i należy mu się szczególna uwaga. Mamy wtedy do czynienia z rzędowością równą zero. Zdecydowanie to jedyny taki związek.
Rzędowość atomów węgla w innych klasach związków
Rzędowość związku, np. w przypadku m.in. alkoholi, jest równa rzędowości atomu węgla, do którego przyłączona jest odpowiednio grupa hydroksylowa. Wynika to z faktu, że podstawniki te nie mają możliwości utworzenia wiązań z więcej niż jednym atomem węgla. Nierealne jest zatem istnienie czwartorzędowego alkoholu, nitrozwiązku, halogenku alkilowego, ponieważ wtedy jeden z atomów węgla byłby połączony aż z czterema innymi atomami węgla, a więc podstawnik nie mógłby się już przyłączyć do tego atomu węgla.
Na przykład rzędowość alkoholi:
Podobnie jak w powyższym przypadku, rzędowość wyznacza się dla atomów azotu w aminach, arsenu w arsynach, bizmutu w bizmutynach, fosforu w fosfinach i antymonu w stybinach oraz dla grup alkilowych, karbokationów, karborodników, karboanionów.
Oznaczenia rzędowości w pisowni
Do oznaczenia rzędowości mogą służyć cyfry rzymskie lub arabskie – te ostatnie z symbolem (). W literaturze rzędowość oznacza się formą skróconą, czyli zapisem złożonym z cyfry arabskiej i znaku stopnia, np. alkohol oznacza alkohol pierwszorzędowy. Ten słowny opis jest również stosowany – alkohol oznacza alkohol drugorzędowy itd.
Zależność właściwości związków od ich rzędowości.
Rzędowość związku dla większości grup związków organicznych wiąże się z ich stabilnością, co oczywiście przekłada się na różne zachowanie związków w trakcie reakcji chemicznej i wpływa na powstanie w jej wyniku różnych produktów. Wraz ze wzrostem rzędowości, zwiększa się również zawada przestrzennazawada przestrzenna. O zawadzie przestrzennej mówimy wtedy, gdy rozmiar grup funkcyjnych w cząsteczce powoduje brak dostępu czynnika atakującego do potencjalnego miejsca aktywnego.
Słownik
liczba atomów węgla, związanych z danym tetraedrycznym atomem węgla wiązaniami pojedynczymi
przeszkoda, która w pewnych warunkach może utrudnić lub uniemożliwić przereagowanie cząsteczki; ma miejsce wtedy, gdy rozmiar grup funkcyjnych w cząsteczce powoduje brak dostępu czynnika atakującego do jej potencjalnego miejsca reakcji
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
McMurry J., Chemia organiczna. Halogenki alkilowe, tłum. H. koroniak i in., t. 2, Warszawa 2013.
Morrison R. T., Boyd R. N., Chemia organiczna, Warszawa 1997.