Przeczytaj
Węglowodory aromatyczne
Węglowodory aromatyczneWęglowodory aromatyczne (areny) to pierścieniowe związki organiczne, składające się z atomów węgla i wodoru. Aby przypisać związek chemiczny do węglowodorów aromatycznych, musi on spełniać równocześnie następujące warunki:
musi być związkiem pierścieniowym;
pierścienie muszą wykazywać konformację płaską – czyli znajdować się w jednej płaszczyźnie – oraz atomy węgla, tworzące pierścień, muszą posiadać hybrydyzację ;
liczba zdelokalizowanych elektronów musi spełniać regułę Hückla, czyli musi być równa , gdzie jest liczbą naturalną lub zerem;
musi posiadać zdelokalizowane wiązania , obejmujące wszystkie atomy węgla w pierścieniu, co nadaje wiązaniom węgiel‑węgiel charakter pośredni pomiędzy wiązaniem pojedynczym a podwójnym.
W przypadku cyklicznych węglowodorów, zbudowanych z wielu atomów węgla (ośmiu lub więcej), hybrydyzacja atomów węgla pierścienia może nie być wystarczająca do zachowania przez niego płaskiej struktury, która wymagana jest do tego, aby związek był aromatyczny.
Warto zaznaczyć, że jeśli dany węglowodór cykliczny jest karboanionem lub karbokationem, wtedy atomy węgla, na których zlokalizowany jest ładunek, przyjmują hybrydyzację .
Pierścień cyklopropenu wykazuje płaską konformację, jednak jeden z atomów węgla w pierścieniu posiada hybrydyzację , dlatego cyklopropen nie jest związkiem aromatycznym, mimo spełnienia reguły Hückla.
Określ, które z poniższych związków chemicznych, przedstawionych za pomocą wzorów półstrukturalnych, należą do węglowodorów aromatycznych, a które nie. Odpowiedź uzasadnij.
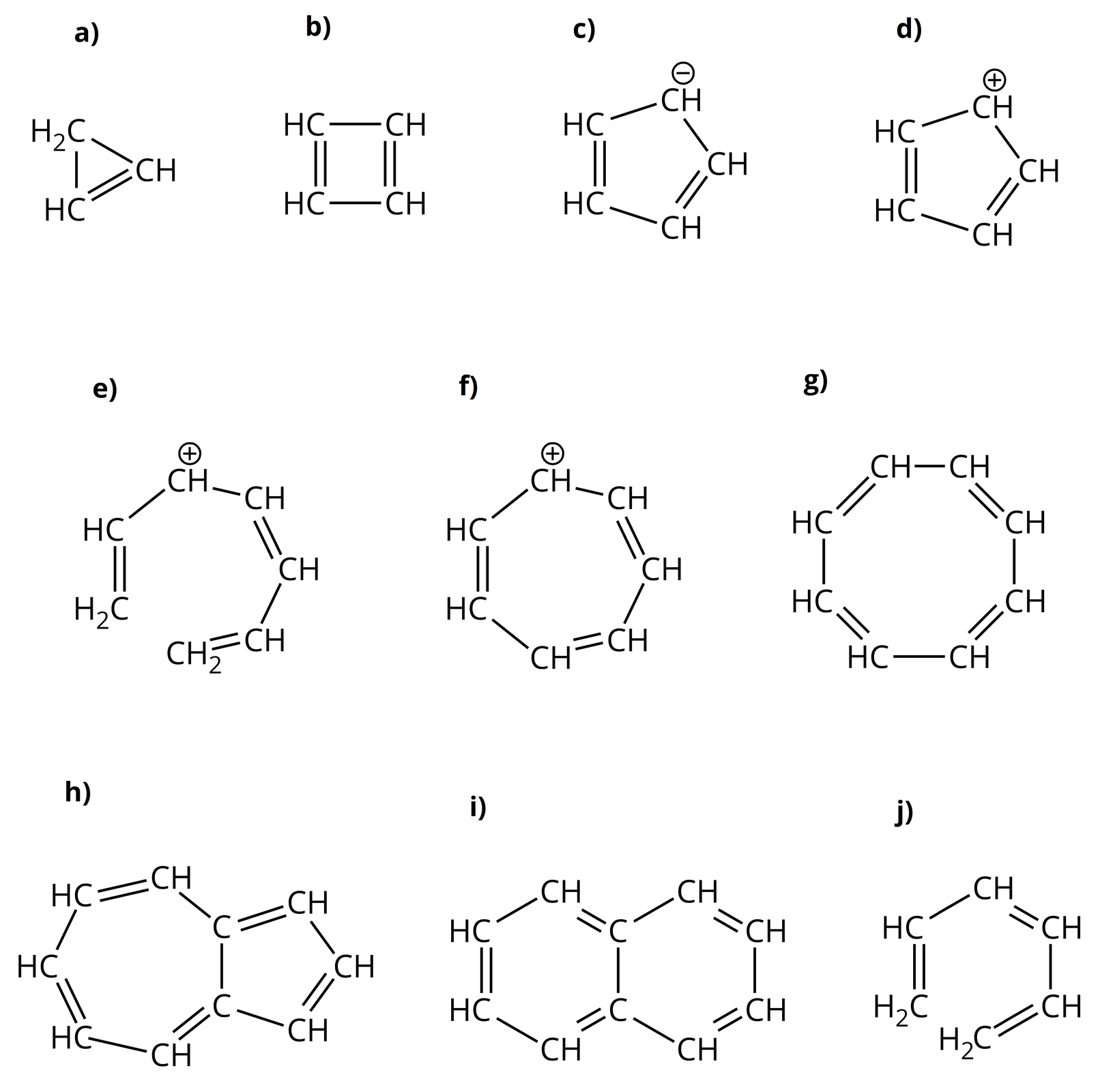
Występowanie i zastosowanie węglowodorów aromatycznych
Związki aromatyczne spełniają określone reguły – są płaskie (lub nieznacznie pofałdowane), cykliczne, wszystkie atomy węgla w pierścieniu są ze sobą połączone zdelokalizowanymi wiązaniami , co sprawia, że wszystkie te wiązania są identyczne, a liczba zdelokalizowanych elektronów jest równa . Ze względu na swoje właściwości, znajdują szereg zastosowań w medycynie czy w syntezie organicznej.
Słownik
(gr. isos „równy”, meros „część”) związki chemiczne o tym samym wzorze sumarycznym, ale posiadające inny sposób lub kolejność wiązań atomowych albo inne rozmieszczenie w przestrzeni
odmiana alotropowa węgla, składająca się z pojedynczych warstw atomów węgla ułożonych w układzie sześciokątnym; wykazuje ciekawe właściwości i cechy strukturalne, takie jak: dwuwymiarowość, wysoka wytrzymałość, elastyczność, przezroczystość, wysoka przewodność cieplna i elektryczna
węglowodory o cząsteczkach, w których występuje płaski pierścień z układem sprzężonych wiązań podwójnych, w których występuje elektronów
()
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
McMurry J., Chemia organiczna, t. 3, Warszawa 2017.
Vollhardt P., Schore N. E., Organic Chemistry: Structure Function, 6th Edition, London 2009.