Przeczytaj
Charakterystyka azanu
Azan jest związkiem o wzorze sumarycznym – to nic innego jak cząsteczka, którą znasz pod nazwą amoniak. Cząsteczka amoniaku jest zbudowana z atomu azotu, połączonego z trzema atomami wodoru. Azot znajduje się w 15. grupie układu okresowego i należy do bloku energetycznego pbloku energetycznego p. Atom azotu posiada 5 elektronów walencyjnych. W cząsteczce azanu 3 elektrony azotu tworzą wiązania z atomami wodoru, a pozostałe dwa tworzą wolną parę elektronową.

Orbitale walencyjne atomu azotu są w stanie hybrydyzacjihybrydyzacji spIndeks górny 33, a cząsteczka azanu przyjmuje kształt piramidy trygonalnej. Kąt między wiązaniami azot‑wodór w cząsteczce azanu wynosi 106°45’, co jest wartością mniejszą niż kąty między wiązaniami w cząsteczce metanu (109°28’). Zmniejszenie tego kąta wynika z silniejszego odpychania pomiędzy wolną parą elektronową, a wiążącą parą elektronową w cząsteczce azanu.
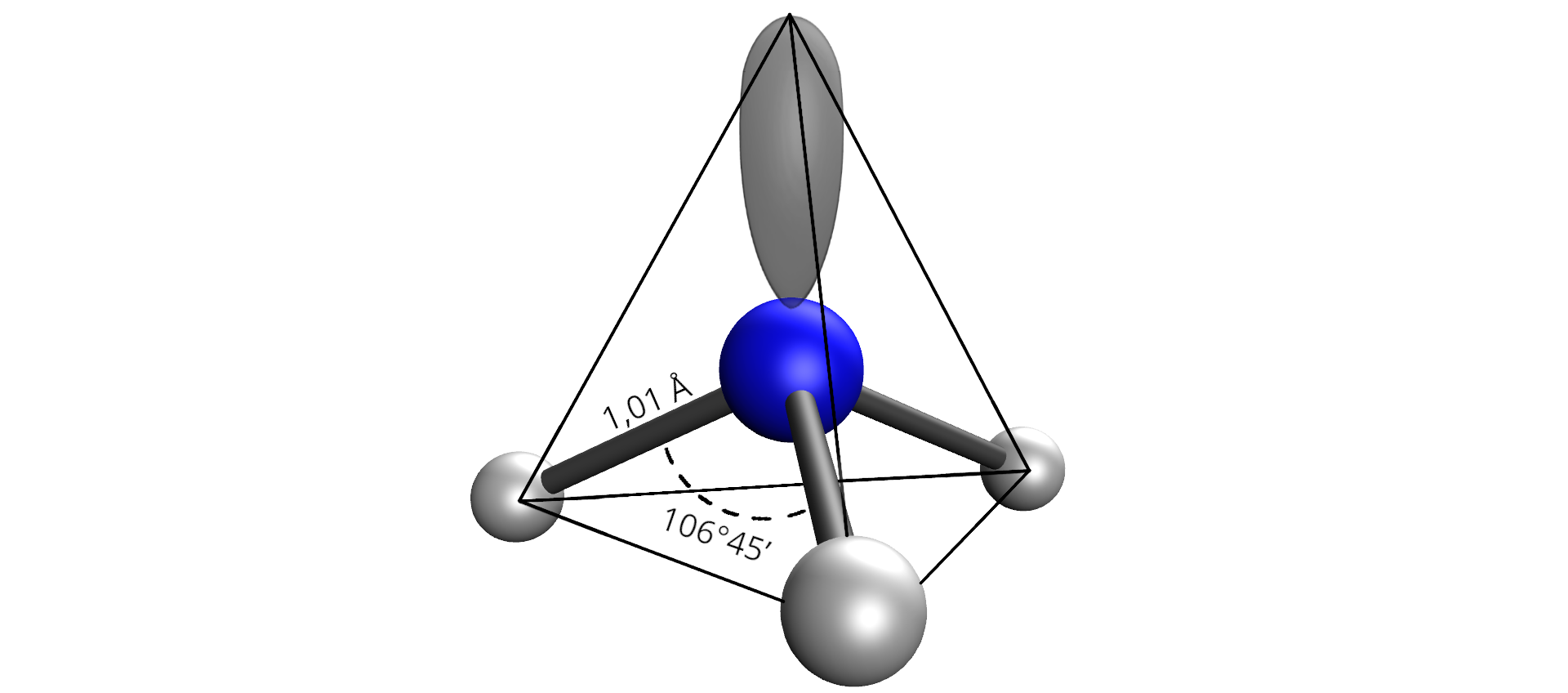
Wartość elektroujemnościelektroujemności atomu azotu w skali Paulinga wynosi 3,0, a atomu wodoru 2,1. Różnica tych wartości wynosi 0,9, co sugeruje występowanie wiązania kowalencyjnego spolaryzowanego w cząsteczce azanu. Można również zauważyć, że cząsteczka ta nie jest symetryczna (posiada budowę przestrzenną). Azan jest dipolem o dużym momencie dipolowymmomencie dipolowym (mu = 1,47 D). Taka wartość świadczy o tym, że cząsteczka azanu jest cząsteczką polarną i powinna dobrze rozpuszczać się w wodzie.

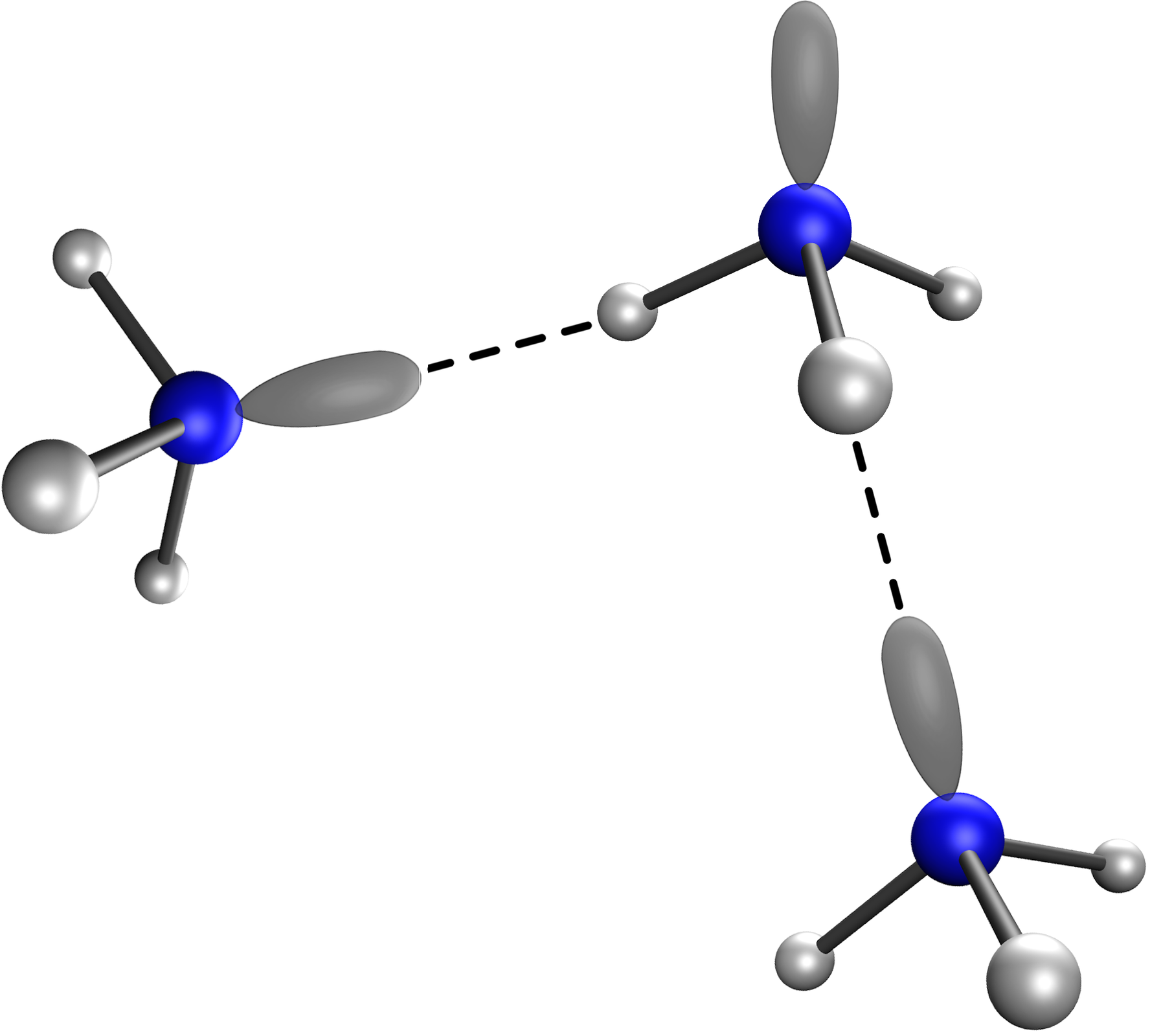
Amoniak w temperaturze pokojowej jest gazem lżejszym od powietrza. Jego temperatura wrzenia wynosi -33,35°C, w przypadku metanu wynosi ona -164°C, a wody aż 100°C. Ciekły amoniak ma właściwości podobne do wody, rozpuszcza związki nieorganiczne, jednak dużo gorzej niż woda. W roztworze amoniak może wytworzyć sieć wiązań wodorowychwiązań wodorowych.
Słownik
należą do niego pierwiastki z grup od 13. do 18. układu okresowego
(łac. hybrida „krzyżówka”, „mieszaniec”) matematyczny zabieg, pozwalający na otrzymanie mieszanych orbitali elektronowych za pomocą linowych kombinacji wybranych funkcji falowych
miara zdolności atomów w cząsteczkach związków chemicznych do przyciągania elektronów
wielkość wektorowa charakteryzująca, opisująca rozkład ładunku elektrycznego w cząsteczce związku
rodzaj oddziaływania międzycząsteczkowego; w wiązaniu wodorowym atom wodoru tworzy mostek łączący dwa elektroujemne (elektroujemność) atomy X–H...Y; z jednym z nich (X) połączony jest wiązaniem kowalencyjnym spolaryzowanym (wiązanie chemiczne), a z drugim — siłami elektrostatycznymi
Bibliografia
Bielański A. Podstawy chemii nieorganicznej, Warszawa 2007.
Albert Cotton F., Wilkinson G., L. Gaus P., Chemia nieorganiczna. Podstawy, Warszawa 2002.
Encyklopedia PWN
Mendiara S. N., Perissinotti L.J., Tetrahedral Geometry and the Dipole Moment of Molecules, „Journal of Chemical Education” 2002, nr 1.