Przeczytaj
Karbokationy
Kabokationem nazywamy kation o cząstkowym ładunku dodatnim na atomie węgla. Karbokationy powstają na skutek oderwania anionu wodorkowego od cząsteczki organicznej, który zabiera również jeden z elektronów węgla.
Trwałość karbokationów
W celu zmierzenia trwałości karbokationów, można obliczyć ilość energii potrzebnej do utworzenia karbokationu z odpowiedniego halogenku:
gdzie:
– grupa alkilowa;
– atom halogenu;
– karbokation;
– anion halogenkowy.
Im bardziej podstawiony halogenek alkilowy, tym mniej energii potrzeba do jego dysocjacji, a więc dysocjuje łatwiej. W związku z tym wyżej rzędowe karbokationy powstają łatwiej, czyli charakteryzują się większą trwałością.

Karbokation może ulec przegrupowaniu, tak aby utworzyć karbokation bardziej trwały.
Karbokationowy mechanizm addycji
Dwuetapowy karbokationowy mechanizm addycji do alkanów nie jest udowodniony, ale wszystkie znane fakty wskazują, że jest on najbardziej prawdopodobny. W latach 30. XX w. Frank C. Whitmore na podstawie przeprowadzonych reakcji stwierdził, że w ich trakcie zachodzą przegrupowania strukturalne. Wniosek ten został wyciągnięty ze względu na otrzymanie dwóch produktów. Przykładem jest reakcja 3‑metylobut‑1-enu (alkenu) z , w wyniku której otrzymuje się oczekiwany 2‑chloro‑3-metylobutan, ale także 2‑chloro‑2-metylobutan.
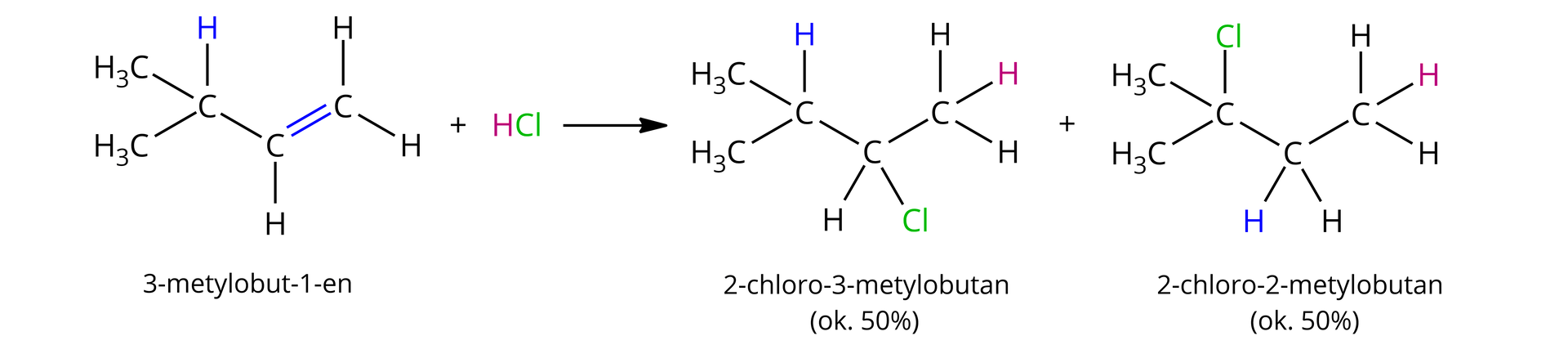
Whitmore zasugerował, że w reakcji pośredniej dochodzi do przegrupowania karbokationu, a więc przejścia dwurzędowego karbokationu do trwalszego karbokationu trzeciorzędowego. W przypadku powyższej reakcji, dzieje się to na skutek przeniesienia jonu wodorkowegojonu wodorkowego między sąsiadującymi ze sobą atomami węgla.
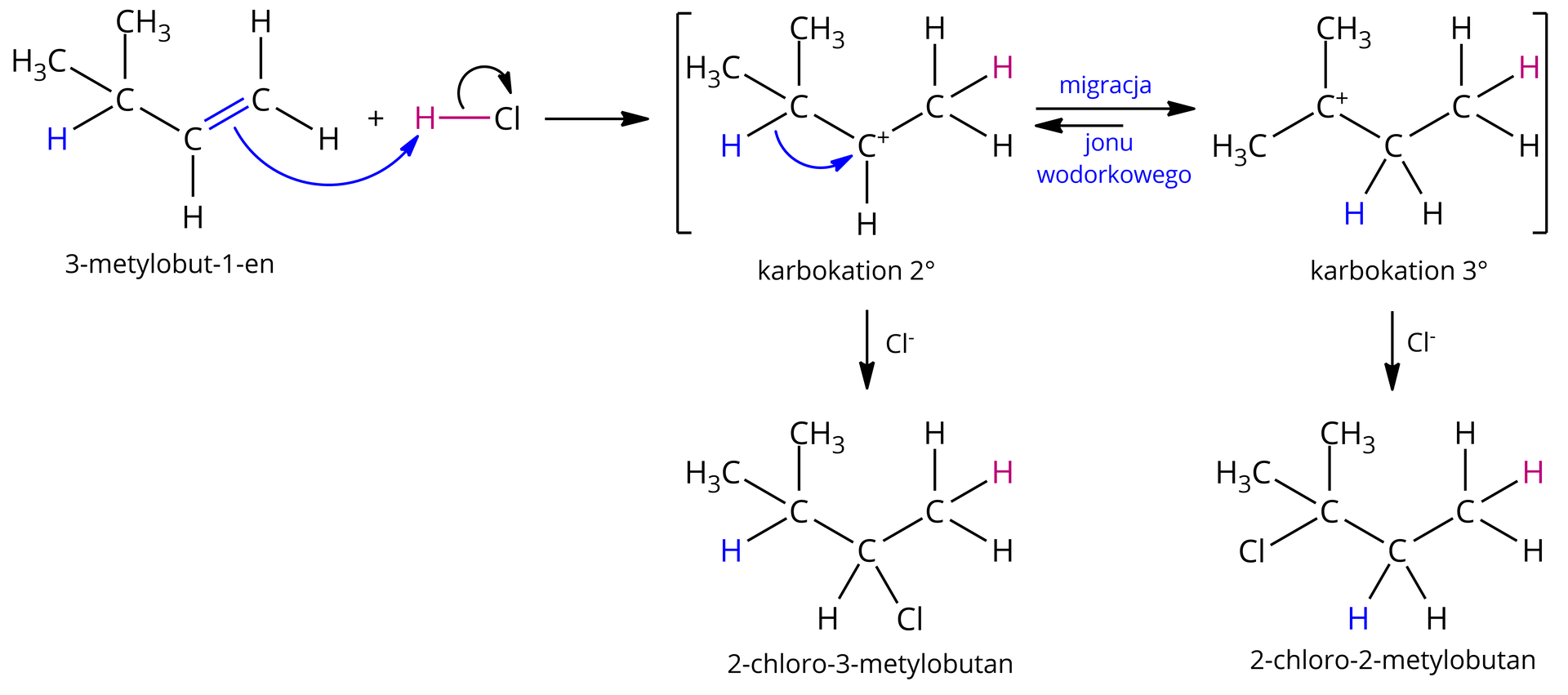
Przeniesienie jonu wodorkowego (ang. hydride shift)
Atom wodoru migruje wraz z parą elektronową, tworzącą wiązanie między nim a atomem węgla (grupa migrująca), do sąsiedniego atomu węgla posiadającego ładunek dodatni. W ten sposób atom węgla, który utracił jon wodorkowyjon wodorkowy, zyskuje ładunek dodatni. Jest to przykład przegrupowania 1,2 (ang. 1,2‑shift), podczas którego grupa migrująca przemieszcza się od jednego atomu do drugiego, czyli tego najbliższego.
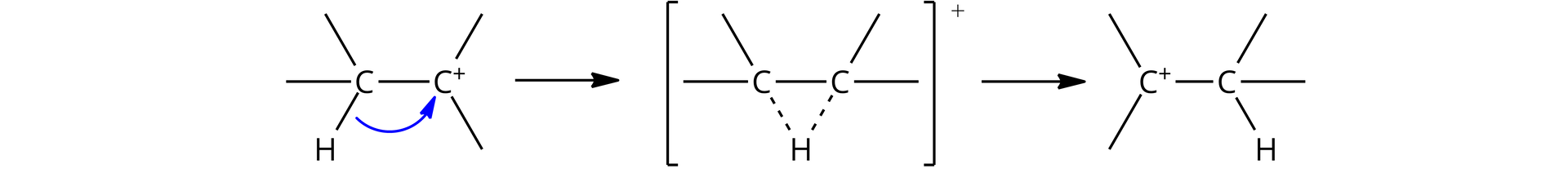
Przeniesienie grupy alkilowej (ang. alkyl shift)
Grupa alkilowaGrupa alkilowa migruje wraz z parą elektronową, tworzącą wiązanie między nim a atomem węgla (grupa migrująca), do sąsiedniego atomu węgla posiadającego ładunek dodatni. W ten sposób atom węgla, który utracił grupę migrującą, zyskuje ładunek dodatni. Jest to kolejny przykład przegrupowania 1,2 (ang. 1,2‑shift), podczas którego grupa migrująca przemieszcza się od jednego atomu do drugiego, czyli tego najbliższego.

Przykładem przegrupowania z przeniesieniem grupy alkilowej, a dokładniej metylowej, jest reakcja 3,3‑dimetylobut‑1-enu z HCl. W etapie pośrednim tworzy się karbokation drugorzędowy, który w wyniku przeniesienia grupy metylowej przekształca się w karbokation trzeciorzędowy. W wyniku reakcji otrzymywany jest oczekiwany 2‑chloro‑3,3‑dimetylobutan, ale także 2‑chloro‑2,3‑dimetylobutan.
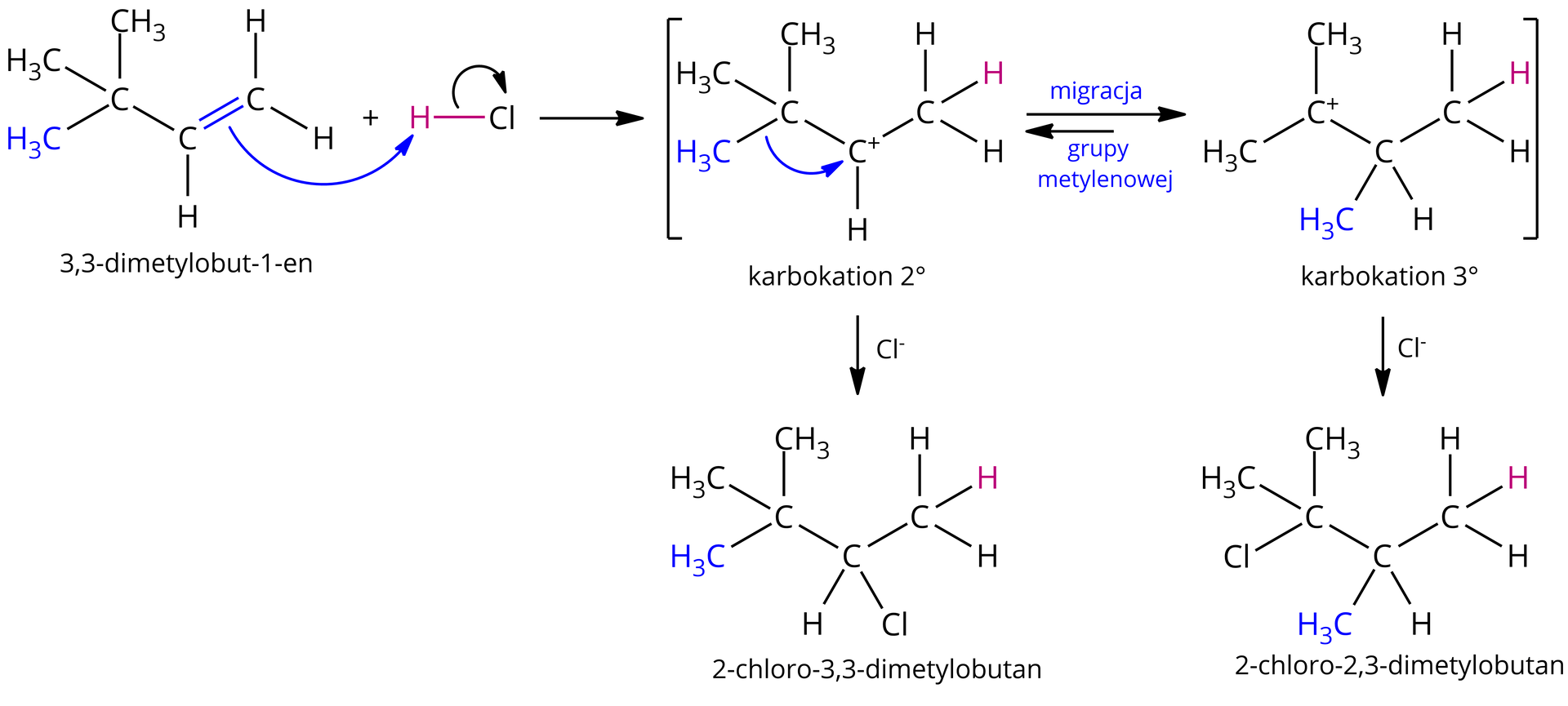
Przykłady przekształceń karbokationów
Słownik
jon zbudowany z protonu i dwóch elektronów, a więc o konfiguracji elektronowej atomu helu
jednowartościowa grupa organiczna wywodząca się z cząsteczki węglowodoru alifatycznego, uboższa od niej o jeden atom wodoru
nierozgałęziony karbokation butylowy
Bibliografia
McMurry J., Chemia organiczna, t. 4, tłum. Henryk Koroniak i in., Warszawa 2018.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 1, tłum. Wiesław Antkowiak i in., Warszawa 1985.