Przeczytaj
Otrzymywanie wodorków w wyniku syntezy bezpośredniej
Tak jak większość wodorkówwodorków, wodorki pierwiastków 17. grupy można otrzymać w reakcji syntezy reakcji syntezy bezpośredniej danego pierwiastka z wodorem.
Spośród fluorowcówfluorowców wyróżnia się fluor, który z wodorem łączy się samorzutnie. Reakcja ta jest gwałtowna, wybuchowa, oraz przebiega bez dostępu światła i w niskiej temperaturze. W jej wyniku powstaje fluorowodór:
Otrzymany fluorowodór – nawet przy śladowych ilościach wody – staje się bardzo aktywny. Jego roztwór wodny, czyli kwas fluorowodorowy, ma właściwości żrące i silnie toksyczne.

Synteza wodorków innych fluorowców przebiega z udziałem światła, płomienia lub katalizatorów.
Reakcja chloru z wodorem wymaga światła lub płomienia:
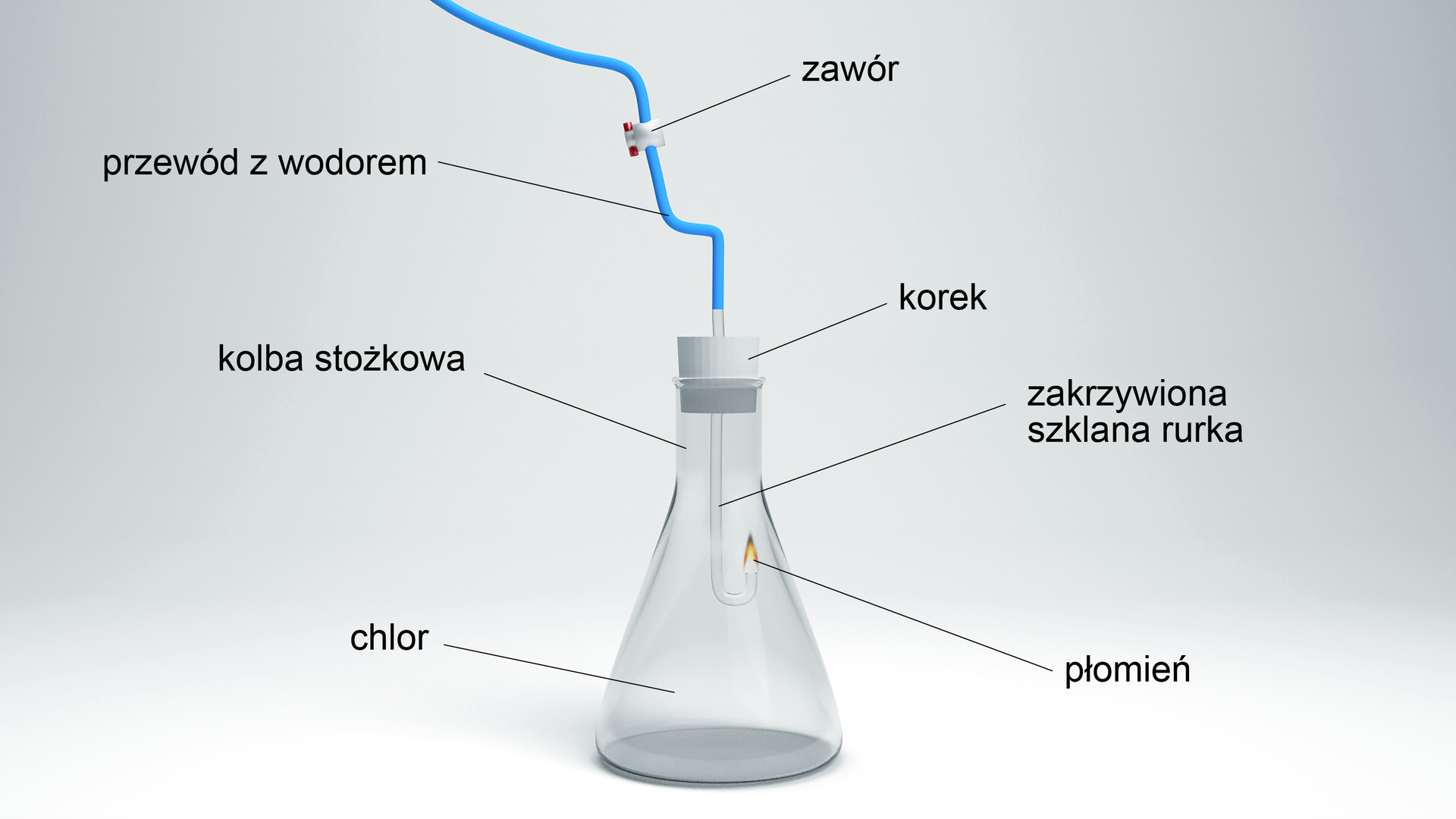
Syntezę chlorowodoru w laboratorium przeprowadza się pod sprawnie działającym wyciągiem. Zarówno chlor, jak i produkt reakcji, a mianowicie chlorowodór, są gazami drażniącymi i toksycznymi.
Brom i jod reagują z wodorem znacznie łagodniej.
Ciekły brom łączy się z wodorem po podgrzaniu lub w obecności katalizatora (np. platyny). W wyniku reakcji powstaje gazowy bromowodór. Jest to reakcja odwracalnareakcja odwracalna, ponieważ bromowodór dość łatwo rozkłada się na pierwiastki.
Podobnie przebiega reakcja syntezy jodwodoru:
Fluorowodór powstaje także w wyniku bezpośredniej reakcji fluoru, który jest najbardziej aktywnym ze wszystkich niemetali – z wodą. Drugim produktem tej reakcji jest atomowy tlen:
Otrzymywanie wodorków pierwiastków 17. grupy z ich soli
Chlorowodór i jego roztwór (kwas chlorowodorowy) są ważnymi surowcami w przemyśle chemicznym i wielu innych, dlatego wytwarzany jest w dużych ilościach. Na skalę przemysłową produkuje się go, działając stężonym kwasem siarkowym(VI) na sól kamienną:
Do otrzymania bromowodoru i jodowodoru nie można stosować metody polegającej na działaniu kwasem siarkowym(VI) na odpowiednie ich sole. Jony i utleniają się pod wpływem stężonego kwasu siarkowego(VI) do bromu i jodu.
Otrzymywanie bromowodoru w reakcji bromku z kwasem siarkowym(VI) jest nieefektywne, ponieważ powstający bromowodór ulega, pod wpływem kwasu, dalszemu utlenianiu do bromu:
Dlatego też do otrzymywania i stosować można kwas fosforowy(V). Na przykład reakcja otrzymywania bromowodoru przebiega zgodnie z równaniem:
Kwas solny (chlorowodorowy) jest ważnym składnikiem soku żołądkowego. Wytwarzany jest w serii reakcji biochemicznych przez komórki okładzinowe gruczołów błony śluzowej żołądka. Podstawową reakcją w powstawaniu kwasu solnego jest synteza jonu wodorowęglanowego z i jonów , pochodzących z dysocjacji wody. Jony wodorowęglanowe są transportowane do osocza krwi, a stamtąd są pobierane i wykorzystywane do produkcji jonów .
Słownik
to związki wodoru z innymi pierwiastkami; ze względu na skład, wodorki możemy podzielić na:
wodorki niemetali – związki, w których wodór występuje na +I stopniu utlenienia;
wodorki metali – związki, w których wodór występuje na -I stopniu utlenienia
synteza, reakcja tworzenia, typ reakcji chemicznej
pierwiastki 17. grupy układu okresowego: fluor (), chlor (), brom (), jod (), astat ()
związki pierwiastków 17. grupy z wodorem: fluorowodór (), chlorowodór , bromowodór , jodowodór
oksydacja, chemiczny proces polegający na oddaniu elektronu (elektronów) przez jon, atom lub grupę atomów, w wyniku czego podwyższa się stopień utlenienia atomu pierwiastka oddającego elektrony
reakcja chem. złożona z elementarnych procesów przebiegających jednocześnie w przeciwnych kierunkach: , w której produkty reakcji przebiegającej z lewa na prawo są substratami reakcji biegnącej w kierunku przeciwnym i odwrotnie
Bibliografia
Atkins P., Jones L., Chemia ogólna, Warszawa 2004, s. 116‑119; 955‑958.
Bielański A., Podstawy chemii nieorganicznej, Warszawa, s. 571 -574.
Czerwiński A, Czerwińska A., Jelińska‑Kazimierczuk M., Kuśmierczyk K., Chemia 1. Podręcznik, Warszawa 2002, s. 243‑345.
Pac B., Zegar A., Podstawy klasyfikacji związków nieorganicznych w teorii i zadaniach, Kraków 2019.