Reakcja strącania
Czym jest reakcja strącenia?
Reakcja strącaniaReakcja strącania, jak sama nazwa wskazuje, polega na strącaniu substancji trudno rozpuszczalnej. Gdy połączymy dwie odpowiednio dobrane, dobrze rozpuszczalne substancje, otrzymamy produkt trudno rozpuszczalny. Zachodzi wówczas reakcja wytrącania osadu oraz wymiany podwójnej, podczas której produkt wytrąca się w postaci osadu. W wyniku tych procesów otrzymany produkt można oddzielić od reszty roztworu i przeprowadzić odpowiednie badania chemiczne.
Zapoznaj się z instrukcją doświadczenia, a następnie zapisz hipotezę i problem badawczy oraz równanie reakcji.
Schemat doświadczenia:
Powstający osad chlorku srebra. Na zdjęciu znajduje się probówka zawierająca przeźroczysty roztwór oraz powstający biały, kłaczkowaty osad chlorku srebra A g C l.
Model sieci krystalicznej A g C l. Ilustracja przedstawiająca model sieci krystalicznej chlorku srebra. Naprzemiennie ułożone atomy srebra symbolizowane przez szare kulki i chloru symbolizowane przez zielone kulki. Cała struktura tworzy kształt przypominający sześcienną kostkę.
W jaki sposób opisuje się reakcje strącenia?
W opisanej w doświadczeniu reakcji nastąpiło wytrącenie chlorku srebra() w postaci białego osadu. Reakcję tę można opisać równaniem chemicznym w formie cząsteczkowej.
Powyższy proces przebiega w środowisku wodnym, a użyte reagenty są solami dobrze rozpuszczalnymi w wodzie, dlatego ulegają dysocjacjidysocjacji elektrolitycznej i występują w roztworze w postaci jonów. Odpowiednie dwa jony, w wyniku połączenia, tworzą trudno rozpuszczalny osad. Uwzględniając w równaniu postać, w jakiej występują sole, opisywane równanie chemiczne można zapisać w następujący sposób:
Zapis jonowy pełny:
W powyższym równaniu chemicznym – zarówno po stronie substratów, jak i produktów – występują takie same jony, a reakcja zachodzi tylko pomiędzy kationem srebra oraz anionem chlorkowym. Skreślając po obu stronach równania identyczne jony, otrzymujemy skrócony zapis jonowy tego równania.
Zapis jonowy skrócony:
Jak teoretycznie można przewidzieć przebieg reakcji strącenia?
Substancje dobrze rozpuszczalne w wodzie dysocjują, czyli występują w roztworze w postaci jonów (dodatnich – kationów – oraz ujemnych – anionów). Po zmieszaniu dwóch roztworów może zajść reakcja, w wyniku której kation jednej substancji utworzy trudno rozpuszczalną sól z anionem drugiej substancji.
W jaki sposób możemy teoretycznie przewidzieć, czy w danej reakcji wytrąci się osad?
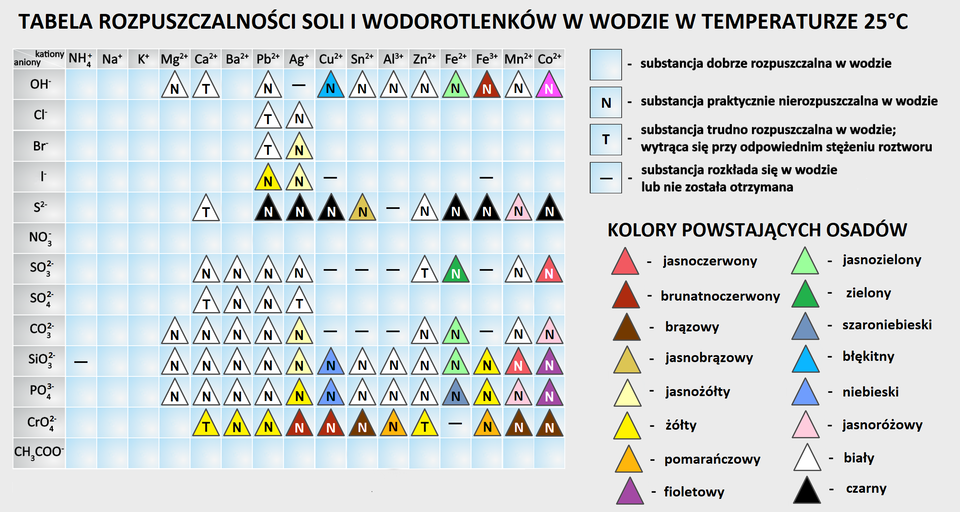
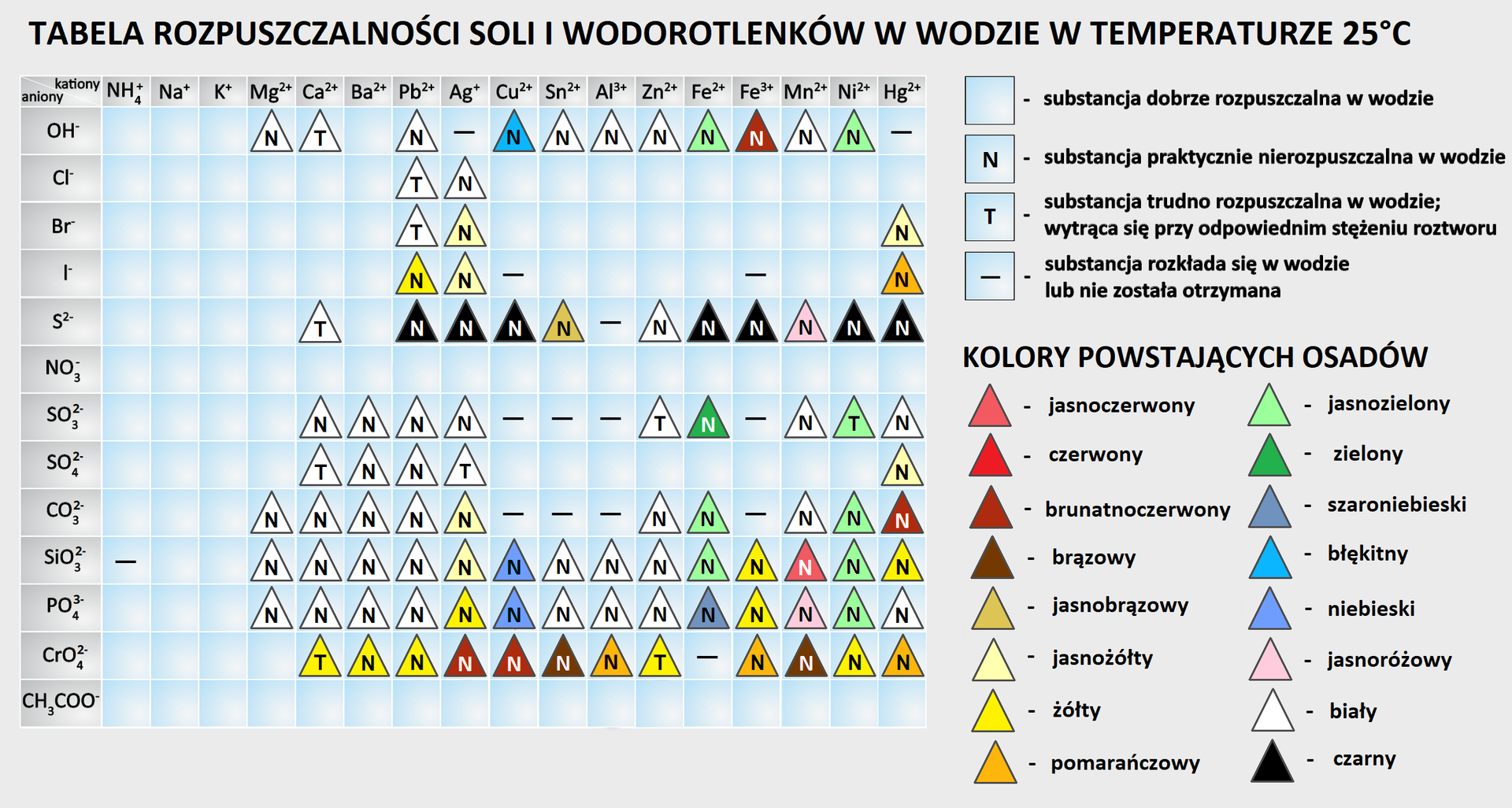
Otóż rozpuszczalnośćrozpuszczalność soli można sprawdzić, posługując się tabelą rozpuszczalności. Jeśli podczas doświadczenia chcemy otrzymać sól trudno rozpuszczalną, korzystamy z tabeli i dobieramy jony, które po zmieszaniu utworzą związek trudno rozpuszczalny. Pamiętajmy, że chcemy otrzymać tylko jeden produkt trudno rozpuszczalny. Trzeba jednak pamiętać, że warunkiem wytrącenia osadu są odpowiednio dobrane stężenia reagentów. Jeżeli stężenia są zbyt małe, osad może się nie wytrącić.
Reakcje strąceniowe są wykorzystywane w analizie jakościowej, w celu potwierdzenia obecności danego jonu w próbce.
Wyobraź sobie, że dostajesz próbkę roztworu do analizy, w którym prawdopodobnie znajduje się sól srebra().
W jaki sposób sprawdzisz obecność jonów srebra w otrzymanej próbce?
Tutaj z pomocą przychodzą reakcje, w wyniku których otrzymasz osad o charakterystycznym wyglądzie. Dobrym przykładem jest powyższa reakcja otrzymywania chlorku srebra(). Następnym jest reakcja otrzymywania jodku srebra() o charakterystycznym wyglądzie. Jodek srebra() otrzymuje się jako żółtawy osad. Jego obecność wskazuje, że w analizowanym roztworze znajdowała się sól srebra.
Czy w wyniku wymieszania niektórych soli, może powstać osad jodku srebra()? Korzystając z tabeli rozpuszczalności, należy wybrać dobrze rozpuszczalne sole, zawierające kation srebra oraz anion jodkowy, np. i .

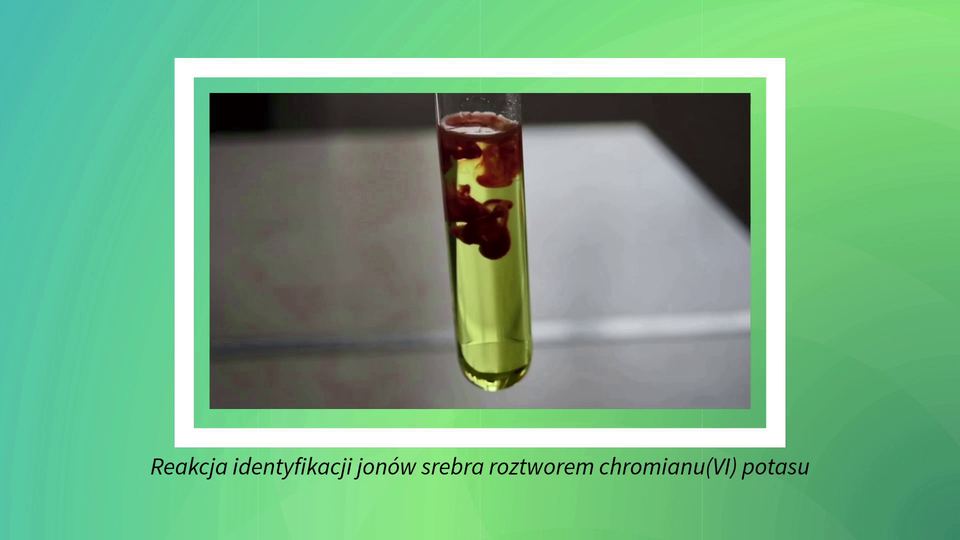
Następnym przykładem barwnej reakcji strącania jest otrzymywanie trudno rozpuszczalnego, żółtego chromianu() ołowiu(). Reakcja przebiega po zmieszaniu roztworu azotanu() ołowiu() i chromianu() potasu.
Zapisz przebieg opisanej reakcji równaniem chemicznym w formie cząsteczkowej, jonowej pełnej i jonowej skróconej.
Czy reakcje strącania można przewidzieć?
Oczywiście, że tak! Aby sprawdzić, czy jony, które znajdą się w roztworze po zmieszaniu dwóch rozpuszczalnych substancji, połączą się ze sobą w związek trudno rozpuszczalny w wodzie, warto posłużyć się tablicą rozpuszczalności. Skorzystanie wyłącznie z niej jednak nie wystarczy. Konieczne jest również zapewnienie odpowiednich stężeń reagentów, by nastąpiło wytrącenie osadu.
Zapoznaj się z poniższym samouczkiem, w którym zostało przedstawione rozwiązanie przykładowego zadania. Zatrzymaj film w odpowiednim momencie i spróbuj wykonać je samodzielnie.
Film dostępny pod adresem /preview/resource/R1TIc3KduNeGA
Film nawiązujący do treści materiału - dotyczy reakcji wytrącenia osadów, sprawdzania rozpuszczalności związków według tabeli, rozwiązywania zadania.
Poszukaj w dostępnych Ci źródłach, jaką barwę mają otrzymane osady:
chromianu() baru ();
metakrzemianu magnezu ().
Zastosowanie reakcji strąceniowej
Czy zastanawiasz się czasami, jak kiedyś artyści pozyskiwali kolory do malowania swoich dzieł? Jakie reakcje były stosowane do otrzymania niektórych farb/związków chemicznych użytych przez artystę? Jakie metale wchodziły w skład tych związków chemicznych? Z pewnością znasz obraz Vincenta van Gogha „Widok na Arles z irysami na pierwszym planie”. Przeanalizuj poniższą grafikę interaktywną na temat substancji nierozpuszczalnych użytych przez artystę do wytworzenia farb o różnych kolorach, które otrzymał poprzez utworzenie mieszaniny pigmentu w odpowiednim medium (wodzie, oleju), zależnym od typu farby. Zwróć szczególną uwagę na nazwy oraz wzory sumaryczne związków chemicznych. Po przeanalizowaniu grafiki, rozwiąż ćwiczenia sprawdzające.
Także i jego stosuje się już od starożytności, a więc nie datuje dzieł sztuki. Największą popularnością cieszył się w średniowiecznym malarstwie książkowym, tablicowym i ściennym. Z czasem minia zaczęła być stopniowo wypierana z użycia ze względu na toksyczne właściwości. Nazwa pigmentu pochodzi od nazwy rzeki Miño płynącej poprzez półwysep Iberyjski, gdzie tlenek ten został po raz pierwszy wydobyty. Można go otrzymać poprzez termiczny rozkład bieli ołowiowej P b nawias O H zamknięcie nawiasu indeks dolny, dwa, koniec indeksu dolnego, razy, dwa P b C O indeks dolny, trzy, koniec indeksu dolnego, gdzie pośrednim produktem przemiany jest masykot – tlenek ołowiu(II), o barwie żółtej. Minia zastosowana w dziełach sztuki jest nietrwała i pod wpływem działania światła/wilgoci ciemnieje. Ciekawostką jest fakt, że wielkim fanem tego pigmentu był Vincent Van Gogh. Minia bywała też stosowana jak czynnik zabezpieczający – np. ołtarz Wita Stwosza w Bazylice Mariackiej w Krakowie został od tyłu pokryty warstwą minii. Ilustracja przedstawia usypaną z pomarańczowo‑czerwonego proszku górkę, na białym tle. 6. Eozyna To czerwony barwnik organiczny, o podanym poniżej wzorze chemicznym: Wzór przedstawia układ trzech pierścieni aromatycznych w dolnym narożu środkowego znajduje się tlen a w górnym wiązanie z kolejnym pierścieniem aromatycznym z grupą minus, C O O indeks górny, minus, koniec indeksu górnego, dwa pozostałe pierścienie są u dołu wiązane z bromem obok z tlenem (pierścień po prawej wiązaniem podwójnym, pierścień po lewej wiązaniem pojedynczym a tlen ma ładunek ujemny), obok kolejne wiązania z bromem. 7. Koszenila Kwas karminowy (koszenila, karmina) to ciemnoczerwony barwnik organiczny o podanym poniżej wzorze chemicznym: Układ 4 pierścieni, (od lewej) pierścień cykloheksanu i trzy połączone benzeny. Pierwszy cykloheksen to cukier z tlenem w strukturze zamiast jednego węgla, od niego odchodzą grupy hydroksylowe i minus, C H indeks dolny, dwa, koniec indeksu dolnego, O H, ten pierścień jest połączony wiązaniem pojedynczym z benzenem, w pierścieniu aromatycznym grupy -OH są rozlokowane tak, że jedna jest po prawej stronie od wiązania z cukrem, a po lewej dwie w kolejnych pozycjach. Następny benzen jest połączony wiązaniem podwójnym z dwoma tlenami u góry i dołu struktury, kolejny benzen u dołu ma wiązanie z grupą metylową, obok grupę karboksylową i w kolejnej pozycji grupę -OH. Występuje naturalnie u owadów (np. czerwców polskich). Z 1 kg suszonych owadów koszenilowych uzyskuje się ok. 50 g karminu. 8. Viridian Viridian to niebiesko‑zielony pigment, uwodniony tlenek chromu(III). Jest bardziej zielony niż niebieski. Ilustracja przedstawia broń leżącą na szarej powierzchni z widocznym włączonym zielonym laserem do namierzania. Tlenek chromu(III) można otrzymać w reakcji uwodnionego siarczanu(VI) chromu(III) z wodnym roztworem amoniaku C r indeks dolny, dwa, koniec indeksu dolnego, nawias S O indeks dolny, cztery, koniec indeksu dolnego, zamknięcie nawiasu indeks dolny, trzy, koniec indeksu dolnego, razy, dwanaście H indeks dolny, dwa, koniec indeksu dolnego, O, plus, sześć N H indeks dolny, trzy, koniec indeksu dolnego, razy, H indeks dolny, dwa, koniec indeksu dolnego, O, strzałka w prawo, C r indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, trzy nawias s zamknięcie nawiasu, koniec indeksu dolnego, plus, trzy nawias N H indeks dolny, cztery, koniec indeksu dolnego, zamknięcie nawiasu indeks dolny, dwa, koniec indeksu dolnego, S O indeks dolny, cztery, koniec indeksu dolnego, plus, piętnaście H indeks dolny, dwa, koniec indeksu dolnego, O 9. Błękit pruski. Charakteryzuje się formułą: F e indeks dolny, cztery, koniec indeksu dolnego, nawias kwadratowy F e nawias C N zamknięcie nawiasu indeks dolny, sześć, koniec indeksu dolnego, zamknięcie nawiasu kwadratowego indeks dolny, trzy, koniec indeksu dolnego, jest to niebieski pigment, otrzymywany sztucznie, a po raz pierwszy przez alchemika i farbiarza Deisbacha w 1704 r. w Berlinie. Jako datę początku jego stosowania przez artystów uznaje się rok 1724. Błękit pruski jest średnio odporny na działania światła i ma niezbyt dobre właściwości kryjące, chociaż odznacza się dużą intensywnością barwienia. Przykład dzieła, w którym można zobaczyć ów pigment to María de los Dolores Collado y Echagüe, duquesa de Bailén Vincenta Palmaroliego. Na ilustracji widnieje szkiełko zegarkowe z nasypanym intensywnie niebieskim proszkiem, na białym tle. Może być otrzymany w reakcji soli żelaza(III) z heksacyjanożelazianem(II) potasu: cztery F e C l indeks dolny, trzy, koniec indeksu dolnego, plus, trzy K indeks dolny, cztery, koniec indeksu dolnego, nawias kwadratowy I I powyżej F e nawias C N zamknięcie nawiasu indeks dolny, sześć, koniec indeksu dolnego, zamknięcie nawiasu kwadratowego, strzałka w prawo, I I I powyżej F e nawias kwadratowy I I I powyżej F e I I powyżej F e nawias C N zamknięcie nawiasu indeks dolny, sześć, koniec indeksu dolnego, zamknięcie nawiasu kwadratowego indeks dolny, trzy, koniec indeksu dolnego, plus, dwanaście K C l 10. Ultramaryna. To pigment naturalny, otrzymywany z minerału lapis lazuli. Jest to złożony związek glinokrzemianu sodowego i siarkowego o zmiennym składzie. Przybliżony wzór można zapisać w formie: N a indeks dolny, osiem, minus, dziesięć, koniec indeksu dolnego, A l indeks dolny, sześć, koniec indeksu dolnego, S i indeks dolny, sześć, koniec indeksu dolnego, O indeks dolny, dwadzieścia cztery, koniec indeksu dolnego, S indeks dolny, dwa, minus, cztery, koniec indeksu dolnego. Najstarsze doniesienia o stosowaniu ultramaryny jako pigmentu wiążą się z malarstwem ściennym. Birsztein zidentyfikował ją w malowidłach ściennych w Kara‑Tape, datowanych na II‑IV w. n.e. Również pojedyncze ziarna ultramaryny wykryto w malowidłach egipskich na płótnie datowanych na IV w. n.e. Ultramaryna naturalna była pigmentem bardzo drogim, którego wartość zbliżona była do wartości złota. Z tego powodu bardzo intensywnie poszukiwano metody jej syntetycznego otrzymywania na przełomie XVIII i XIX w. Poszukiwania te wspierały nawet różne instytucje, które gwarantowały nagrody finansowe dla odkrywców metody syntezy tego pigmentu. Przełom nastąpił około 1830 r., kiedy metody produkcji przedstawili niezależnie od siebie: Jean Baptiste Guimet oraz Christian Gottlob Gmelin. Od tego czasu ultramaryna syntetyczna praktycznie wyparła tę naturalną z użycia. Pigment ten posiada jasnobłękitne kryształy, ale – oprócz ziaren tego koloru – w ultramarynie naturalnego pochodzenia występują zazwyczaj również ziarna kalcytu oraz pirytu. Ilustracja przedstawia usypany w górkę intensywnie niebieski proszek na białym tle. Ultramaryna jest otrzymywana w kilku etapach. Surowce używane do jej produkcji to: biały kaolin nawias A l indeks dolny, dwa, koniec indeksu dolnego, S i indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, dwa, koniec indeksu dolnego, nawias O H zamknięcie nawiasu indeks dolny, cztery, koniec indeksu dolnego, zamknięcie nawiasu; bezwodny siarczan(VI) sodu nawias N a indeks dolny, dwa, koniec indeksu dolnego, S O indeks dolny, cztery, koniec indeksu dolnego, zamknięcie nawiasu; bezwodny węglan sodu nawias N a indeks dolny, dwa, koniec indeksu dolnego, C O indeks dolny, trzy, koniec indeksu dolnego, zamknięcie nawiasu; sproszkowana siarka; sproszkowany węgiel drzewny lub węgiel względnie bezpopiołowy. 11. Błękit kobaltowy Jest to glinian kobaltu(II) – związek opisywany w literaturze wzorami: C o O, razy, A l indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, trzy, koniec indeksu dolnego lub C o A l indeks dolny, dwa, koniec indeksu dolnego, O indeks dolny, cztery, koniec indeksu dolnego. Oficjalnie, otrzymał go po raz pierwszy Józef Leithner w Wiedniu w 1795 r. Natomiast w latach 1802‑1804 chemik Louis Jacque Thenard, profesor Uniwersytetu i Politechniki Paryskiej, opracował metodę otrzymywania tego błękitu oraz zaproponował jego praktyczne zastosowanie jako właśnie pigmentu. Co ciekawe, badania prowadzone w wykopaliskach El Amarna i datowane na 1370 r. p.n.e. wskazują, że partie błękitne obiektów zawierają właśnie glinian kobaltu(II). Przykładem obrazu, w którym znajduje się ten pigment, jest dzieło Wiliama Turnera Ostatnia droga Temeraire’a. Ilustracja przedstawia usypaną z błękitno‑niebieskiego proszku górkę, na szarym tle. Glinian kobaltu(II) można otrzymać w następującej reakcji: dwa C o nawias N O indeks dolny, trzy, koniec indeksu dolnego, zamknięcie nawiasu indeks dolny, dwa, koniec indeksu dolnego, plus, dwa A l indeks dolny, dwa, koniec indeksu dolnego, nawias S O indeks dolny, cztery, koniec indeksu dolnego, zamknięcie nawiasu indeks dolny, trzy, koniec indeksu dolnego, strzałka w prawo, dwa C o nawias A l O indeks dolny, dwa, koniec indeksu dolnego, zamknięcie nawiasu indeks dolny, dwa nawias s zamknięcie nawiasu, koniec indeksu dolnego, plus, cztery N O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, O indeks dolny, dwa nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus, sześć S O indeks dolny, trzy nawias g zamknięcie nawiasu, koniec indeksu dolnego 12. Żółcienie chromianowe To pigmenty zawierające anion chromianowy(VI) C r O indeks dolny, cztery, koniec indeksu dolnego, indeks górny, dwa, minus, koniec indeksu górnego.
Mogą to być: żółcień barytowa B a C r O indeks dolny, cztery, koniec indeksu dolnego; żółcień cynkowa Z n C r O indeks dolny, cztery, koniec indeksu dolnego; żółcień strontowa S r C r O indeks dolny, cztery, koniec indeksu dolnego. W języku angielskim często określane są one wspólną nazwą lemon yellow. Istnieje również tzw. żółcień chromowa, którą stanowi chromian(VI) ołowiu P b C r O indeks dolny, cztery, koniec indeksu dolnego, często spotykany również w postaci P b C r O indeks dolny, cztery, koniec indeksu dolnego, razy, P b nawias O H zamknięcie nawiasu indeks dolny, dwa, koniec indeksu dolnegolub P b C r O indeks dolny, cztery, koniec indeksu dolnego, razy, P b S O indeks dolny, cztery, koniec indeksu dolnego. Wszystkie te pigmenty otrzymuje się najprościej poprzez strącenie osadów z użyciem chromianu(VI) lub dichromianu(VI) potasu. Pojawiły się w użyciu w XIX w. Żółcień chromową stosował wspominany tu już wielokrotnie Van Gogh. Za przykład stanowi obraz Pole pszenicy z cyprysami. Ilustracja przedstawia szalkę Petriego z nasypaną górką żółtego proszku. Chromian ołowiu(II) można otrzymać przez strącanie roztworów chromianów, za pomocą roztworów soli ołowiu: K indeks dolny, dwa, koniec indeksu dolnego, C r O indeks dolny, cztery, koniec indeksu dolnego, plus, P b nawias N O indeks dolny, trzy, koniec indeksu dolnego, zamknięcie nawiasu indeks dolny, dwa, koniec indeksu dolnego, strzałka w prawo, P b C r O indeks dolny, cztery nawias s zamknięcie nawiasu, koniec indeksu dolnego, plus, dwa K N O indeks dolny, trzy, koniec indeksu dolnego
Korzystając z tabeli rozpuszczalności, zaproponuj równanie reakcji otrzymywania żółcieni chromowej w formie cząsteczkowej. Pamiętaj o uwzględnieniu współczynników stechiometrycznych.
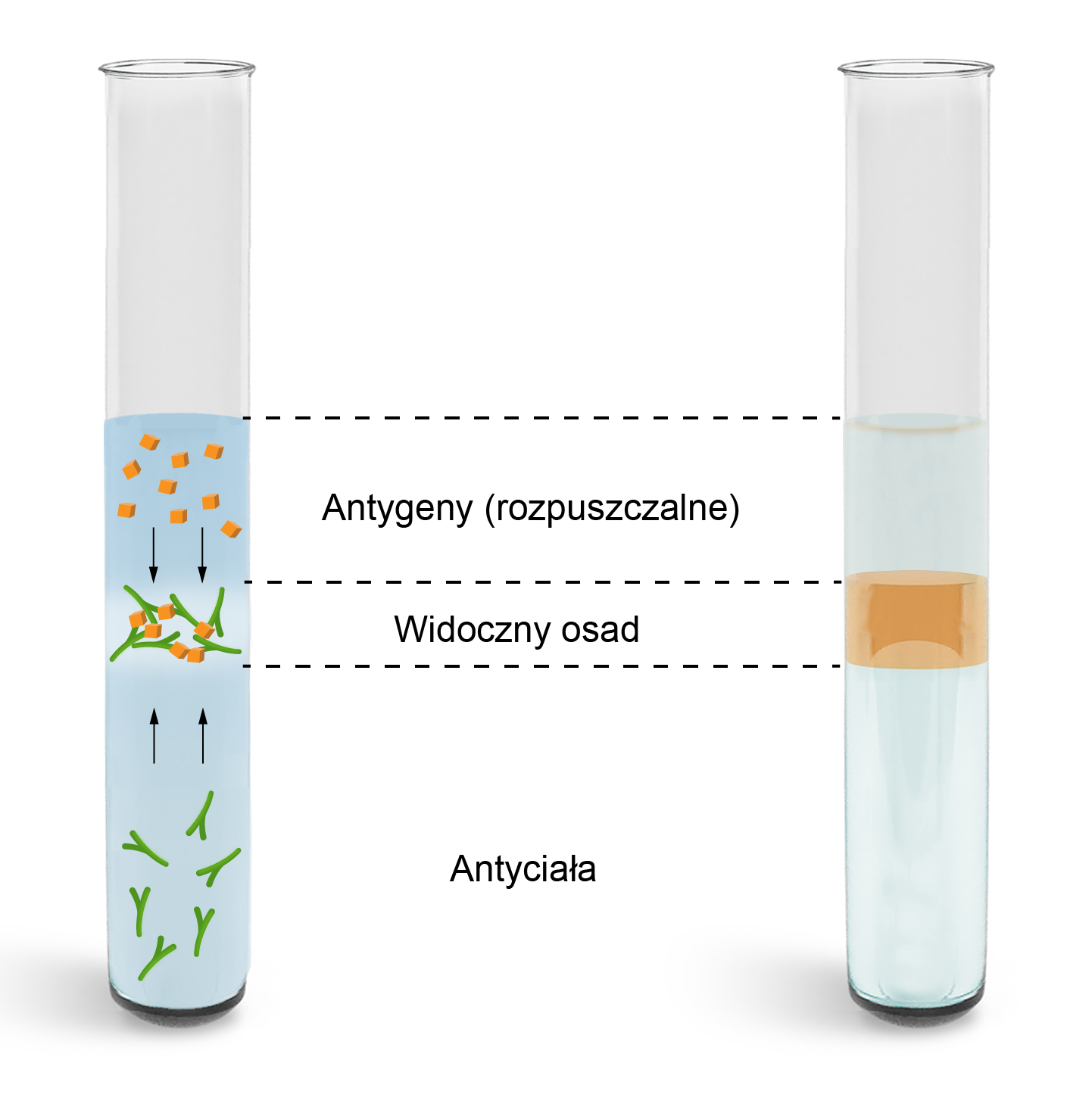
Czy reakcje strąceniowe znalazły zastosowanie w medycynie? Co to jest test Ouchterlony'ego? Jaka jest zasada jego działania? Czy oprócz zalet, istnieją również jego wady? Przeanalizuj poniższą grafikę interaktywną, a następnie odpowiedz na pytania.
Czy reakcje strąceniowe znalazły zastosowanie w medycynie? Co to jest test Ouchterlony'ego? Jaka jest zasada jego działania? Czy oprócz zalet, istnieją również jego wady? Przeanalizuj opis grafiki interaktywnej, a następnie odpowiedz na pytania.
Wyjaśnienie pojęć:
Antygen - preparat chemiczny, która wpływa na odpowiedź immunologiczną organizmu.
Przeciwciała - komórki, które wydziela układ odpornościowy w przypadku kontaktu płynów ustrojowych z antygenami (bakteriami, wirusami) czy z autoantygenami (własnymi tkankami).
Surowica – część osocza krwi, pozbawiona fibrynogenu (białka wytwarzanego w wątrobie) i innych czynników krzepnięcia.
Agar - znany jako E406; preparat żelujący, ekstrahowany z czerwonych alg, takich jak Gracilaria i Gelidium, gdzie głównym składnikiem jest cukier o nazwie galaktoza (trudno przyswajalna przez człowieka).
Żel agarowy - żel powstały przez zmieszanie agaru (dostępnego w handlu w postaci proszku) z wodą.
Wyjaśnij, w jakim celu stosuje się glicerol w próbie obrączkowej, przedstawionej na poniższej fotografii.
Wyjaśnij, w jakim celu stosuje się glicerol w próbie obrączkowej. Zapoznaj się z opisem fotografii.