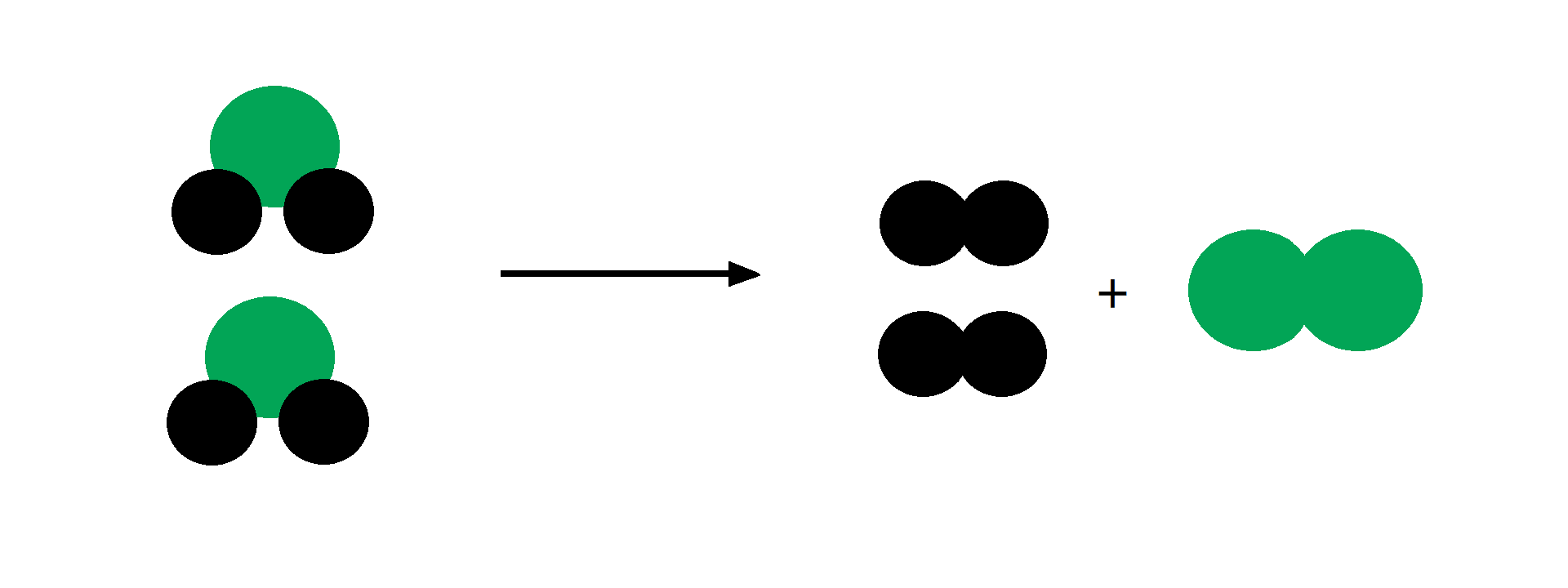Reakcje syntezy i analizy
W przyrodzie stale zachodzi niewyobrażalna liczba przemian chemicznych. Ponadto człowiek sam inicjuje i przeprowadza wiele z nich, aby otrzymać potrzebne mu materiały. Mimo że reakcje chemiczne różnią się między sobą rodzajem substratów i powstających produktów, to jednak wszystkie można podzielić na grupy, które charakteryzują się pewnymi wspólnymi cechami.
symbole pierwiastków chemicznych;
sposoby zapisywania równań reakcji chemicznych;
pojęcie substratów i produktów w reakcji chemicznej.
na czym polegają reakcje syntezy i analizy;
wskazywać przykłady reakcji syntezy i analizy;
zapisywać równania reakcji syntezy i analizy;
dobierać współczynniki w równaniach reakcji chemicznych;
opisywać eksperyment chemiczny, uwzględniając: szkło i sprzęt laboratoryjny, odczynniki chemiczne, obserwacje, weryfikację hipotezy i wnioski.
1. Jakie zasady obowiązują przy zapisywaniu równań reakcji?
Przebieg przemiany chemicznej, z uwzględnieniem substratów i produktów, można opisać słownie, np. węgiel reaguje z tlenem i w wyniku tej reakcji powstaje tlenek węgla.
Zamiast długiego opisu, można posłużyć się równaniem reakcji zawierającym nazwy pierwiastków i związków chemicznych:
Mimo że powyższe sposoby przedstawiania przebiegu reakcji chemicznych są poprawne, to jednak okazują się mało przydatne dla chemików. W swojej pracy stosują oni równania reakcji, w których wykorzystują symbole pierwiastków i wzory związków chemicznych. Dzięki temu chemicy na całym świecie rozumieją się bez słów. Omawianą wcześniej przemianę chemiczną zapisują za pomocą następującego równania reakcji:
Niektóre pierwiastki, takie jak: wodór, azot, tlen, chlor, jod, fluor, brom w stanie wolnym, występują w postaci cząsteczek dwuatomowych. Z tego względu, w równaniach reakcji z ich udziałem, posługujemy się ich wzorami: .
Aby równanie reakcji było poprawnie zapisane, liczby atomów poszczególnych pierwiastków, zapisanych po obu stronach tego równania, muszą być identyczne. W zaprezentowanym powyżej równaniu reakcji () otrzymywania tlenku węgla z węgla i tlenu ten warunek jest spełniony.

Pierwiastek | Liczba atomów po lewej stronie równania | Liczba atomów po prawej stronie równania |
|---|---|---|
węgiel | ||
tlen |
Poniżej przedstawiono słowny zapis równania reakcji, prowadzącej do otrzymania tlenku magnezu.
Przy użyciu symboli i wzorów chemicznych zapisz równanie reakcji magnezu z tlenem, w wyniku której powstaje tlenek magnezu.
Poniżej przedstawiono słowny zapis równania reakcji, prowadzącej do otrzymania tlenku magnezu.
Zaznacz poprawne równanie reakcji magnezu z tlenem, w wyniku której powstaje tlenek magnezu.
Zapis równania reakcji magnezu z tlenem
Liczba atomów każdego z pierwiastków po obu stronach równania jest taka sama. Równanie reakcji jest zapisane prawidłowo. Mówi się, że jest ono uzgodnione lub zbilansowane. Czynności, które wykonywaliśmy od momentu napisania równania reakcji przy użyciu symboli i wzorów, do uzyskania jego prawidłowego zapisu, nazywa się uzgadnianiem (lub bilansowaniem) równania reakcji.
W jaki sposób uzgodnić równanie reakcji otrzymywania wody z wodoru i tlenu? Zapoznaj się z poniższym filmem, a następnie rozwiąż ćwiczenie.
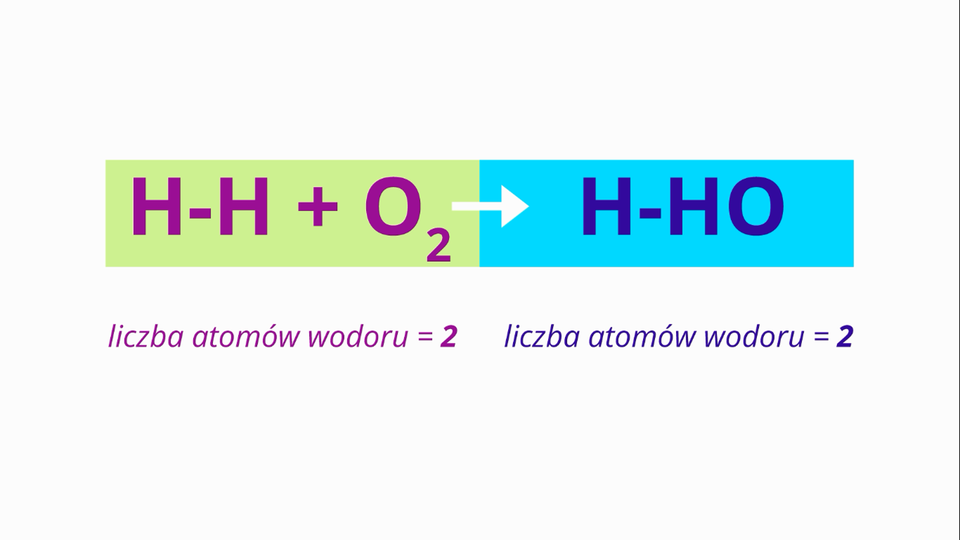
Film dostępny pod adresem /preview/resource/R2LHSRPgd5atn
Na filmie ukazano, w jaki sposób poprawnie uzgodnić równanie reakcji na przykładzie reakcji wodoru z tlenem.
Już w chemicy zapisywali równania reakcji chemicznych. Ta notacja znacznie różniła się od współczesnej. Na przykład reakcję metalu (żelaza) z kwasem azotowym – współczesna nazwa: kwas azotowy – opisywano następująco:
2. Jak nazywamy reakcję, w wyniku której substancje łączą się ze sobą, tworząc jeden związek chemiczny?
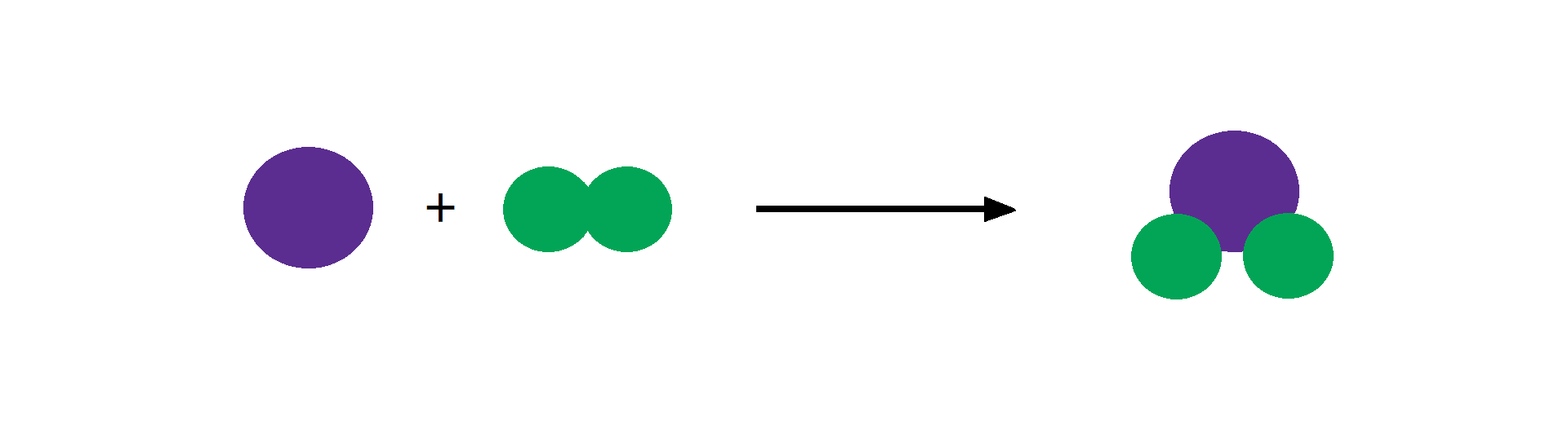
Przyjrzyj się poniższym równaniom reakcji:
Zauważ, że w wyniku tych przemian z dwóch substratów otrzymuje się jeden produkt. Można je opisać poniższym równaniem:
O takich przemianach mówi się, że są to reakcje syntezyreakcje syntezy lub inaczej reakcje łączeniareakcje łączenia.
W poniższej galerii przedstawiono przykłady reakcji syntezy.
Przeprowadź doświadczenie chemiczne polegające na sprawdzeniu, czy jod reaguje z magnezem.
Uwaga!
Doświadczenie należy wykonać pod wyciągiem.
Przeprowadzono doświadczenie chemiczne polegające na sprawdzeniu, czy jod reaguje z magnezem. Zapoznaj się z poniższym opisem doświadczenia, a następnie wykonaj polecenie.
Problem badawczy:
Czy jod reaguje z magnezem? Czy jest to reakcja syntezy?
Hipoteza:
Jod reaguje z magnezem. Jest to reakcja syntezy, czyli łączenia.
Co było potrzebne:
magnez w postaci wiórów;
jod krystaliczny;
woda;
parowniczka porcelanowa;
dwie łyżeczki;
pipeta Pasteura.
Przebieg doświadczenia:
W parowniczce umieszczono niewielką ilość wiórków magnezowych oraz kilka kryształków rozdrobnionego jodu. Do mieszaniny jodu z magnezem dodano kilka kropli wody.
Obserwacje:
Po dodaniu wody reakcja przebiega gwałtownie. Wydzielają się pary o fioletowej barwie.
Wnioski:
W wyniku reakcji magnezu z jodem powstaje jodek magnezu, zgodnie z poniższym równaniem reakcji:
Woda pełni rolę katalizatora tej reakcji, czyli znacznie przyspiesza jej przebieg.
Reakcja ta przebiega z wydzieleniem ciepła. Jest ono wystarczające do tego, aby jod, znajdujący się w mieszaninie reakcyjnej, częściowo uległ sublimacji (fioletowy gaz). Reakcja otrzymywania jodku magnezu z magnezu i jodu jest reakcją syntezy.
Przeanalizuj poniższe przykłady równań reakcji syntezy. Zwróć uwagę na to, że liczby atomów poszczególnych pierwiastków, zapisanych po obu stronach równania reakcji, są takie same.
Lp. | Zapis słowny | Zapis z użyciem symboli i wzorów |
Synteza jądrowa
Podczas omawianej reakcji syntezy z dwóch lub większej liczby substratów powstaje jeden produkt. Jądra atomów pierwiastków, które tworzą substraty, a następnie – produkt, nie ulegają zmianie.
Istnieje jednak typ reakcji nazywany syntezą jądrową. Przemiana ta polega na łączeniu się jąder lekkich pierwiastków w jądra cięższych pierwiastków. Taka przemiana zachodzi na przykład na Słońcu. Podczas niej z dwóch jąder atomów wodoru powstaje jądro atomu helu i wydziela się ogromna ilość energii. Reakcję syntezy helu opisuje równanie uwzględniające budowę jąder poszczególnych reagentów:

3. Jak nazywamy reakcję chemiczną, w wyniku której z jednej substancji powstaje kilka produktów?
W odpowiednich warunkach woda ulega reakcji, w wyniku której powstają pierwiastki, z jakich się składa. Przebieg tej reakcji opisuje równanie:
Zauważmy, że w omawianej reakcji z jednej substancji (wody) powstają dwie inne (tlen i wodór).
Przemiana chemiczna, podczas której z jednego substratu powstają co najmniej dwa produkty, nazywana jest reakcją rozkładureakcją rozkładu lub reakcją analizyreakcją analizy. Można ją opisać za pomocą schematu:
Omówiona przemiana wody w wodór i tlen należy do tego typu reakcji.
Obejrzyj film, a następnie zaznacz produkty rozkładu tlenku rtęci.

Film dostępny pod adresem /preview/resource/Rih29SnQGcBoL
Na filmie ukazano reakcję analizy na przykładzie reakcji rozkładu tlenku rtęci dwa, w wyniku której powstała rtęć oraz tlen.
Tlenek rtęci ulega reakcji rozkładu zgodnie z poniższym równaniem reakcji:
Reakcje analizy zachodzą w naszym otoczeniu. Są one również wykorzystywane w przemyśle do otrzymywania użytecznych pierwiastków i związków chemicznych.

(), dlatego, jako środek apteczny, ma określony termin użycia

Proces otrzymywania tlenku wapnia w wyniku rozkładu węglanu wapnia przebiega w wysokiej temperaturze. Można go opisać następującymi równaniami reakcji:
W równaniach reakcji chemicznych często zaznacza się warunki, w jakich reakcje te przebiegają. Jeśli reakcja wymaga ogrzewania, to nad strzałką zapisujemy słowo „temperatura” lub symbol „T”. Czasami również podajemy konkretną wartość temperatury, potrzebną do zajścia reakcji chemicznej.

* Z uwagi na to, że wartościowość glinu we wszystkich związkach chemicznych jest równa trzy, w nazwach tych związków nie podaje się jego wartościowości.
Zapis słowny | Zapis z użyciem symboli i wzorów |
|---|---|
Zastanów się i odpowiedz, czy poniższe równanie:
przedstawia reakcję rozkładu. Odpowiedź uzasadnij.
Podsumowanie
Równania reakcji chemicznych zapisuje się przy użyciu symboli i wzorów chemicznych. Liczby atomów poszczególnych pierwiastków chemicznych po obu stronach równania muszą być identyczne.
Uzupełnianie równania reakcji o współczynniki stechiometryczne nazywa się uzgadnianiem (bilansowaniem) równania reakcji chemicznej.
Reakcja syntezy (łączenia) to rodzaj reakcji chemicznej, w wyniku której z dwóch lub większej liczby substratów powstaje tylko jeden produkt.
Reakcja analizy (rozkładu) to rodzaj reakcji chemicznej, w wyniku której z jednego substratu powstają co najmniej dwa produkty.
Korzystając z dostępnych materiałów, przedstaw za pomocą modeli równanie dowolnej reakcji syntezy i analizy.
Słownik
przemiana chemiczna polegająca na łączeniu się dwóch lub większej liczby substratów w jeden produkt
przemiana chemiczna polegająca na rozkładzie jednego substratu (związku chemicznego) na co najmniej dwa produkty (pierwiastki bądź związki chemiczne)
Ćwiczenia
Uzupełnij luki w tekście. Wybierz właściwe określenia spośród podanych.
Reakcja syntezy, współczynniki stechiometryczne, powstają więcej niż trzy produkty, liczby uzgodnione, Reakcja analizy, powstaje jeden produkt, powstają co najmniej dwa produkty, reakcja analizy, indeksy stechiometryczne, przemiana fizyczna, reakcja syntezy, liczby zbilansowane, reakcja rozkładu, powstają co najwyżej dwa produkty
Reakcje, w których z dwóch lub więcej substratów powstaje tylko jeden produkt, to ......................................................................... ........................................................................ to przemiana chemiczna, w której z jednego substratu ......................................................................... Liczby umieszczane przed symbolami i wzorami substancji w równaniach reakcji chemicznej w celu ich zbilansowania to .........................................................................
Wskaż prawidłowo zbilansowane równanie następującej reakcji chemicznej:
.
Wskaż prawidłowo zbilansowane równanie reakcji otrzymywania tlenku siarki(VI) z tlenku siarki(IV) i tlenu.
Wskaż prawidłowo zapisane i zbilansowane równanie reakcji rozkładu tlenku ołowiu(IV) do tlenku ołowiu(II) i tlenu.
Oceń, czy podane zdania są prawdziwe, czy fałszywe.
| Prawda | Fałsz | |
| Reakcje metali z tlenem, w wyniku których otrzymuje się tlenki tych metali, są reakcjami analizy. | □ | □ |
| Reakcja rozkładu związku chemicznego to reakcja analizy. | □ | □ |
| Przemiana zachodząca podczas prażenia węglanu wapnia to reakcja syntezy. | □ | □ |
| W reakcji syntezy uczestniczą co najmniej dwa substraty, a otrzymuje się w jej wyniku jeden produkt. | □ | □ |
| W reakcji analizy uczestniczy jeden substrat, z którego powstają co najmniej dwa produkty. | □ | □ |
W szkolnym laboratorium uczniowie przeprowadzili następujące doświadczenie chemiczne.
Na łyżce do spalań uczniowie umieścili niewielką ilość siarki. Następnie ogrzewali zawartość łyżki nad płomieniem palnika. Siarka początkowo zaczęła się topić, a następnie spalać niebieskim płomieniem.
Reakcja, którą przeprowadzili uczniowie, należy do: Możliwe odpowiedzi: 1. reakcji analizy, czyli rozkładu., 2. reakcji syntezy, czyli łączenia.
Bibliografia
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy siódmej szkoły podstawowej, Warszawa 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy siódmej szkoły podstawowej, Kielce 2020.