Słownik
Słownik
pierwiastek chemiczny lub związek chemiczny powstały w przyrodzie w wyniku naturalnych procesów geologicznych lub kosmologicznych, o określonym składzie chemicznym i właściwościach chemicznych i fizycznych oraz strukturze krystalicznej
(łac. passivus „bierny”) pasywowanie, proces chemiczny lub elektrochemiczny powodujący zwiększenie odporności korozyjnej metalu w wyniku wytworzenia na jego powierzchni bardzo cienkiej, szczelnej i dobrze związanej z podłożem warstewki tlenków lub soli
mieszanina substancji, składająca się z dwóch lub więcej pierwiastków chemicznych, z których jeden występuje w przeważającej ilości i jest metalem
metoda polegająca na pokrywaniu przedmiotów warstwą metalu w wyniku elektrolizy, w celu ozdobienia lub ochrony przedmiotu, np. przed korozją
sole kwasu chromowego() zawierają anion
sole kwasu dichromowego() zawierają anion
w ujęciu kinetycznym – stan, do którego dąży układ w miarę przebiegu reakcji odwracalnej
to reakcja chemiczna, polegająca na łączeniu się substratów w większy od nich produkt
pokrywanie powierzchni metalu cienką warstwą związku (tlenkiem), zapobiegając tym samym dalszemu utlenianiu
nakładanie na powierzchnię przedmiotów metalowych (najczęściej stalowych) warstwy chromu — ochronno‑dekoracyjnej lub techn. (np. w celu zwiększenia odporności na ścieranie pierścieni tłokowych, regeneracji zużytych części, zwiększenia żaroodporności)
żółcień królewska; chromian(VI) ołowiu(II), PbCrOIndeks dolny 44; żółty pigment nieorganiczny
odmiana minerału, która pod względem wyglądu zewnętrzengo oraz sposobu wykształcenia przypomina ziemię; w kolorze podobnym do ziemi, szary z odcieniem brunatnym
mieszanina substancji, składająca się z dwóch lub więcej pierwiastków chemicznych, z których jeden występuje w przeważającej ilości i jest metalem
termin przyjęty umownie na określenie pierwiastków metalicznych, których gęstość jest większa niż 4,5 , np. srebro, iryd.
związek lub pierwiastek chemiczny, powstały wskutek procesów geologicznych
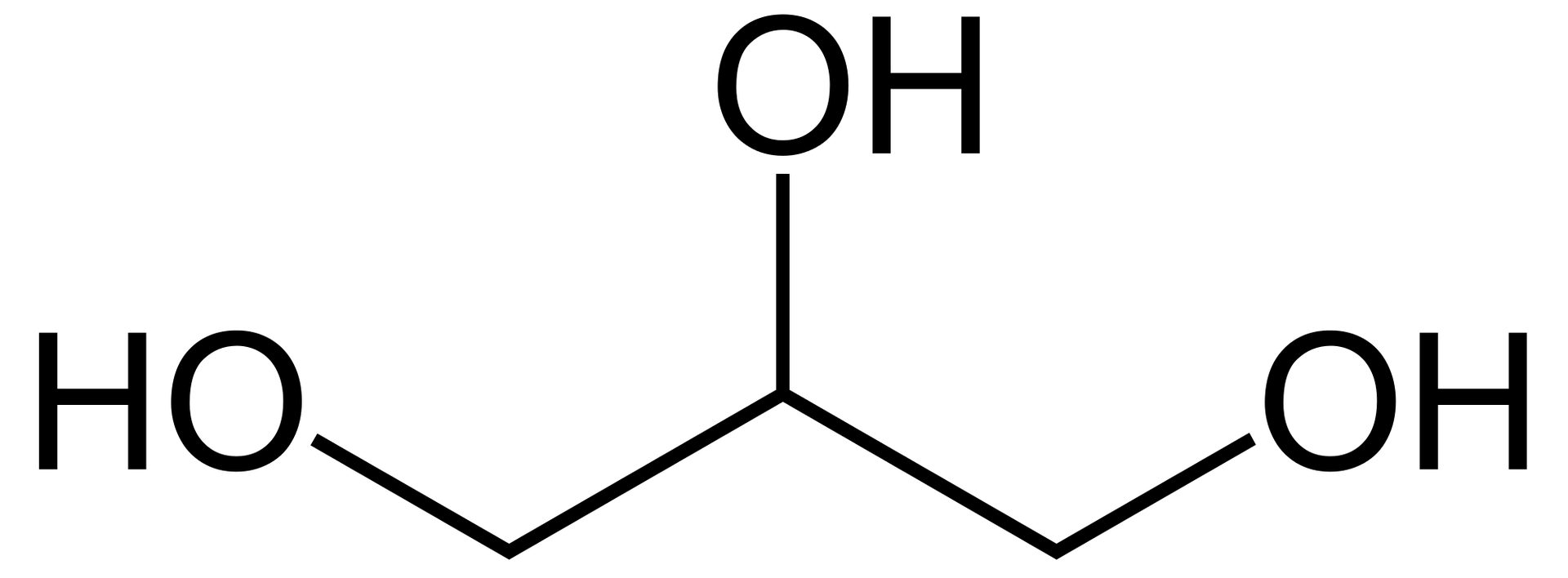
(gr. glykerós „słodki”) glicerol, propano-,,-triol, związek organiczny, najprostszy alkohol trihydroksylowy
(łac. ferrum „żelazo”) symbol Fe jest to pierwiastek chemiczny, należący do metali przejściowych. Jego masa atomowa wynosi 26. W układzie okresowym pierwiastków chemicznych leży w VIII grupie i w 4 okresie
jest to temperatura, powyżej której substancja będąca ferromagnetykiem traci swoje właściwości magnetyczne i staje się paramagnetykiem. Ma to związek ze zmianą fazy danego ciała stałego. Nazwa ta została nadana na cześć francuskiego fizyka Pierre'a Curie (męża Marii Skłodowskiej-Curie)
jest to pojęcie matematyczne, które oznacza powtarzające się w przestrzeni upakowanie drobin
(łac. ferrum „żelazo”, magneticus „magnetyczny”) ciało, które posiada własności ferromagnetyczne, czyli wykazuje spontaniczne namagnesowanie. Takie ciało jest kryształem, który posiada obszary stałego namagnesowania, zwane domenami magnetycznymi; ułożone są one w sposób chaotyczny
jest to proces termodynamiczny polegający na przejściu substancji z jednej fazy w inną, np. parowanie, krystalizacja, przemiana alotropowa
jest to skala twardości minerałów
ilość energii, jaką należy dostarczyć do jednostki masy danej substancji, aby zmienić jej stan skupienia w gazowy w stałej temperaturze i ciśnieniu
ilość energii potrzebnej do jednostki masy danej substancji stałej, aby zmienić jej stan skupienia w ciekły przy stałym ciśnieniu
ciśnienie, przy którym w określonej temperaturze gaz jest w stanie równowagi z cieczą
ciepło potrzebne do zmiany temperatury ciała w jednostkowej masie o jedną jednostkę
przewodność elektryczna właściwa, przewodnictwo elektryczne właściwe – wielkość fizyczna charakteryzująca przewodnictwo elektryczne przewodnika jednorodnego o oporze właściwym 1 oma na metr
(gr. piupsilonrhoomicronphiόrhoomicronς od piῦrho „ogień” i phiomicronrhoός „niosący”) właściwość powodująca samozapłon w kontakcie z tlenem z powietrza
w wyniku ich działania może dochodzić do utlenienia metalu i jednoczesnej redukcji nie tylko wodoru, ale również atomu centralnego reszty kwasowej
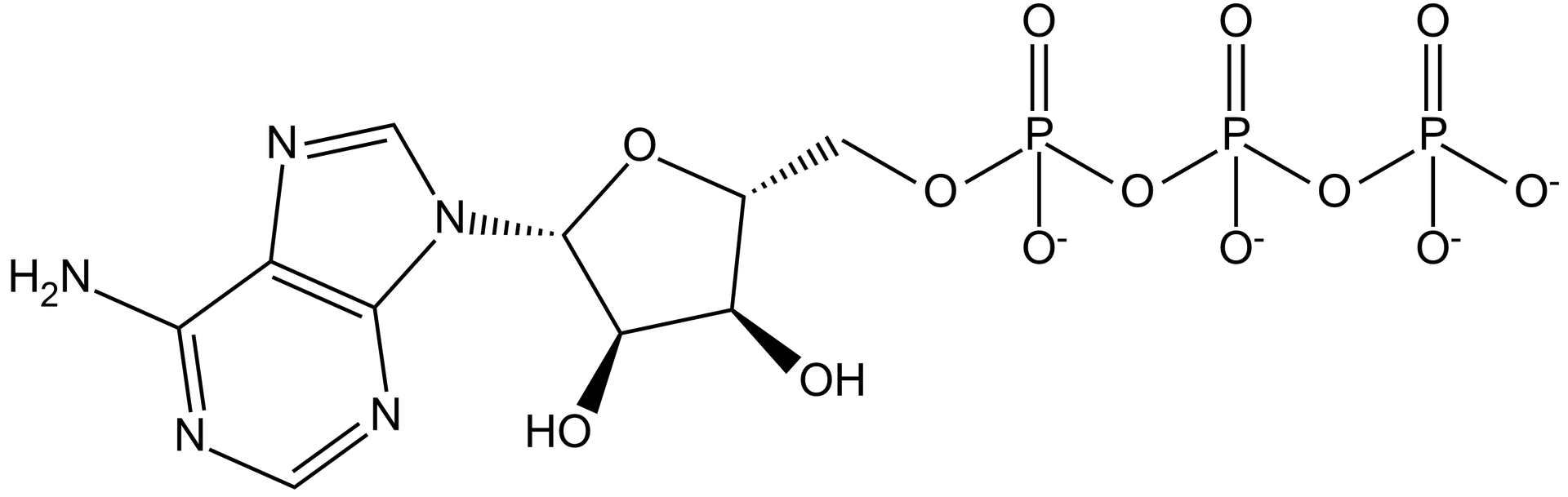
nukleotyd adeninowy, zbudowany z adenozyny z przyłączoną wiązaniem estrowym w pozycji 5′-OH grupą trifosforanową; stanowi nośnik energii chemicznej, używanej w metabolizmie komórki; powstaje jako magazyn energii w procesach fotosyntezy i oddychania komórkowego
białko złożone z grupy metaloproteidów, występujące w mięśniach poprzecznie prążkowanych; posiada zdolność nietrwałego wiązania tlenu i stanowi jego magazyn w tkance mięśniowej poprzecznie prążkowanej
białko z grupy metaloproteidów, pełniące rolę czerwonego barwnika oddechowego; należy do białek złożonych zawierający żelazo ; wiąże się nietrwale z tlenem; występuje u kręgowców w postaci zamkniętej w komórkach krwi – erytrocytach lub w postaci rozpuszczonej w osoczu u niektórych bezkręgowców
potencjał elektrody znajdującej się w stanie standardowym
formalna wartość ładunku atomu w związku chemicznym przy założeniu, że wszystkie wiązania chemiczne w danej cząsteczce mają charakter wiązań jonowych
kwas, który może powodować utlenienie innego indywiduum chemicznego jednocześnie, redukując nie tylko jon , ale również resztę kwasową
produkt korozji atmosferycznej miedzi bądź jej stopów
gazowy składnik atmosfery biorący udział w efekcie cieplarnianym; powodują podwyższenie temperatury na Ziemi poprzez zatrzymywanie promieniowania elektromagnetycznego
cząstka materii o wielkości do ()
(łac. patina „naczynie” – dawniej naczynia wykonywane były z miedzi lub brązu); grynszpan szlachetny, śniedź; cienka (50‑80 µm) warstewka, najczęściej o niebieskozielonej barwie, która pokrywa powierzchnię wyrobów z miedzi i jej stopów oraz chroni głębsze warstwy metalu przed korozją
(łac. corrosio „zżeranie”) proces niszczenia (degradacji) materiałów, w wyniku reakcji chemicznych lub elektrochemicznych, które przebiegają na granicy zetknięcia z otaczającym je środowiskiem
dodatni potencjał elektrodowy (oznaczany jako ) posiadają metale szlachetne , które wykazują słabe właściwości redukujące (trudno je utlenić), przy czym jony tych metali wykazują silne właściwości utleniające (łatwo je zredukować)
Szereg elektrochemiczny metali:
Elektroda | E° [V] |
|---|---|
-3,04 | |
-2,86 | |
-2,36 | |
-1,69 | |
-1,18 | |
-0,76 | |
-0,74 | |
-0,44 | |
-0,40 | |
-0,28 | |
-0,26 | |
-0,14 | |
-0,14 | |
-0,04 | |
0,00 | |
+0,32 | |
+0,34 | |
+0,80 | |
+0,85 | |
+1,52 |
Indeks górny Witowski D., Zbiór zadań 2002‑2012. Liceum i Technikum, Warszawa 2012. Indeks górny koniecWitowski D., Zbiór zadań 2002‑2012. Liceum i Technikum, Warszawa 2012.
reakcja charakterystyczna stosowana w celu jakościowego oznaczania aldehydów; polega ona na reakcji redoks wodorotlenku miedzi() z aldehydami, w wyniku której aldehydy ulegają utlenieniu do kwasów karboksylowych (a właściwie ich soli), a jony miedzi() redukują się do miedzi() – powstaje ceglastoczerwony osad tlenku miedzi()
reakcja charakterystyczna stosowana w celu jakościowego oznaczania aldehydów; polega ona na reakcji redoks jonów miedzi() do miedzi() – tlenek miedzi() jest ceglastoczerwonym osadem; stosowanym odczynnikiem są kompleksy winianowe miedzi(); zastosowany kompleks miedzi() jest bardziej reaktywny i lepiej rozpuszczalny w porównaniu do wodorotlenku miedzi(), stosowanego w próbie Trommera
środek grzybobójczy do ochrony zbóż, kwiatów, drzew owocowych
proces usuwania związków tiolowych z ropy naftowej i jej pochodnych poprzez ich utlenienie do disiarczków o mniejszej szkodliwości i większej lepkości, co sprzyja usuwaniu związków siarki z lekkich frakcji ropy naftowej i ich akumulacji w cięższych frakcjach ropy naftowej; do procesu słodzenia wykorzystuje się chlorek miedzi()