Sprawdź się
Na wykresie przedstawiono wartości promieni atomowych litowców (bez fransu).
Zapoznaj się z opisem wykresu i wykonaj zadanie.

Litowce zaliczamy do najbardziej aktywnych metali. Atomy litowców mają małe wartości energii jonizacji, czyli łatwo oddają elektron walencyjny.
a) Zapisz równanie tworzenia kationu litowca. Atom litowca oznacz symbolem Me.
b) Napisz konfigurację elektronową kationu sodu.
Czy w rzeczywistości możliwa jest do zrealizowania reakcja, której równanie przedstawiono poniżej? Odpowiedz na pytanie i podaj krótkie uzasadnienie.
Dlaczego sód i potas powinny być przechowywane w oleju parafinowym lub w nafcie? Napisz wyjaśnienie.
Na podstawie tabeli elektroujemności, określ typ wiązania w tlenkach berylowców i .
Rysunek przedstawia sposób przeprowadzenia reakcji sodu z wodą. Odpowiedz na poniższe pytania.
Zapoznaj się z opisem rysunku przedstawiającego sposób przeprowadzenia reakcji sodu z wodą. Odpowiedz na poniższe pytania.
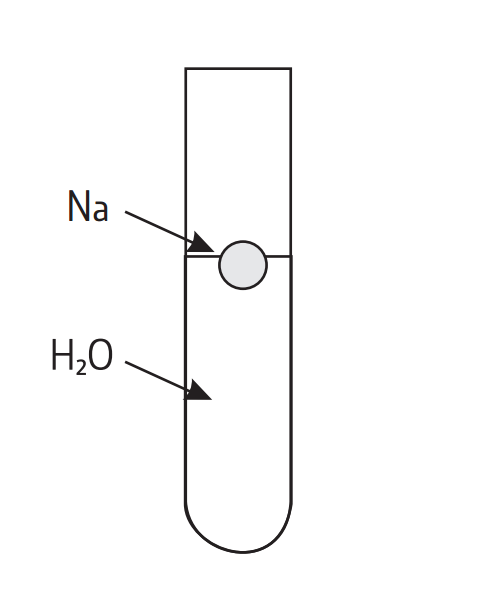
a) Na podstawie rysunku określ, czy gęstość sodu jest większa od gęstości wody.
b) Jaki gaz wydziela się w czasie tej reakcji?
c) Po reakcji dodano do roztworu kroplę fenoloftaleiny. Jak zabarwi się roztwór?
d) Jaki odczyn ma roztwór po reakcji?
e) Napisz odpowiednie równanie jonowe reakcji zachodzącej w probówce.
Który pierwiastek, , , czy , reaguje najbardziej gwałtownie z wodą? Odpowiedź uzasadnij.