Sprawdź się
Pokaż ćwiczenia:
Ćwiczenie 1
Zaznacz poprawną odpowiedź.
Ćwiczenie 2
Ćwiczenie 3
Zaznacz poprawną odpowiedź.
Ćwiczenie 4
Zaznacz poprawną odpowiedź.
Ćwiczenie 5
Informacja do zadania
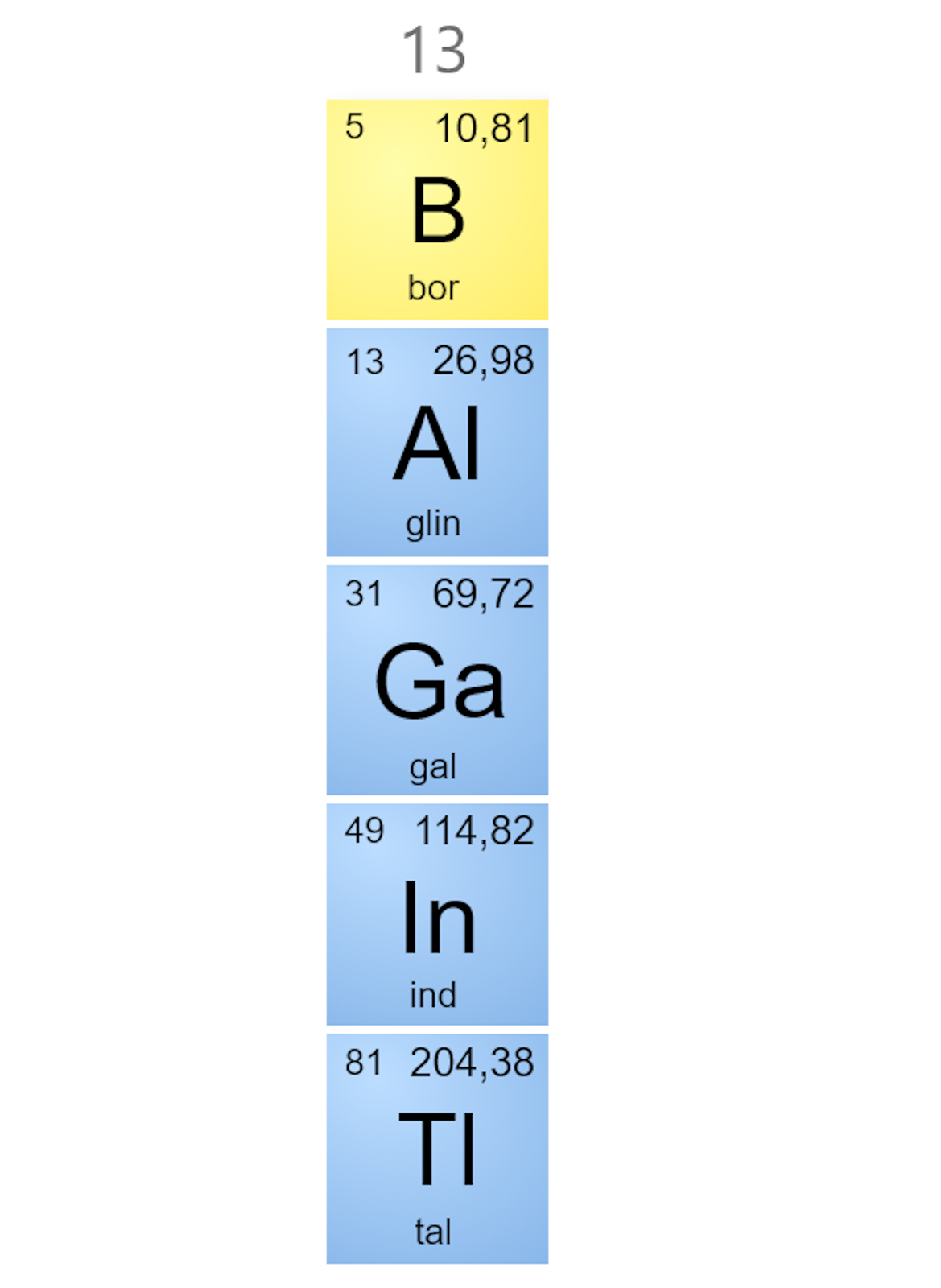
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Ćwiczenie 6
Uszereguj poniższe pierwiastki zgodnie ze wzrastającą elektroujemnością:
Ćwiczenie 7
Odpowiedz na pytanie.
Odpowiedź:
Ćwiczenie 8
Informacja do zadania
numer grupy/numer okresu | ||||||||
|---|---|---|---|---|---|---|---|---|
Korzystając tylko z powyższego fragmentu układu okresowego, odpowiedz na pytania (Uwaga: pogrubione litery nie są symbolami pierwiastków)