Tlenki - właściwości chemiczne tlenków
Właściwości tlenków w głównej mierze zależą od położenia pierwiastka tworzącego dany tlenek w układzie okresowym. Ogólnie można wywnioskować, że tlenki niemetali są w dużej mierze tlenkami wykazującymi charakter kwasowy, natomiast tlenki metali wykazują zazwyczaj charakter zasadowy. Mimo to tej tendencji nie powinno się traktować w sposób bezwzględny.
Badanie charakteru chemicznego wybranych tlenków1
Czy wiesz, w jaki sposób zbadać charakter chemiczny następujących tlenków: , , ? Zapoznaj się z poniższym laboratorium i zbadaj charakter chemiczny tych związków chemicznych. Następnie uzupełnij dzienniczek, wpisując do niego sprzęt laboratoryjny oraz odczynniki chemiczne, z których korzystałeś, a także instrukcję wykonywanego eksperymentu. Na koniec rozwiąż ćwiczenia sprawdzające.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DEO7C16VZ
Analiza doświadczenia: Badanie charakteru chemicznego tlenków.
Problem badawczy: Jaki charakter chemiczny posiadają tlenki: magnezu, glinu oraz fosforu()?
Hipoteza: Tlenek magnezu ma charakter zasadowy, tlenek glinu ma charakter amfoteryczny, a tlenek fosforu() ma charakter kwasowy.
Odczynniki: wodny roztwór wodorotlenku sodu o stężeniu ; kwas chlorowodorowy o stężeniu ; , , ; roztwór oranżu metylowego; alkoholowy roztwór fenoloftaleiny.
Sprzęt laboratoryjny: probówek – podłużnych naczyń szklanych do przeprowadzania prostych reakcji chemicznych; łyżki laboratoryjne – długie trzonki wykonane ze szkła, porcelany lub metalu zakończone z jednej strony łyżeczką. Służą do nabierania sypkich substancji chemicznych; statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki; szklanych bagietek – sprzętów laboratoryjnych, o kształcie prostego pręta szklanego, czasami zakończonego z jednej strony małą rączką, a z drugiej małą łopatką; pipety Pasteura – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Instrukcja wykonania doświadczenia:
1. Do trzech probówek wlano po kwasu chlorowodorowego, a następnie dodano kilka kropli roztworu oranżu metylowego
2. Do każdej z trzech probówek dodano kolejno niewielką ilość (pół łyżeczki) tlenków: , ,.
3. Zawartość probówek zamieszano.
4. Do kolejnych trzech probówek wlano po wodnego roztworu wodorotlenku sodu, a następnie dodano kilka kropli alkoholowego roztworu fenoloftaleiny.
5. Do każdej z trzech probówek dodano kolejno niewielką ilość (pół łyżeczki) tlenków: , , .
6. Zawartość probówek zamieszano.
Obserwacje:
Po dodaniu roztworu oranżu metylowego do probówek z kwasem chlorowodorowym roztwory w probówkach zabarwiły się na czerwono, a po dodaniu alkoholowego roztworu fenoloftaleiny do probówek z wodnym roztworem wodorotlenku sodu roztwory w probówkach zabarwiły się na malinowo.
Po wprowadzeniu tlenku magnezu oraz tlenku glinu do probówek z kwasem chlorowodorowym i oranżem metylowym zaobserwowano roztworzenie się obydwu tlenków oraz zmianę zabarwienia roztworów z czerwonego na żółtopomarańczowe. Po wprowadzeniu tlenku fosforu() do probówki z kwasem chlorowodorowym i oranżem metylowym zaobserwowano roztworzenie się tlenku (roztwór pozostał jednak czerwony).
Po wprowadzeniu tlenku glinu oraz tlenku fosforu() do probówek z wodnymi roztworami wodorotlenku sodu i fenoloftaleiną zaobserwowano roztworzenie się obydwu tlenków oraz odbarwienie się malinowych roztworów. Po wprowadzeniu tlenku magnezu do probówki z wodnym roztworem wodorotlenku sodu i fenoloftaleiną zaobserwowano roztwarzanie się tlenki i wytrącanie się białego osadu (uzyskano zmętniony malinowy roztwór).
Wyniki:
Tlenek magnezu zareagował z kwasem chlorowodorowym, czego skutkiem był wzrost pH roztworu, nie zareagował on z kolei z wodnym roztworem wodorotlenku.
W przypadku tlenku glinu doszło do reakcji zarówno z kwasem chlorowodorowym, jak i wodnym roztworem wodorotlenku sodu – w obydwóch przypadkach doszło do zmiany pH.
Tlenek fosforu() zareagował z wodnym roztworem wodorotlenku, czego wynikiem był spadek pH roztworu, nie uległ on jednak reakcji z kwasem chlorowodorowym.
Wnioski:
Tlenek magnezu nie uległ reakcji z wodnym roztworem wodorotlenku, nie doszło do zmiany pH, a roztworzenie tlenku wynika z jego reakcji z wodą. Uległ on z kolei reakcji z kwasem, w wyniku czego nastąpił wzrost pH – była to zatem reakcja neutralizacji. Tlenek magnezu jest więc tlenkiem zasadowym.
Tlenek glinu uległ reakcji w obydwóch przypadkach i w obydwóch przypadkach doszło do zmiany pH – w reakcji z kwasem nastąpił wzrost, a w reakcji z wodnym roztworem wodorotlenku nastąpił spadek pH. Jest on zatem tlenkiem amfoterycznym.
Tlenek fosforu() uległ reakcji z wodnym roztworem wodorotlenku, czego skutkiem był spadek pH i nie zareagował on z kwasem (roztworzenie tlenku w tym przypadku było skutkiem jego reakcji z wodą). Jest to więc tlenek kwasowy.
Hipoteza została potwierdzona.
Równania reakcji chemicznych:
1.
2.
3.
4.
5.
6.
7.
8.
Hipoteza została potwierdzona.
Tlenki kwasowe
Doświadczenie: Badanie charakteru chemicznego tlenku siarki().
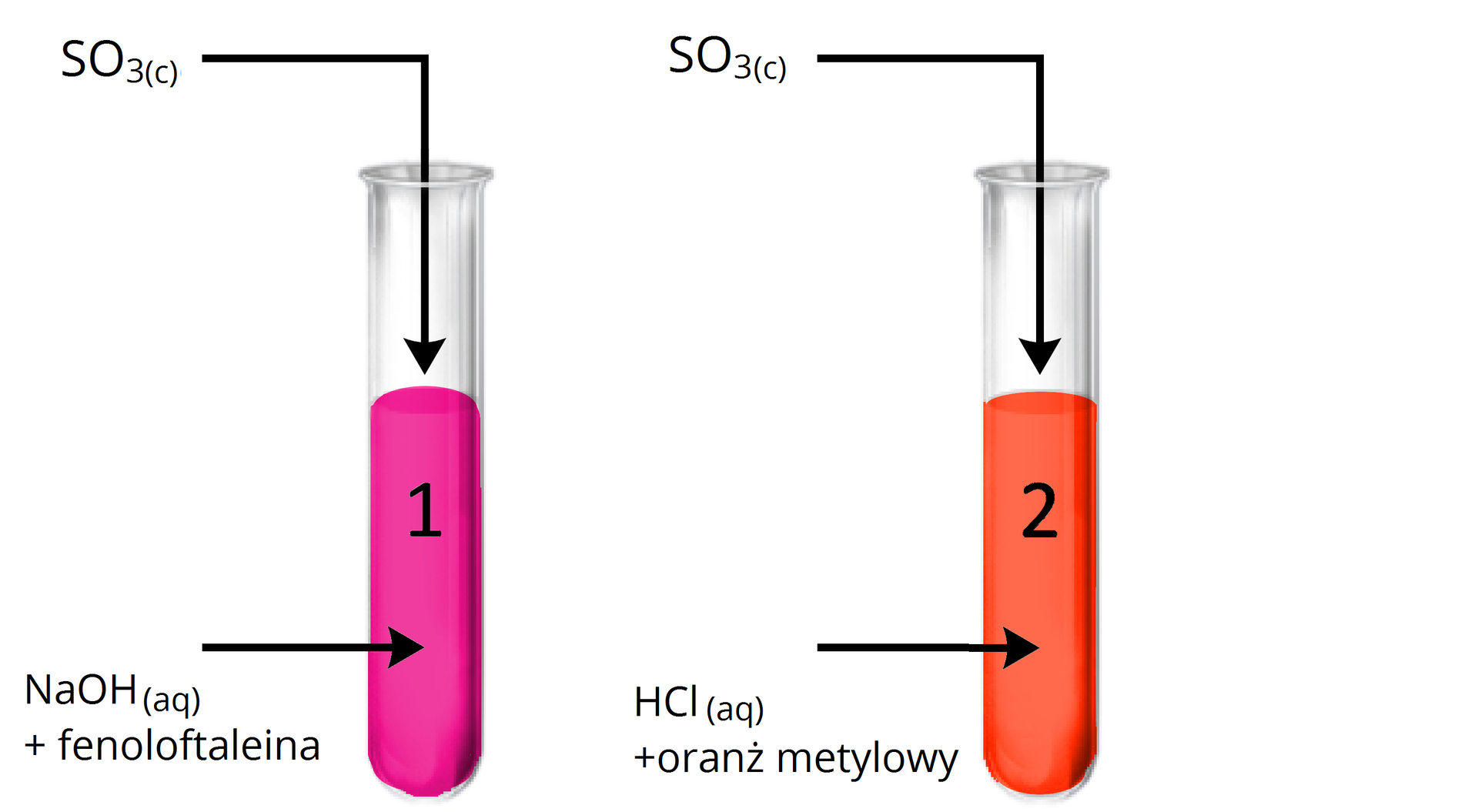
Obserwacje:
Probówka : Malinowy roztwór uległ odbarwieniu.
Probówka : Brak widocznych objawów reakcji.
Wniosek:
Tlenek siarki() jest tlenkiem kwasowym, ponieważ reaguje z zasadą (wodnym roztworem wodorotlenku), a nie reaguje z kwasem.
Równanie reakcji chemicznej z zasadą:
W formie cząsteczkowej:
W formie jonowej – skróconej:
Równanie reakcji chemicznej z kwasem:
Tlenki kwasowe są to tlenki niemetali oraz tlenki niektórych metali, które reagują z wodnymi roztworami wodorotlenków, a nie reagują z kwasami.
Tlenki kwasowe pierwiastków | ||
bloku | bloku | bloku |
brak | - | - |
W reakcjach tlenków kwasowych z roztworami wodorotlenków powstaje sól i woda. Reakcję tą można zapisać w sposób ogólny jako:
Tlenki zasadowe
Doświadczenie: Badanie charakteru chemicznego tlenku baru.
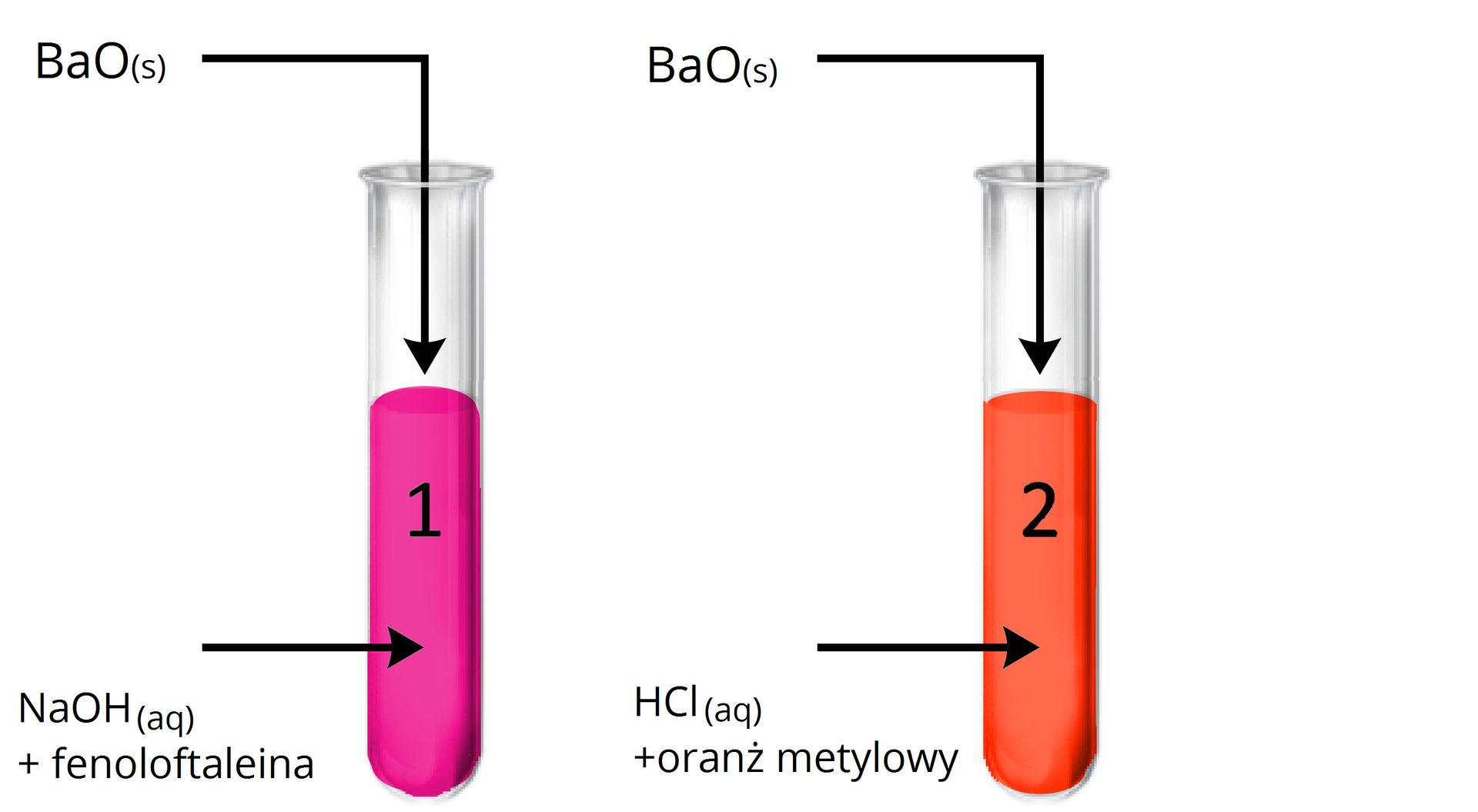
Obserwacje:
Probówka : Brak widocznych oznak reakcji z wodnym roztworem wodorotlenku sodu (Tlenek ulega rozpuszczeniu, ale roztwór nie zmienia zabarwienia).
Probówka : Ciało stałe uległo roztworzeniu. Roztwór zmienił barwę z czerwonej na żółtopomarańczową.
Wniosek:
Tlenek baru jest tlenkiem zasadowym, ponieważ reaguje z kwasem, a nie reaguje z zasadą (wodnym roztworem wodorotlenku).
Równanie reakcji chemicznej z kwasem:
W formie cząsteczkowej:
W formie jonowej – skróconej:
Równanie reakcji chemicznej z wodorotlenkiem:
Tlenki zasadowe, to tlenki metali, które reagują z kwasami, a nie reagują z wodorotlenkami.
Tlenki zasadowe metali | ||
bloku | bloku | bloku |
Wszystkie za wyjątkiem na przykład: | - | - |
W reakcjach tlenków zasadowych z kwasem powstaje sól i woda. Równanie tej reakcji można zapisać w sposób ogólny jako:
Tlenki amfoteryczne
Czy wiesz, jak zbadać właściwości amfoteryczne tlenków? Wprowadź do kolejnych probówek z tlenkiem cynku i tlenkiem glinu odpowiednio: kwas solny, wodny roztwór wodorotlenku sodu i wodę, a następnie rozwiąż poniższe ćwiczenia.
Zapoznaj się z opisem symulacji. Sprawdź, jak zbadać właściwości amfoteryczne tlenków.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DEO7C16VZ
Zapisz obserwacje i wnioski dotyczące właściwości chemicznych badanych tlenków.
Uzupełnij równania reakcji chemicznych.
Uzupełnij równania reakcji chemicznych.
Tlenki amfoteryczne typu ( – metal, – tlen), np. tlenek berylu ()
Reagują z mocnymi kwasami, np. z kwasem solnym:
Przykładowo, tlenek berylu reaguje z kwasem solnym, dzięki czemu powstaje chlorek berylu i woda:
Reagują z mocnymi zasadami, np. z wodnym roztworem wodorotlenku sodu.
W roztworze wodnym powstają sole kompleksowe, w których resztach kwasowych obecne są atomy lub jony metalu pochodzące od amfoterycznego tlenku, skompleksowane odpowiednią ilością grup hydroksylowych. Liczba grup hydroksylowych zależy od liczby koordynacyjnej charakterystycznej dla pierwiastka, która, w przypadku atomów pochodzących od tlenków typu , wynosi zazwyczaj 4.
Dla przykładu – tlenek berylu reaguje z wodorotlenkiem sodu i wodą, za sprawą czego powstaje tetrahydroksoberylan sodu:
Tlenki amfoteryczne typu ( – metal, – tlen), np. tlenek glinu ()
Reagują z mocnymi kwasami, np. z kwasem solnym:
Przykładowo tlenek glinu reaguje z kwasem solnym, w wyniku czego powstaje chlorek glinu i woda:
Reagują z mocnymi zasadami, np. z wodorotlenkiem sodu.
W roztworze wodnym powstają sole kompleksowe o liczbie koordynacyjnej 4 lub 6:
Dla przykładu – tlenek glinu reaguje z wodorotlenkiem sodu i wodą, w wyniku czego powstaje tetrahydroksoglinian sodu:
lub heksahydroksoglinian sodu:
Tlenki amfoteryczne nie reagują z wodą.
Przeanalizuj poniższą mapę myśli i zastanów się, gdzie w układzie okresowym zlokalizowane są pierwiastki, które tworzą tlenki amfoteryczne.
- Nazwa kategorii: Tlenki amfoteryczne
- Nazwa kategorii: tlenek berylu BeO
- Nazwa kategorii: tlenek glinu Al indeks dolny 2 koniec indeksu dolnego O indeks dolny 3 koniec indeksu dolnego
- Nazwa kategorii: tlenek cynku ZnO
- Nazwa kategorii: tlenek cyny dwa SnO
- Nazwa kategorii: tlenek ołowiu(II) PbO
- Nazwa kategorii: tlenek ołowiu cztery PbO indeks dolny 2 koniec indeksu dolnego
- Nazwa kategorii: tlenek cyny cztery SnO indeks dolny 2 koniec indeksu dolnego
- Nazwa kategorii: tlenek manganu cztery MnO indeks dolny 2 koniec indeksu dolnego
- Nazwa kategorii: tlenek miedzi dwa CuO
- Nazwa kategorii: tlenek chromu trzy Cr indeks dolny 2 koniec indeksu dolnego O indeks dolny 3 koniec indeksu dolnego Koniec elementów należących do kategorii Tlenki amfoteryczne
- Elementy należące do kategorii Tlenki amfoteryczne
Tlenki amfoteryczne, to tlenki metali oraz niemetali, które reagują zarówno z mocnymi kwasami jak i mocnymi zasadami (wodnymi roztworami wodorotlenków). Tlenki amfoteryczne nie reagują z wodą.
Tlenki amfoteryczne pierwiastków | ||
bloku | bloku | bloku |
- | - | - |
W reakcji tlenków amfoterycznych z mocnym kwasem powstaje sól i woda zgodnie z poniższym ogólnym równaniem reakcji:
W reakcji tlenków amfoterycznych z mocną zasadą (na przykład wodny roztwór lub ) powstaje związek koordynacyjny, tzw. sól kompleksowa, w której kation metalu stanowi atom centralny, a aniony wodorotlenkowe pełnią funkcję ligandów. W reakcji jednym z substratów jest również woda. Schemat równania tej reakcji można zapisać w sposób ogólny:
Klasyfikacja tlenków według charakteru chemicznego
- Nazwa kategorii: Charakter chemiczny tlenków
- Nazwa kategorii: Kwasowy
- Nazwa kategorii: Reagują z wodnymi roztworami wodorotlenków tworząc sole.
- Nazwa kategorii: W większości reagują z wodą tworząc odpowiednie kwasy.
- Nazwa kategorii: Tworzą sole z tlenkami zasadowymi. Koniec elementów należących do kategorii Kwasowy
- Nazwa kategorii: Zasadowy
- Nazwa kategorii: Reagują z kwasami tworząc sole.
- Nazwa kategorii: Tlenki litowców i berylowców reagują z wodą tworząc odpowiedni wodorotlenek. Koniec elementów należących do kategorii Zasadowy
- Nazwa kategorii: Amfoteryczny
- Nazwa kategorii: Reagują z kwasami i wodnymi roztworami wodorotlenków tworząc sole.
- Nazwa kategorii: Zazwyczaj nie reagują z wodą. Koniec elementów należących do kategorii Amfoteryczny
- Nazwa kategorii: Obojętny
- Nazwa kategorii: Nie reagują z kwasami, wodnymi roztworami wodorotlenków ani z wodą. Koniec elementów należących do kategorii Obojętny
- Elementy należące do kategorii Charakter chemiczny tlenków
- Elementy należące do kategorii Kwasowy
- Elementy należące do kategorii Zasadowy
- Elementy należące do kategorii Amfoteryczny
- Elementy należące do kategorii Obojętny
Ze względu na jakie czynniki klasyfikuje się tlenki? Przeanalizuj mapę interaktywną, uzupełnij ją o inne przykłady tlenków pasujących do róznych kategorii, a następnie rozwiąż ćwiczenia znajdujące się pod mapą.
Mapa pojęciowa dotycząca klasyfikacji tlenków ze względu na: charakter chemiczny, stan skupienia, charakter wiązania chemicznego, zachowanie wobec wody i rodzaj pierwiastka wchodzącego w skład tlenku, wraz z przykładami.
Nazwa kategorii: Klasyfikacja tlenków.
Elementy należące do kategorii Klasyfikacja tlenkówNazwa kategorii: ze względu na charakter chemiczny
Elementy należące do kategorii ze względu na charakter chemicznyNazwa kategorii: kwasowe
Elementy należące do kategorii kwasoweKoniec elementów należących do kategorii kwasowe
Nazwa kategorii: obojętne
Elementy należące do kategorii obojętneKoniec elementów należących do kategorii obojętne
Nazwa kategorii: zasadowe
Elementy należące do kategorii zasadoweKoniec elementów należących do kategorii zasadowe
Nazwa kategorii: amfoteryczne
Elementy należące do kategorii amfoteryczneKoniec elementów należących do kategorii amfoteryczne
Koniec elementów należących do kategorii ze względu na charakter chemiczny
Nazwa kategorii: ze względu na stan skupienia
Elementy należące do kategorii ze względu na stan skupieniaNazwa kategorii: ciecze
Elementy należące do kategorii cieczeKoniec elementów należących do kategorii ciecze
Nazwa kategorii: gazy
Elementy należące do kategorii gazyKoniec elementów należących do kategorii gazy
Nazwa kategorii: ciała stałe
Elementy należące do kategorii ciała stałeKoniec elementów należących do kategorii ciała stałe
Koniec elementów należących do kategorii ze względu na stan skupienia
Nazwa kategorii: ze względu na charakter wiązania chemicznego
Elementy należące do kategorii ze względu na charakter wiązania chemicznegoNazwa kategorii: zawierające wiązanie kowalencyjne
Elementy należące do kategorii zawierające wiązanie kowalencyjneKoniec elementów należących do kategorii wiązanie kowalencyjne
Nazwa kategorii: zawierające wiązanie jonowe
Elementy należące do kategorii zawierające wiązanie jonoweKoniec elementów należących do kategorii wiązanie jonowe
Koniec elementów należących do kategorii ze względu na charakter wiązania chemicznego
Nazwa kategorii: ze względu na zachowanie wobec wody
Elementy należące do kategorii ze względu na zachowanie wobec wodyNazwa kategorii: reagujące z wodą
Elementy należące do kategorii reagujące z wodąNazwa kategorii: zasadotwórcze
Elementy należące do kategorii zasadotwórczeKoniec elementów należących do kategorii zasadotwórcze
Nazwa kategorii: kwasotwórcze
Elementy należące do kategorii kwasotwórczeKoniec elementów należących do kategorii kwasotwórcze
Koniec elementów należących do kategorii reagujące z wodą
Nazwa kategorii: niereagujące z wodą
Elementy należące do kategorii niereagujące z wodąKoniec elementów należących do kategorii niereagujące z wodą
Koniec elementów należących do kategorii ze względu na zachowanie wobec wody
Nazwa kategorii: ze względu na rodzaj pierwiastka wchodzącego w skład tlenku
Elementy należące do kategorii ze względu na rodzaj pierwiastka wchodzącego w skład tlenkuNazwa kategorii: tlenki metali
Elementy należące do kategorii tlenki metaliKoniec elementów należących do kategorii tlenki metali
Nazwa kategorii: tlenki niemetali
Elementy należące do kategorii tlenki niemetaliKoniec elementów należących do kategorii tlenki niemetali
Koniec elementów należących do kategorii ze względu na rodzaj pierwiastka wchodzącego w skład tlenku
Koniec elementów należących do kategorii Klasyfikacja tlenków
Do jakiej grupy klasyfikuje się tlenek glinu ze względu na charakter chemiczny? Zapisz równania reakcji chemicznych, które potwierdzają tę tezę.
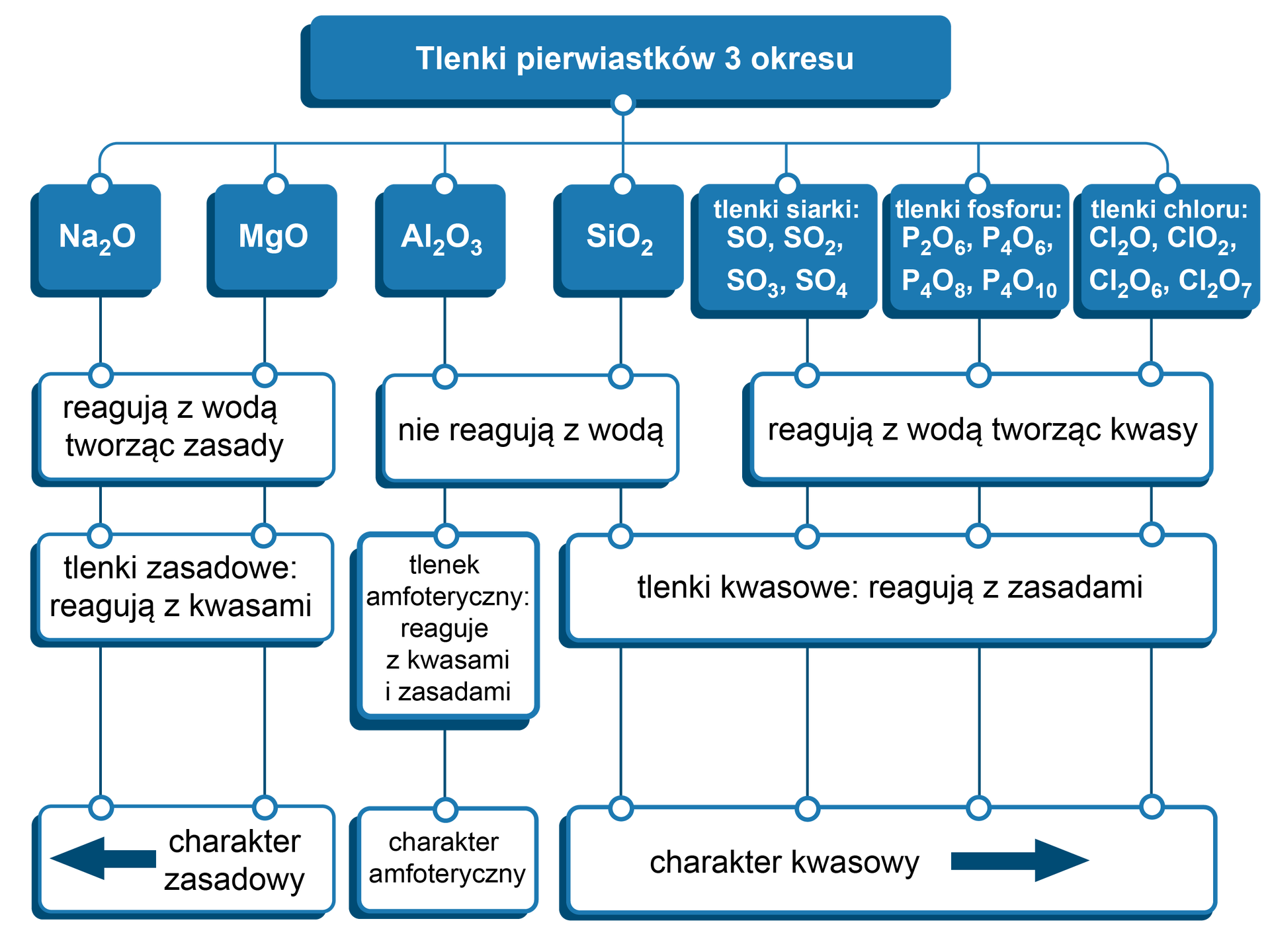
Zmiana charakteru chemicznego wybranych tlenków na tle układu okresowego
Zmiana charakteru tlenków zależna jest od położenia pierwiastka tworzącego dany tlenek w układzie okresowym. Tlenki metali reagują z kwasami – nazywamy je tlenkami zasadowymi. Te, które reagują z zasadami, nazywamy tlenkami kwasowymi – są to głównie tlenki niemetali. Istnieją również tlenki amfoteryczne, reagują one zarówno z kwasami, jak i zasadami.
Czy znasz wzory sumaryczne tlenków metali należących do układu okresowego pierwiastków? Jaki wykazują charakter te tlenki? Przeanalizuj poniższą grafikę interaktywną, a następnie rozwiąż ćwiczenia sprawdzające.
Czy znasz wzory sumaryczne tlenków metali należących do układu okresowego pierwiastków? Jaki wykazują charakter te tlenki? Przeanalizuj opis grafiki interaktywnej, a następnie rozwiąż ćwiczenia sprawdzające.
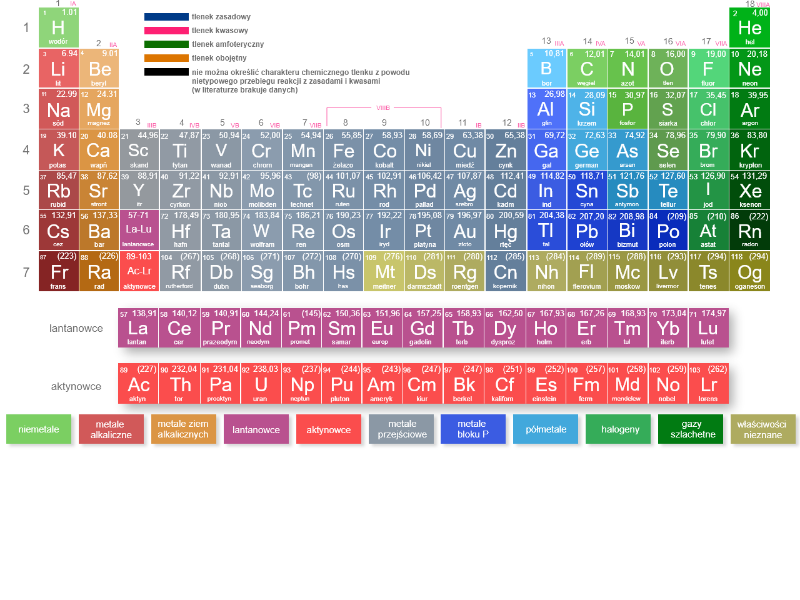
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DEO7C16VZ