Właściwości kwasów karboksylowych
Poniższy materiał stanowi uzupełnienie treści zawartych w materiale: https://zpe.gov.pl/a/kwasy-karboksylowe–wlasciwosci/D105PJpVe
Czy wiesz, co jest głównym składnikiem świec? Składnik ten służy między innymi do utwardzania wosku i wpływa na jego temperaturę topnienia, a przy tym długość palenia świecy. Dodatkowo zwiększa jej trwałość. Co ciekawe, ta sama substancja wykorzystywana jest do utwardzania mydeł i nadaje im perłowy połysk. A mowa o stearynie, czyli mieszaninie przede wszystkim dwóch substancji: kwasu stearynowego i kwasu palmitynowego. Kwasy te należą do wyższych kwasów karboksylowych i znalazły zastosowanie w wielu dziedzinach.
budowę cząsteczek kwasów karboksylowych;
sposób rysowania wzorów strukturalnych kwasów karboksylowych;
sposób nazewnictwa kwasów karboksylowych.
opisywać właściwości fizyczne kwasu mrówkowego (metanowego) oraz kwasu octowego (etanowego);
zapisywać równania reakcji dysocjacji jonowej kwasu mrówkowego i kwasu octowego;
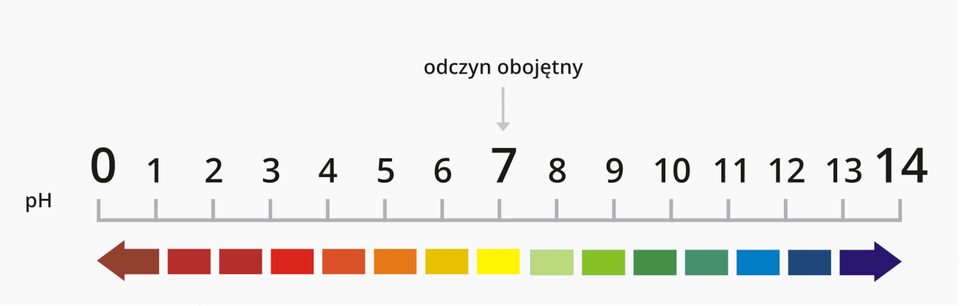
badać odczyn wodnych roztworów kwasu mrówkowego i kwasu octowego;
zapisywać równania reakcji kwasu mrówkowego i kwasu octowego z wodorotlenkami, tlenkami metali, metalami;
opisywać wybrane właściwości fizyczne i chemiczne długołańcuchowych kwasów monokarboksylowych;
odróżniać kwas oleinowy od palmitynowego lub stearynowego.
Kwasy karboksylowe to związki chemiczne o wzorze ogólnym:
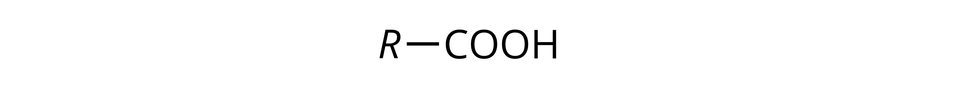
gdzie:
– oznacza grupę węglowodorową;
– grupę karboksylową.
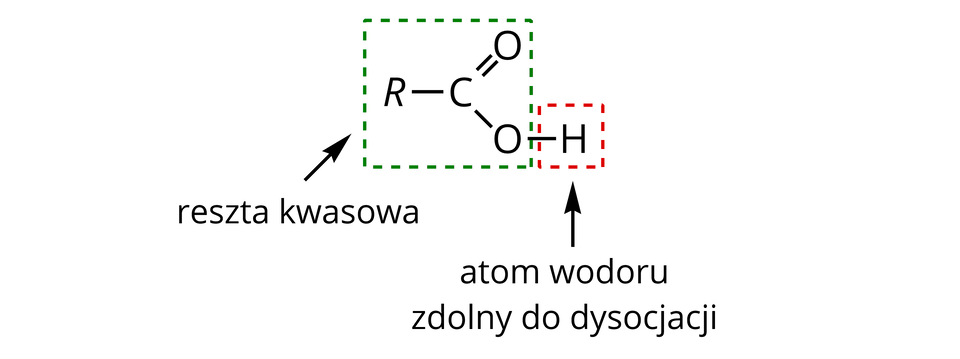
Kwasy karboksylowe są pochodnymi węglowodorów, w których część łańcucha węglowego stanowi grupa funkcyjna – grupa karboksylowagrupa karboksylowa.
W poniższej tabeli zestawiono kilka najważniejszych kwasów karboksylowych.
Nazwa kwasu | Wzór z zaznaczeniem grupy karboksylowej | Wzór grupowy (Wzór uwzględniający występowanie izomerii geometrycznej) |
|---|---|---|
kwas metanowy (kwas mrówkowy) | ||
kwas etanowy (kwas octowy) | ||
kwas heksadekanowy (kwas palmitynowy) | ||
kwas oktadekanowy (kwas stearynowy) | ||
kwas octadec––enowy (kwas oleinowy) | 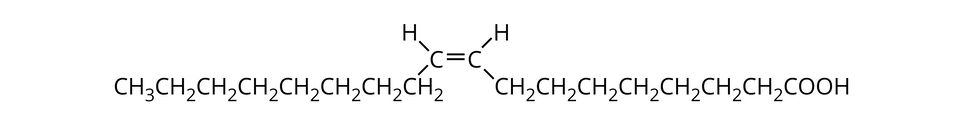 Wzór uwzględniający występowanie izomerii geometrycznej. Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |
Kwas mrówkowyKwas mrówkowy i kwas octowykwas octowy należą do niższych kwasów karboksylowych i są pochodnymi odpowiednio metanu i etanu. Dlatego kwas mrówkowy zawiera jeden atom węgla w cząsteczce, a kwas octowy – dwa. Kwasy (palmitynowy, stearynowy oraz oleinowy) należą do wyższych kwasów karboksylowychwyższych kwasów karboksylowych i pochodzą od alkanów zawierających kilkanaście atomów węgla w cząsteczkach.
1. Jakie właściwości fizyczne i chemiczne mają kwas mrówkowy i kwas octowy?
Zarówno kwas mrówkowy, jak i kwas octowy w temperaturze pokojowej są bezbarwnymi cieczami o gęstości zbliżonej do gęstości wody (nieznacznie większej).
Kwasy te dobrze rozpuszczają się w wodzie i ulegają w niej dysocjacji jonowejdysocjacji jonowej (rozpadowi na jony). Podobnie jak w przypadku kwasów nieorganicznych, kwasy karboksylowe dysocjują na kation wodoru i anion reszty kwasowej.
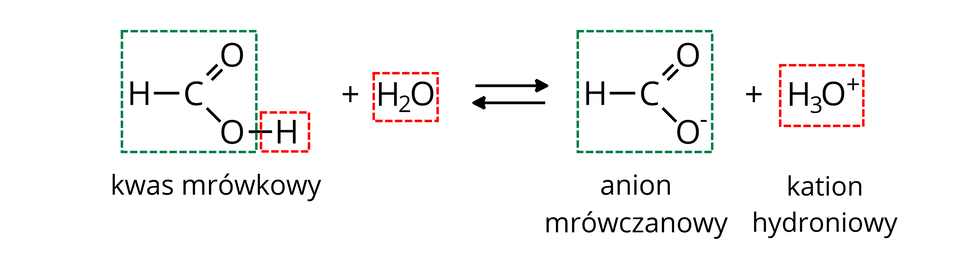
Równanie dysocjacji jonowej kwasu mrówkowego:
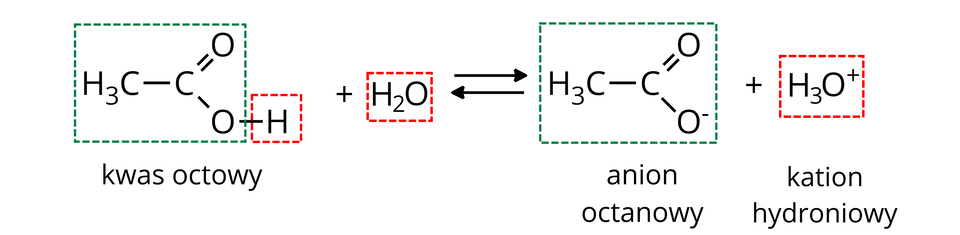
Równanie dysocjacji jonowej kwasu octowego:
Uwaga! W równaniach dysocjacji jonowej obu kwasów zapisuje się strzałki w obie strony, ponieważ substancje te nie ulegają dysocjacji w . Oznacza to, że w wodzie obecne są, oprócz anionów reszt kwasowych i kationów hydroniowych, cząsteczki kwasów.
Pamiętaj! Powstający podczas dysocjacji jonowej kation hydroniowy odpowiedzialny jest za kwasowy odczyn obu kwasów oraz ich właściwości kwasowe.
Zbadano odczyn wodnych roztworów kwasu mrówkowego i octowego za pomocą uniwersalnego papierka wskaźnikowego i wodnego roztworu oranżu metylowego. Tym samym wykazano kwasowy odczyn tych substancji.
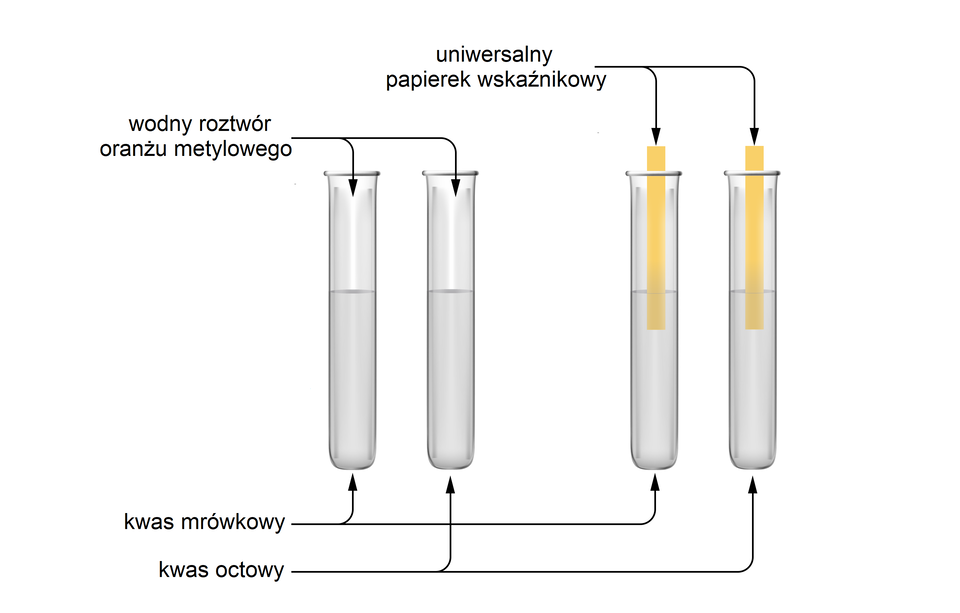
Zbadano odczyn wodnych roztworów kwasu mrówkowego i octowego za pomocą uniwersalnego papierka wskaźnikowego i wodnego roztworu oranżu metylowego. Tym samym wykazano kwasowy odczyn tych substancji. Probówki ponumerowano jako:
Probówka : kwas mrówkowy wodny roztwór oranżu metylowego;
Probówka : kwas octowy wodny roztwór oranżu metylowego;
Probówka : kwas mrówkowy uniwersalny papierek wskaźnikowy;
Probówka : kwas octowy uniwersalny papierek wskaźnikowy.
2. Jakie właściwości fizyczne i chemiczne mają wyższe kwasy karboksylowe?
Do wyższych kwasów karboksylowych zaliczamy wszystkie te kwasy, w których cząsteczkach znajduje się od do atomów węgla. Potocznie nazywa się je również kwasami tłuszczowymi, ze względu na ich występowanie oraz ich pochodnych w tłuszczach.
Kwas palmitynowy i stearynowy to bezwonne, białe ciała stałe. Kwas oleinowy to natomiast jasnożółta ciecz o charakterystycznym, nieprzyjemnym zapachu. Kwasy tłuszczowe charakteryzują się mniejszą gęstością od gęstości wody, a zatem unoszą się na jej powierzchni.
Ze względu na obecność długich, niepolarnych łańcuchów węglowych, kwasy tłuszczowe są trudno rozpuszczalne w wodzie. Zatem odczyn wodnych roztworów wyższych kwasów karboksylowych jest obojętny. Z tego samego powodu kwasy tłuszczowe bardzo dobrze rozpuszczają się w rozpuszczalnikach organicznych, np. trichlorometanie (chloroformie) czy benzynie.
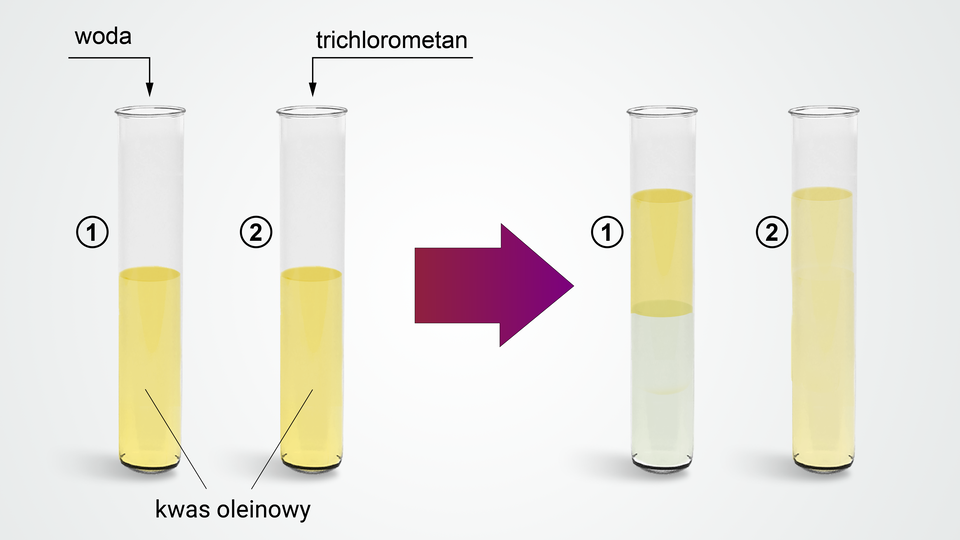
Kwas palmitynowy oraz kwas stearynowy należą do nasyconych wyższych kwasów karboksylowych. Oznacza to, że pomiędzy atomami węgla w ich cząsteczkach występują wyłącznie wiązania pojedyncze. Natomiast kwas oleinowy należy do nienasyconych wyższych kwasów karboksylowych, ponieważ pomiędzy a atomem węgla w cząsteczce tego kwasu występuje wiązanie podwójne. Charakter nienasycony posiadają substancje zawierające wiązania wielokrotne pomiędzy atomami węgla w cząsteczce.
Różnica w budowie tych kwasów pozwala na odróżnienie ich od siebie za pomocą próby z roztworem bromu w rozpuszczalniku organicznym (np. trichlorometanie (chloroformie) o wzorze ). Nienasycone kwasy tłuszczowe reagują z bromem w temperaturze pokojowej, a nasycone kwasy tłuszczowe w temperaturze pokojowej nie reagują.
Przyjrzyj się poniższemu schematowi doświadczenia.
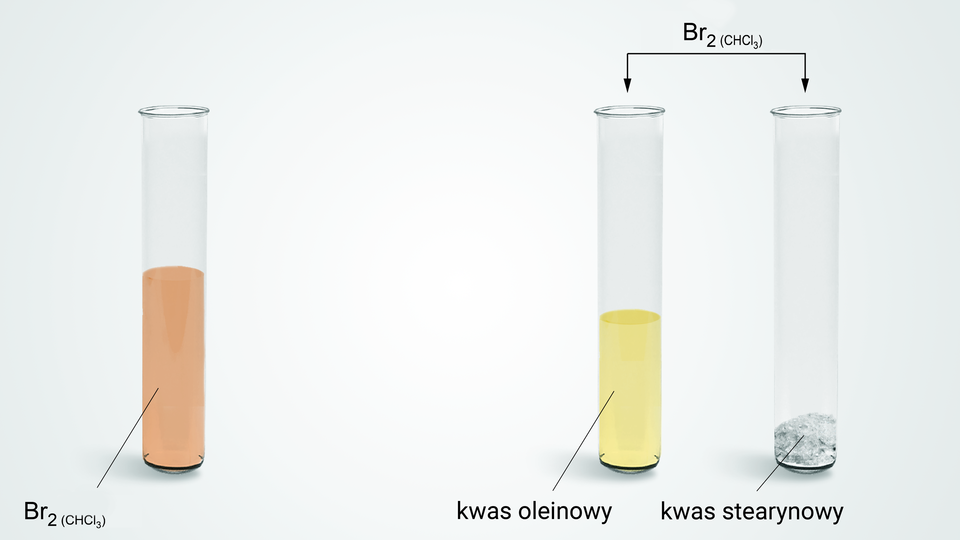
W wyniku wprowadzenia roztworu bromu w chloroformie do kwasu oleinowego otrzymujemy bezbarwny roztwór. Oznacza to, że pomarańczowy roztwór bromu odbarwia się pod wpływem kwasu oleinowego. Natomiast po wprowadzeniu roztworu bromu w chloroformie do kwasu stearynowego, biała substancja stała wypływa na powierzchnię, a roztwór bromu nie zmienia swojego zabarwienia. Kwas stearynowy nie uległ zatem reakcji z bromem. Kwas oleinowy natomiast uległ reakcji z bromem, co można zapisać następującym równaniem reakcji chemicznej:
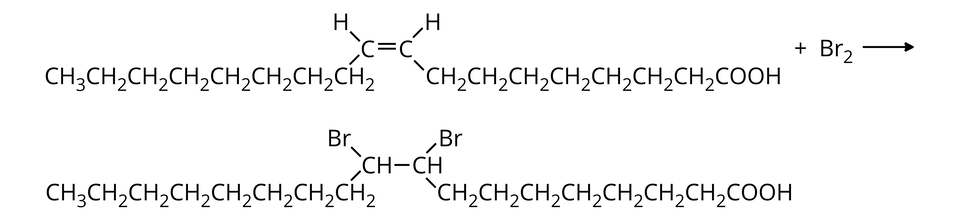
Uwaga! Bardzo często przeprowadza się tą próbę z wodą bromową (oznaczaną jako ). Jednak brom lepiej rozpuszcza się w rozpuszczalniku organicznym niż nieorganicznym, jakim jest woda. Dzieje się tak ze względu na podobieństwo wiązań chemicznych pomiędzy atomami. Pomiędzy atomami bromu występuje wiązanie kowalencyjne (atomowe), takie jak pomiędzy atomami węgla w cząsteczkach organicznych.
Wyższe kwasy karboksyloweWyższe kwasy karboksylowe ulegają reakcji z wodorotlenkiem sodu i potasu w podwyższonej temperaturze. W ich wyniku powstają mydłamydła (np. stearynian potasu czy oleinian sodu).

Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym polegające na zbadaniu właściwości fizykochemicznych kwasu octowego. Rozwiąż problem badawczy i zweryfikuj hipotezę.
Zapoznaj się z opisem doświadczenia przeprowadzonego w wirtualnym laboratorium chemicznym, polegającym na zbadaniu właściwości fizykochemicznych kwasu octowego. Zapoznaj się z problemem badawczym, hipotezą, obserwacjami oraz wnioskami wyciągniętymi z eksperymentu.
Temat:
Badanie właściwości fizykochemicznych kwasu octowego.
Problem badawczy:
Jaka barwę ma wodny roztwór kwasu octowego? Jaki odczyn wykazuje wodny roztwór kwasu octowego? Czy kwas octowy reaguje z wodorotlenkiem sodu, magnezem i tlenkiem miedzi()
Hipoteza:
Wodny roztwór kwasu octowego jest bezbarwny i ma odczyn kwasowy. Kwas octowy reaguje z wodorotlenkiem sodu, magnezem i tlenkiem miedzi().
Sprzęt laboratoryjny:
statyw z czterema probówkami;
pipety;
pręciki szklane;
łyżeczki.
Odczynniki chemiczne:
wodny roztwór kwasu octowego;
wodny roztwór oranżu metylowego;
wodny roztwór wodorotlenku sodu;
wiórki magnezowe;
tlenek miedzi().
Przebieg eksperymentu:
Za pomocą pipety do wszystkich probówek wlano po około roztworu kwasu octowego i sprawdzono jego barwę i zapach.
Do pierwszej oraz drugiej probówki dodano za pomocą pipety kilka kropel wodnego roztworu oranżu metylowego. Całość następnie zamieszano.
Do drugiej probówki wlano około wodnego roztworu wodorotlenku sodu. Całość następnie zamieszano.
Do trzeciej probówki wsypano kilka wiórków magnezowych.
Do czwartej probówki wsypano niewielką ilość tlenku miedzi(). Całość następnie zamieszano.
Obserwacje:
Wodny roztwór kwasu octowego jest bezbarwny. Wyczuwalny jest charakterystyczny zapach octuoctu. Po dodaniu kilku kropel wodnego roztworu oranżu metylowego do probówki i , obserwujemy powstanie klarownego roztworu barwy czerwonej. Po dodaniu wodnego roztworu wodorotlenku sodu do probówki – obserwujemy zmianę barwy roztworu z czerwonej na pomarańczowo–żółtą. W probówce wiórki magnezowe stopniowo roztwarzają się. Jednocześnie wydziela się intensywnie bezbarwny gaz (widoczne pęcherzyki gazu w probówce). W probówce stopniowo roztwarza się czarny proszek i pojawia się klarowny roztwór barwy niebieskiej.
Wyniki:
Wodny roztwór kwasu octowego jest bezbarwny i ma charakterystyczny zapach. Wykazuje odczyn kwasowy, ponieważ barwi wodny roztwór oranżu metylowego na czerwono. Kwas octowy reaguje z wodorotlenkiem sodu, magnezem i tlenkiem miedzi().
Wnioski:
W przypadku zaproponowanej hipotezy: Hipoteza została potwierdzona.
W formularzu zapisz obserwacje, a następnie sformułuj wnioski.
Kwas octowy, reagując z wodorotlenkami, tlenkami metali i metalami aktywnymi, tworzy: Możliwe odpowiedzi: 1. kwasy, 2. sole, 3. wyższe kwasy karboksylowe, 4. tlenki
Uniwersalny papierek wskaźnikowy po zanurzeniu w wodnym roztworze kwasu octowego: Możliwe odpowiedzi: 1. pozostaje żółty, 2. przyjmuje zielone zabarwienie, 3. przyjmuje pomarańczowe zabarwienie, 4. przyjmuje czerwone zabarwienie, 5. przyjmuje fioletowo–zielone zabarwienie
Słownik
grupa funkcyjna kwasów karboksylowych
pierwszy związek chemiczny w szeregu homologicznym kwasów karboksylowych
drugi związek chemiczny w szeregu homologicznym kwasów karboksylowych
–procentowy lub –procentowy wodny roztwór kwasu octowego; na półkach sklepowych możemy znaleźć kilka rodzajów octu (jabłkowy, winny, spirytusowy)
Kwasy karboksylowe zawierające od do atomów węgla w cząsteczce
rozpad związku chemicznego na jony pod wpływem rozpuszczalnika, np. wody
sole sodowe lub potasowe wyższych kwasów karboksylowych
Ćwiczenia
Zaznacz, które z poniższych produktów powstają podczas tej reakcji chemicznej. Produktami reakcji octu z wodorotlenkiem sodu są:
Bezbarwny, bezwonny gaz wydziela się podczas reakcji kwasów karboksylowych z: Możliwe odpowiedzi: 1. wodorotlenkami., 2. tlenkami metali., 3. metalami aktywnymi., 4. solami.
Spośród poniższych wzorów zapisz dwie pary wzorów grupowych tych kwasów, które możesz odróżnić od siebie za pomocą roztworu bromu w chloroformie.
Bibliografia
Danikiewicz W., Chemia organiczna, cz. 3, Warszawa 2009.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy siódmej szkoły podstawowej, Mac Edukacja 2020.