Wodorki – właściwości i zastosowanie
Jak budowa związku wpływa na jego właściwości fizykochemiczne?
Właściwości fizyczne, takie jak np. stan skupienia w temperaturze pokojowej oraz właściwości chemiczne (rozpuszczalność w wodzie, charakter kwasowo–zasadowy), wynikają z budowy danego związku oraz z charakteru występującego w nim wiązania.
Na podstawie temperatury wrzenia można wysnuć wnioski dotyczące rodzaju wiązania oraz oddziaływań międzycząsteczkowych. Niskie temperatury wrzenia cechują substancje zbudowane z cząsteczek o charakterze niepolarnym, wówczas jedynym rodzajem oddziaływań, które zachodzą między cząsteczkami, są wyłącznie słabe oddziaływania van der Waalsa. Silniejsze oddziaływania obserwuje się między dipolami, a z kolei obecność atomu wodoru, związanego z silnie elektroujemnym atomem fluoru, tlenu lub azotu, warunkuje możliwość tworzenia wiązań wodorowych. Najwyższe temperatury wrzenia są obserwowane dla substancji o budowie jonowej, ponieważ wiązanie jonowe ma charakter kolektywny, tj. obejmuje wszystkie jony, które wchodzą w skład kryształu.
Budowa związku chemicznego warunkuje także właściwości chemiczne, takie jak charakter kwasowy lub zasadowy.
Właściwości fizyczne i chemiczne wodorków
Wodorki niemetali mają następujące właściwości:

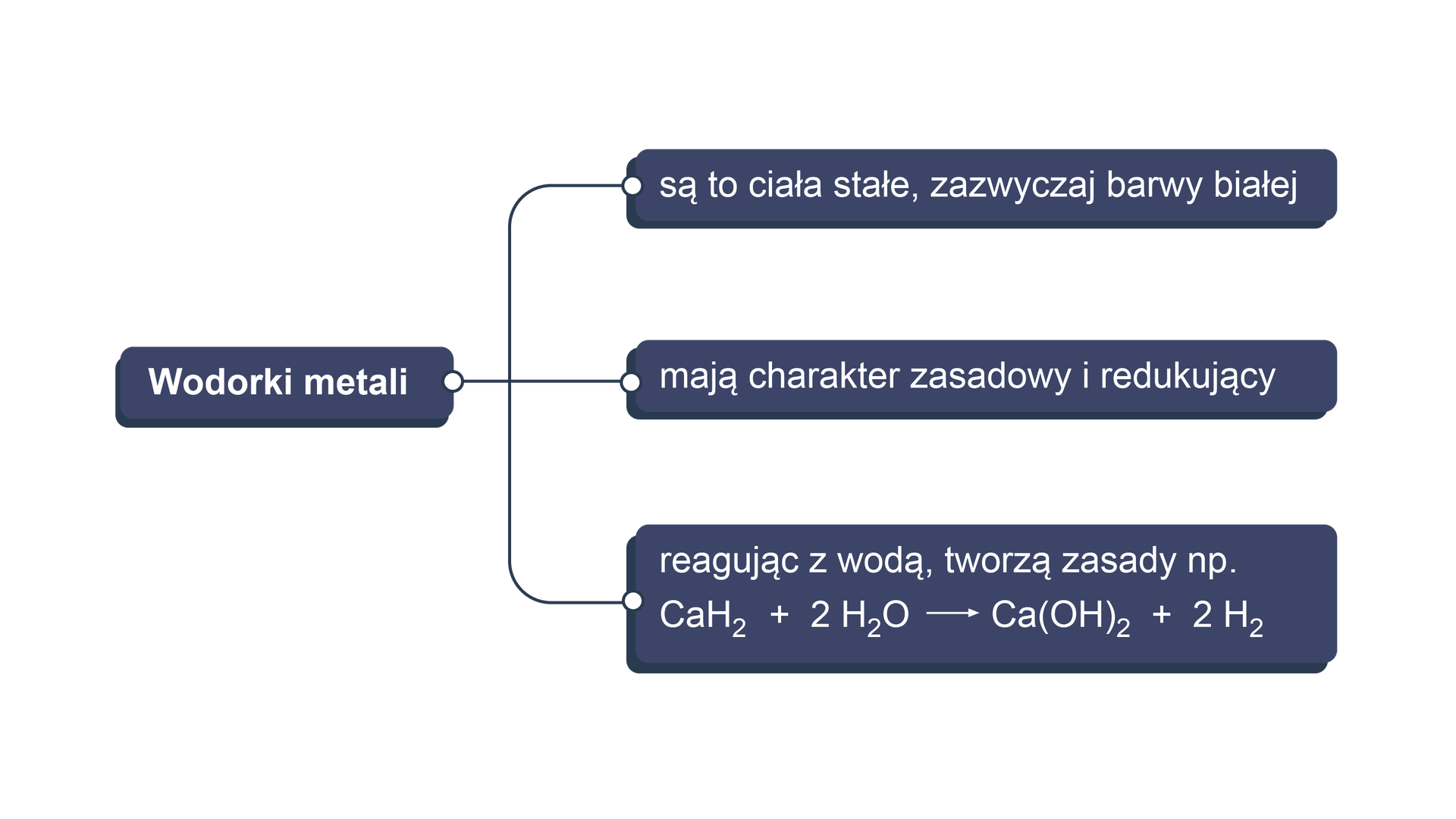
Wodorki metali mają odmienne właściwości:
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje i wyniki, a następnie sformułuj wnioski. Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się pod ikoną notatnika w lewym górnym rogu.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D381ELASJ
Analiza doświadczenia: Badanie właściwości fizykochemicznych wodorków.
Problem badawczy: Czy właściwości fizykochemiczne wodorków zależą od rodzaju wodorku?
Hipoteza: Właściwości fizykochemiczne wodorków są zależne od rodzaju wodorku.
Odczynniki: wodorek wapnia, metan, amoniak, siarkowodór, chlorowodór, alkoholowy roztwór fenoloftaleiny, roztwór oranżu metylowego, woda destylowana.
Sprzęt laboratoryjny: pięć probówek podłużnych – naczynie szklane do przeprowadzania prostych reakcji chemicznych; statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki; cztery korki – niewielki element wykonany z plastiku, służący do szczelnego zamykania probówek; pięć zlewek – naczynia szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych; cztery rurki szklane.
Instrukcja wykonania doświadczenia:
1. Zbadano właściwości fizyczne następujących związków: wodorku wapnia, metanu, amoniaku, siarkowodoru oraz chlorowodoru.
2. Zbadano właściwości chemiczne tych samych związków.
3. Do pięciu zlewek dodano wodę destylowaną. Do zlewek numer i dodano kilka kropli alkoholowego roztworu fenoloftaleiny, a do zlewek numer i roztwór oranżu metylowego.
4. Do pierwszej zlewki wsypano wodorek wapnia.
5. W probówkach z gazami, zatkanych korkiem, umieszczono rurki, a następnie umieszczono je dnem do góry w zlewkach w sposób następujący: zlewka numer – metan, zlewka numer – amoniak, zlewka numer – siarkowodór, zlewka numer – chlorowodór.
6. Zaobserwowano zmiany.
Obserwacje:
Badanie właściwości fizycznych:
Stan skupienia: metan, amoniak, kwas siarkowodorowy i kwas chlorowodorowy są bezbarwnymi gazami, zaś wodorek wapnia białym ciałem stałym.
Zapach: wodorek wapnia i metan są bezwonne, amoniak i kwas siarkowodorowy mają charakterystyczny zapach, natomiast kwas chlorowodorowy ma ostry, drażniący zapach.
Badanie właściwości chemicznych:
Zlewka : po wprowadzeniu wodorku wapnia do zlewki z wodą destylowaną wydziela się bezbarwny gaz oraz pojawia się biały osad.
Zlewka : brak dostrzegalnych zmian.
Zlewka : gaz rozpuszcza się w wodzie, powstały roztwór zmienia zabarwienie na kolor malinowy.
Zlewka : gaz rozpuszcza się w wodzie, powstały roztwór zmienia zabarwienie na kolor czerwony.
Zlewka : gaz rozpuszcza się w wodzie, powstały roztwór zmienia zabarwienie na kolor czerwony.
Wyniki:
Wydzielającym się gazem w reakcji wodorku wapnia z wodą destylowaną jest wodór. Brak zmiany zabarwienia w przypadku roztworu w zlewce numer świadczy o jego obojętnym odczynie. W zlewce numer dostrzegalna jest zmiana zabarwienia roztworu na kolor malinowy, co charakteryzuje roztwory o odczynie zasadowym. W zlewce numer i roztwory zmieniają zabarwienie na kolor czerwony, co warunkuje ich kwasowy odczyn.
Wnioski:
Hipoteza została potwierdzona – właściwości fizyczne i chemiczne są zależne od rodzaju wodorku.
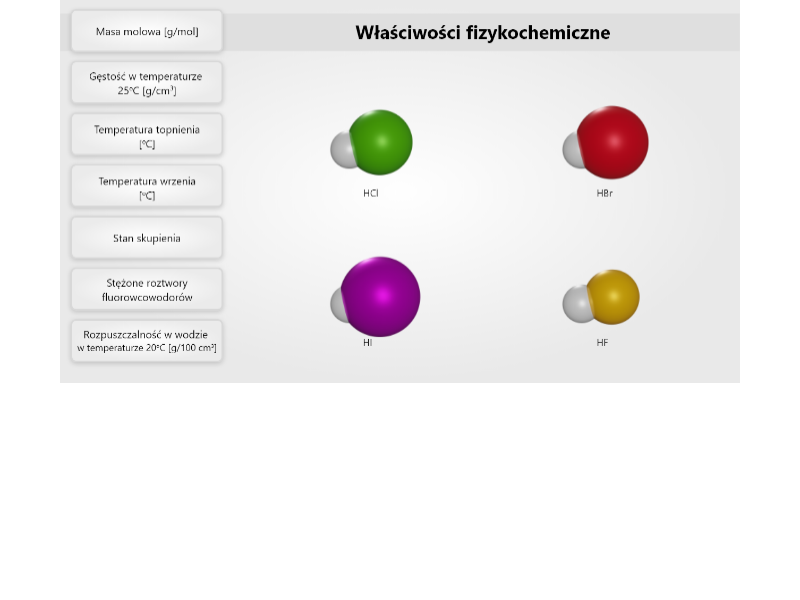
Przeanalizuj poniższą symulację. Zwróć uwagę, jak zmieniają się właściwości fizykochemiczne wodorków pierwiastków grupy, a następnie rozwiąż ćwiczenia sprawdzające.
Zapoznaj się z opisem symulacji. Zwróć uwagę, jak zmieniają się właściwości fizykochemiczne wodorków pierwiastków grupy, a następnie rozwiąż ćwiczenia sprawdzające.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D381ELASJ
Przeanalizuj dane zawarte w symulacji i odpowiedz na poniższe pytanie.
W jaki sposób zmieniają się temperatury topnienia i wrzenia wodorków fluorowców, w zależności od położenia fluorowców w układzie okresowym?
W trzech probówkach znajdowało się po -molowego, wodnego roztworu, odpowiednio: w probówce , w probówce , probówce . Zbadano odczyn tych roztworów oraz ich pH. W której z probówek stwierdzono najniższą wartość pH?
Czy wiesz, jak reagują wodorki z innymi wodorkami? W poniższej symulacji wybierz dwa dowolne wodorki pierwiastków 2. i 3. okresu (nie ma możliwości wybrania dwóch pól z tej samej grupy) i sprawdź, czy reagują ze sobą oraz jak przebiega reakcja chemiczna pomiędzy wybraną parą. Następnie rozwiąż poniższe zadania.
Czy wiesz, jak reagują wodorki z innymi wodorkami? Zapoznaj się z opisem symulacji. Następnie rozwiąż poniższe zadania.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D381ELASJ
Zapisz, jak reaguje amoniak z innymi wodorkami.
Zaprojektuj doświadczenie, w którym amoniak reaguje z wybranym wodorkiem.