Zapisy chemiczne - interpretacja
Chemicy na całym świecie potrafią porozumiewać się bez słów, ponieważ wszyscy władają jednym wspólnym językiem chemicznym. Opiera się on na znajomości symboli pierwiastków chemicznych, wzorów związków chemicznych, cząsteczek i innych drobin, a także zapisie równań reakcji, czyli przede wszystkim na interpretacji różnych zapisów chemicznych. W tym materiale przeczytasz między innymi, jaka jest różnica między zapisami: , , , czy , oraz nauczysz się, w jaki sposób interpretujemy równania reakcji chemicznych.
symbole pierwiastków chemicznych;
definicję pierwiastka chemicznego;
rodzaje wiązań chemicznych.
wyjaśniać, czym różni się atom od cząsteczki;
interpretować zapisy, takie jak np.: , , , ;
interpretować równania reakcji chemicznych.
Symbole chemiczne to międzynarodowe skróty łacińskich nazw pierwiastków chemicznych, składające się z pierwszej litery i czasami kolejnych liter nazwy. Symbole te stosuje się do zapisu substancji prostych, czyli pierwiastków chemicznych, ale również do zapisu wzorów związków chemicznych. Posługujemy się przy tym przede wszystkich wzorami sumarycznymi oraz wzorami elektronowymiwzorami elektronowymi bądź strukturalnymistrukturalnymi.
Interpretując różne zapisy chemiczne, należy pamiętać o kilku regułach:
Pojedynczy symbol pierwiastka interpretujemy jako jeden atom, np.:
– atom wodoru;
– atom sodu;
– atom ołowiu;
– atom tlenu;
– atom azotu.
Jeżeli przed pojedynczym symbolem pierwiastka chemicznego występuje liczba (współczynnik stechiometrycznywspółczynnik stechiometryczny), to jest to liczba atomów tego pierwiastka, np.:
– dwa atomy wodoru;
– pięć atomów potasu;
– trzy atomy chromu;
– dwa atomy helu;
– dziesięć atomów węgla.
Niektóre niemetale w stanie wolnym w przyrodzie występują jako cząsteczki homojądrowe. Są to między innymi: wodór, tlen, azot, fluor, chlor, brom, jod, tlen, siarka oraz fosfor. W równaniach reakcji chemicznych zapisujemy zatem czasami symbol pierwiastka chemicznego wraz z indeksem dolnym (indeksem stechiometrycznymindeksem stechiometrycznym), informującym o liczbie atomów budujących daną cząsteczkę. Powstają wówczas wzory sumarycznewzory sumaryczne cząsteczek, które wskazują, jakie atomy i w jakiej liczbie są zawarte w danej cząsteczce.
Interpretujemy je wówczas następująco:
– (dwuatomowa) cząsteczka wodoru
Jedna (dwuatomowa) cząsteczka wodoru jest zbudowana z dwóch atomów wodoru.– (dwuatomowa) cząsteczka tlenu
Jedna (dwuatomowa) cząsteczka tlenu jest zbudowana z dwóch atomów tlenu.– (dwuatomowa) cząsteczka azotu
Jedna (dwuatomowa) cząsteczka azotu jest zbudowana z dwóch atomów azotu.– (dwuatomowa) cząsteczka fluoru
Jedna (dwuatomowa) cząsteczka fluoru jest zbudowana z dwóch atomów fluoru.– (dwuatomowa) cząsteczka chloru
Jedna (dwuatomowa) cząsteczka chloru jest zbudowana z dwóch atomów chloru.– (dwuatomowa) cząsteczka bromu
Jedna (dwuatomowa) cząsteczka bromu jest zbudowana z dwóch atomów bromu.– (dwuatomowa) cząsteczka jodu
Jedna (dwuatomowa) cząsteczka jodu jest zbudowana z dwóch atomów jodu.– (ośmioatomowa) cząsteczka siarki
Jedna (ośmioatomowa) cząsteczka siarki jest zbudowana z ośmiu atomów siarki.– (czteroatomowa) cząsteczka fosforu
Jedna (czteroatomowa) cząsteczka fosforu jest zbudowana z czterech atomów fosforu.
W cząsteczkach tych atomy połączone są trwale za pomocą wiązań kowalencyjnych, co można przedstawić, używając wzorów strukturalnych oraz elektronowych (uwzględniających niewiążące pary elektronowe).
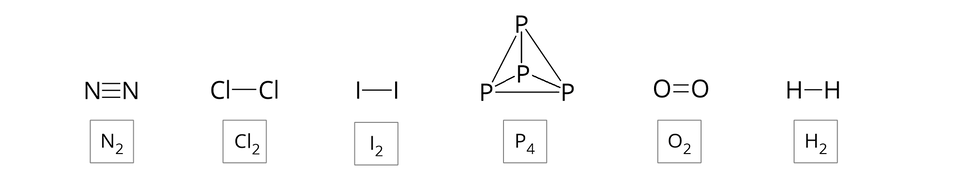
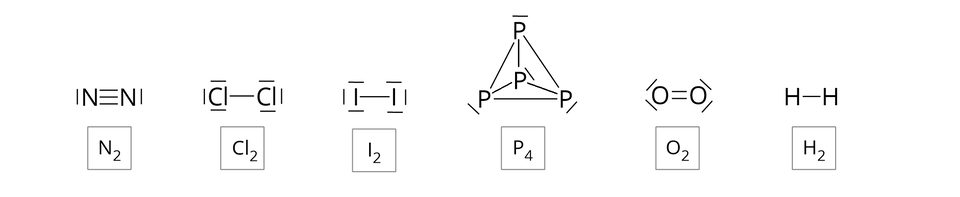
Jeżeli przed wzorem sumarycznym danej cząsteczki występuje liczba, to zapis interpretujemy następująco:
– trzy (dwuatomowe) cząsteczki chloru;
– dwie (czteroatomowe) cząsteczki fosforu;
– cztery (dwuatomowe) cząsteczki wodoru.
We wzorach sumarycznych związków chemicznych liczba atomów każdego pierwiastka jest zapisana jako indeks dolny. Gdy występuje tylko jeden atom danego pierwiastka, indeks dolny jest pomijany.
W jaki sposób interpretujemy wzory sumaryczne kowalencyjnych związków chemicznych?
Kowalencyjne związki chemiczne, czyli takie, w których pomiędzy atomami występują wyłącznie wiązania kowalencyjne, tworzą cząsteczki. Należą do nich przede wszystkim kwasy, wodorki niemetali oraz tlenki niemetali, np.:
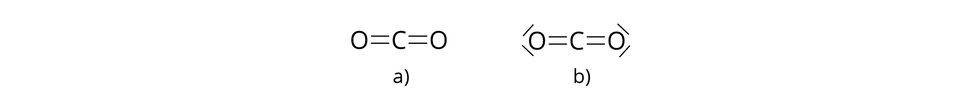
– cząsteczka tlenku węgla()
Jedna cząsteczka tlenku węgla() składa się z jednego atomu węgla i dwóch atomów tlenu, połączonych za pomocą wiązań kowalencyjnych.
Uwaga! Pomimo tego, że tlen w przyrodzie występuje jako cząsteczka , złożona z dwóch atomów tlenu, połączonych za pomocą wiązań kowalencyjnych, to w cząsteczce tlenku węgla() nie występuje takie połączenie. Atomy tlenu połączone są wiązaniami kowalencyjnymi z atomem węgla.
– cząsteczka kwasu siarkowego()
Jedna cząsteczka kwasu siarkowego() jest złożona z dwóch atomów wodoru, jednego atomu siarki i czterech atomów tlenu, połączonych za pomocą wiązań kowalencyjnych.
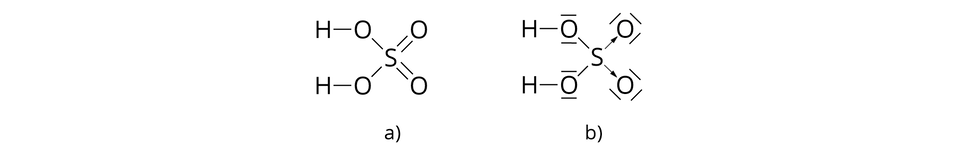
*Wiązanie oznaczone strzałką to wiązanie donorowo–akceptorowe, czyli koordynacyjne, o którym dowiesz się więcej w dalszych etapach nauki.
– cząsteczka bromowodoru
Jedna cząsteczka bromowodoru jest złożona z jednego atomu wodoru i jednego atomu bromu, połączonych za pomocą wiązania kowalencyjnego.

– cząsteczka kwasu azotowego()
Jedna cząsteczka kwasu azotowego() jest złożona z jednego atomu wodoru, jednego atomu azotu i dwóch atomów tlenu.
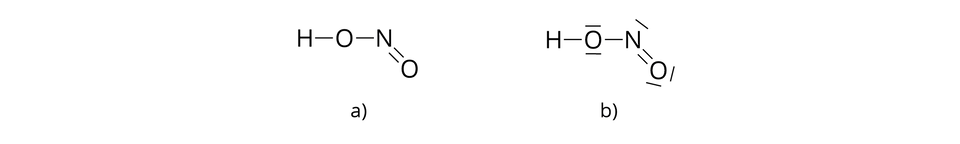
– cząsteczka amoniaku
Jedna cząsteczka amoniaku jest złożona z jednego atomu azotu i trzech atomów wodoru, połączonych za pomocą wiązań kowalencyjnych.
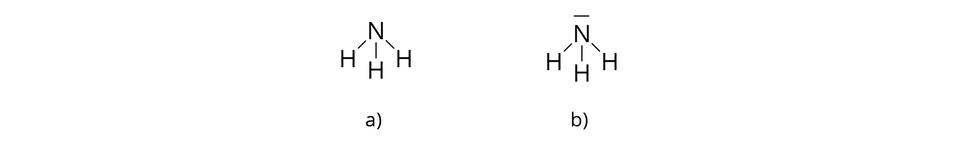
Jeżeli przed daną cząsteczką występuje liczba (współczynnik stechiometryczny), to interpretujemy zapis następująco:
– dwie cząsteczki kwasu fosforowego(),
– trzy cząsteczki tlenku siarki(),
– cztery cząsteczki wody,
– pięć cząsteczek kwasu metanowego.
Liczba atomów wodoru:1. jeden, 2. osiem, 3. trzy, 4. dwa, 5. sześć, 6. dwanaście, 7. cztery
W jaki sposób interpretujemy wzory sumaryczne jonowych związków chemicznych?
Jonowe związki chemiczne nie tworzą cząsteczek, lecz stanowią zbiory jonów, które są związane za pomocą wiązań jonowych. Ułożone naprzemiennie jony tworzą uporządkowane struktury krystaliczne. Wzór sumaryczny związku jonowego przedstawia zatem najmniejszy zbiór powtarzających się jonów w krysztale.
Do jonowych związków chemicznych należy między innymi większość soli, tlenków metali i wodorotlenków. W jaki sposób zatem interpretować wzory sumaryczne związków jonowych?
– zbiór jonów, w którym na jeden kation sodu () przypada jeden anion bromkowy ()
– zbiór jonów, w którym na dwa kationy potasu () przypada jeden anion siarczanowy() ()
– zbiór jonów, w którym na jeden kation wapnia () przypada jeden anion tlenkowy ()
– zbiór jonów, w którym na dwa kationy litu () przypada jeden anion tlenkowy ()
– zbiór jonów, w którym na jeden kation magnezu () przypadają dwa aniony wodorotlenkowe ()
– dwa zbiory jonów, w których na jeden kation sodu () przypada jeden anion wodorotlenkowy ()
– sześć zbiorów jonów składających się z trzech kationów
wapnia () i dwóch anionów fosforanowych() () lub zbiór jonów złożony z osiemnastu kationów wapnia () i dwunastu anionów fosforanowych()
()
dwa A l indeks dolny, dwa, koniec indeksu dolnego, nawias, S O indeks dolny, cztery, koniec indeksu dolnego, zamknięcie nawiasu, indeks dolny, trzy, koniec indeksu dolnego
Liczba anionów siarczanowych(sześć):1. jeden, 2. cztery, 3. sześć, 4. osiem, 5. dwanaście, 6. dwa, 7. trzy
Ponieważ związki jonowe nie tworzą cząsteczek, lecz zbiory jonów – kationów i anionów, to ma to również odzwierciedlenie we wzorach elektronowych. Wiązanie jonowe powstaje, gdy jeden z atomów (atom metalu) oddaje elektrony walencyjne drugiemu atomowi (atomowi niemetalu). Oba atomy uzyskują wówczas trwałe konfiguracje elektronowe najbliższych gazów szlachetnych. Atom, który oddał elektrony walencyjne, staje się kationem, a atom, który je przyjął, staje się anionem. Poniżej przedstawiono wzory elektronowe wybranych związków jonowych.
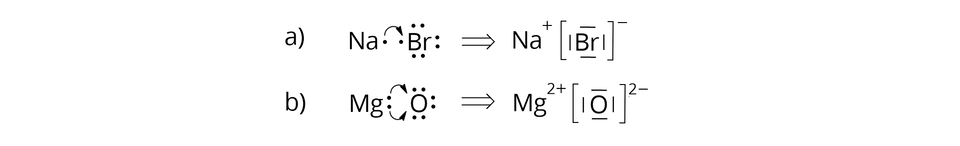
W jaki sposób interpretujemy równania reakcji chemicznych? Wszystkie powyżej wymienione reguły stosujemy również do interpretacji równań reakcji chemicznych, np.:
Jeden atom węgla reaguje z jedną cząsteczką tlenu i powstaje jedna cząsteczka tlenku węgla().
Jedna cząsteczka azotu reaguje z trzema cząsteczkami wodoru i powstają dwie cząsteczki amoniaku.
Dwie cząsteczki jodowodoru rozkładają się i powstaje jedna cząsteczka wodoru i jedna cząsteczka jodu.
W obliczeniach stechiometrycznych najczęściej posługujemy się interpretacją molową równań reakcji. Mol jest jednostką liczności materii – jedną z siedmiu podstawowych wielkości w układzie , podobnie jak masa, długość czy czas. Liczność materii jest miarą liczby drobin zawartych w materii (w przypadku związków o budowie kowalencyjnej) lub jednostek formalnych (w przypadku substancji jonowych). Współczynniki stechiometryczne w równaniach reakcji odpowiadają liczbie moli. Zatem powyższe równania reakcji chemicznych możemy również zinterpretować następująco:
Dwa mole magnezu reagują z jednym molem tlenku węgla() i powstają dwa mole tlenku magnezu i jeden mol węgla.
Jeden mol kwasu siarkowego() reaguje z dwoma molami wodorotlenku sodu i powstaje jeden mol siarczanu() sodu oraz dwa mole wody.
Jeden mol węgla reaguje z jednym molem tlenu i powstaje jeden mol tlenku
węgla().
Jeden mol azotu reaguje z trzema molami wodoru i powstają dwa mole amoniaku.
Dwa mole jodowodoru rozkładają się i powstaje jeden mol wodoru i jeden mol jodu.
Dwa mole magnezu reagują z jednym molem tlenku węgla() i powstają dwa mole tlenku magnezu oraz jeden węgla.
Jeden mol kwasu siarkowego() reaguje z dwoma molami wodorotlenku sodu i powstaje jeden mol siarczanu() sodu oraz dwa mole wody.
Program uczący
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D6vj28LaX
Interpretacja zapisów chemicznych
Symbolika chemiczna
Przeanalizuj poniższe zapisy chemiczne i zobacz, co oznaczają poszczególne jego elementy:
1. Jeżeli widzisz zapisany symbol pierwiastka, to w ujęciu mikroświata oznacza to, że masz do czynienia z pojedynczym atomem danego pierwiastka. W tym przypadku taki zapis zinterpretujemy jako “jeden atom np. tlenu”.
2. Jeżeli w prawym indeksie dolnym przy symbolu pierwiastka chemicznego pojawia się liczba, mamy do czynienia z cząsteczką pierwiastka. Wartość tej liczby określa ilość atomów danego pierwiastka w opisanej cząsteczce. Liczba ta nazywana jest indeksem stechiometrycznym np.
Powyższy zapis możemy zinterpretować jako “jedna cząsteczka tlenu. Cząsteczka pierwiastka może się składać zarówno z dwóch lub więcej atomów tego samego pierwiastka.
3. Jeżeli w zapisie występują symbole dwóch lub więcej pierwiastków mamy do czynienia ze związkiem chemicznym. We wzorze mogą występować również indeksy stechiometryczne, które wskazują jaki jest stosunek atomów poszczególnych pierwiastków w cząsteczce związku chemicznego. Dobrym przykłdem będzie zapis
który możemy zinterpretować jako “jedna cząsteczka tlenku siarki(IV)”, dodatkowo możemy określić, że ta cząsteczka składa się z jednego atomu siarki i dwóch atomów tlenu.
4. Liczba znajdująca się przed wzorem związku chemicznego to współczynnik stechiometryczny. Mówi nam o tym z jaką liczbą cząsteczek mamy do czynienia. Przytoczmy tu przykład
Powyższy zapis interpretujemy jako “trzy cząsteczki tlenku siarki(IV)”. Dodatkowo możemy zobaczyć, że każda z cząsteczek zbudowana jest z jednego atomu siarki oraz dwóch atomów tlenu.
5. Niektóre związki chemiczne nie tworzą cząsteczek, a w stałym stanie skupienia tworzą kryształy jonowe - związki te określamy mianem związków jonowych. Wzór sumaryczny w przypadku tego typu związków nie określa liczby atomów budujących związek, lecz stosunek w jakim jony go tworzące występują w krysztale tego związku chemicznego. W tym przypadku atomy metali tworzą jony o ładunku dodatnim - kationy, a atomy niemetali, lub bardziej złożone reszty kwasowe tworzą jony o ładunku ujemnym - aniony. Powyższy zapis
możemy interpretować jako “zbiór jonów, w którym na jeden kation wapnia przypadają dwa aniony fluorkowe”/”kryształ jonowy, w którym na jeden kation wapnia przypadają dwa aniony fluorkowe”. Związki jonowe to takie, w których różnica elektroujemności pomiędzy pierwiastkami je tworzącymi zwykle jest większa niż 1,7. Zazwyczaj są to związki metali 1. i 2. grupy układu okresowego z niemetalami.
6. Jeżeli za symbolem pierwiastka lub drobiny składającej się z więcej niż jednego atomu w indeksie górnym znajduje się symbol “+”, to mamy do czynienia z jonem o ładunku dodatnim, czyli kationem. Przed znakiem „+” dodatkowo może znajdować się liczba, tak jak ma to miejsce w zaprezentowanym przykładzie, oznaczająca wartość ładunku kationu.
Zapis zaprezentowanego przykładu możemy zinterpretować jako “jeden dwudodatni kation wapnia”.
7. Jeżeli za symbolem pierwiastka lub drobiny składającej się z więcej niż jednego atomu w indeksie górnym znajduje się symbol “-”, to mamy do czynienia z jonem o ładunku ujemnym, czyli anionem. Przed znakiem „-” dodatkowo może znajdować się liczba oznaczająca wartość ładunku anionu.
Zapis zaprezentowanego przykładu możemy zinterpretować jako “jeden jednoujemny anion fluorkowy”.
Interpretacja równań reakcji chemicznych
Przeanalizuj poniższe zapisy chemiczne i zobacz, co oznaczają poszczególne jego elementy.
1. Podobnie jak w zapisach pojedynczych drobin, w zapisach równań reakcji również występują indeksy oraz współczynniki stechiometryczne. Zarówno indeksy jak i współczynniki stechiometryczne są istotne dla poprawnego zbilansowania równania reakcji, jednak do interpretacji zapisu równania reakcji znacznie ważniejsze są współczynniki stechiometryczne, ponieważ mówią nam ile drobin, bądź moli drobin, bierze udział w reakcji oraz ile ich powstaje w jej przebiegu.
Przykładowo powyższy zapis możemy interpretować na dwa następujące sposoby: Jedna cząsteczka wodoru reaguje z jedną cząsteczką chloru i powstają dwie cząsteczki chlorowodoru.
Jeden mol wodoru reaguje z jednym molem chloru i powstają dwa mole chlorowodoru.
Interpretacja molowa jest znacznie bardziej praktyczna, gdyż w laboratorium chemicznym czy też życiu codziennym rzadko kiedy mamy do czynienia z pojedynczymi cząsteczkami, a ich zbiorami.
2. Innym przykładem składającym się z substancji i produktów reakcji jest
Substancje znajdujące się po lewej stronie równania reakcji to substraty, z kolei te, znajdujące się po prawej stronie równania reakcji to produkty. W powyższym równaniu reakcji występują dwa substraty (wodorotlenek wapnia i kwas chlorowodorowy) oraz dwa produkty (chlorek wapnia i woda), jednakże ich liczba może być inna.
3. W równaniach reakcji mogą występować dodatkowe oznaczenia. W przypadku gdy nad strzałką znajduje się litera T oznacza to, że reakcja zachodzi w podwyższonej temperaturze. Nad strzałką mogą być wypisane również inne warunki takie jak ciśnienie i obecność światła, a także inne związki chemiczne niezbędne do przeprowadzenia reakcji, ale nie biorące w niej bezpośredniego udziału - katalizatory.
Czasami w zapisie równania reakcji możemy znaleźć również literowe oznaczenia w nawiasach, znajdujące się po wzorze związku lub pierwiastka chemicznego. W zależności od oznaczenia, świadczy to o tym, w jakim stanie skupienia występuje dany reagent. Litera “g” oznacza reagenty gazowe, litera “c” reagenty ciekłe, a litera “s” reagenty będące ciałami stałymi. Czasami, jeżeli substancja może występować w formie czystej lub w formie roztworu wodnego, spotykamy również oznaczenie “aq”, które oznacza wodny roztwór danego związku chemicznego. Poniżej zamieszczono przykład równiania reakcji z dodaną literą t.
Słownik
liczba umieszczana u dołu z prawej strony symbolu pierwiastka we wzorze chemicznym substancji; jest ona równa liczbie atomów tego pierwiastka w cząsteczce lub w najmniejszym zbiorze powtarzających się jonów w krysztale (tak zwanej jednostce formalnej)
liczba zapisywana przed symbolem lub wzorem chemicznym, która określa liczbę atomów, cząsteczek lub najmniejszych zbiorów powtarzających się jonów w krysztale
ilościowy zapis składu cząsteczek pierwiastków i związków chemicznych za pomocą symboli chemicznych
zapis wskazujący, w jaki sposób łączą się ze sobą atomy tworzące dany związek chemiczny; wzór elektronowy uwzględnia niewiążące pary elektronowe
ilościowy i jakościowy zapis składu cząsteczek pierwiastków i związków chemicznych za pomocą symboli chemicznych oraz wiązań chemicznych,
Ćwiczenia
Liczba anionów fosforanowych(pięć): 1. dwa, 2. trzy, 3. dwanaście, 4. dziewięć, 5. cztery, 6. osiem, 7. jeden, 8. sześć
liczba atomów wodoru 1. jedenaście, 2. dwadzieścia dwa, 3. dziewięćdziesiąt, 4. dwanaście, 5. czterdzieści cztery, 6. dwa, 7. dwadzieścia cztery, 8. czterdzieści pięć
liczba atomów tlenu 1. jedenaście, 2. dwadzieścia dwa, 3. dziewięćdziesiąt, 4. dwanaście, 5. czterdzieści cztery, 6. dwa, 7. dwadzieścia cztery, 8. czterdzieści pięć
sumaryczna liczba atomów 1. jedenaście, 2. dwadzieścia dwa, 3. dziewięćdziesiąt, 4. dwanaście, 5. czterdzieści cztery, 6. dwa, 7. dwadzieścia cztery, 8. czterdzieści pięć
Bibliografia
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy siódmej szkoły podstawowej, Warszawa 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy siódmej szkoły podstawowej, Mac Edukacja 2020.
Encyklopedia PWN