Jak piszemy konfiguracje elektronowe?
Czym jest konfiguracja podpowłokowa elektronowa?
Podpowłokowa konfiguracja elektronowa przedstawia sposób zapełniania poszczególnych podpowłok przez elektrony. Aby posłużyć się tą metodą, stosuje się zapis typu , w którym pierwsza liczba oznacza wartość głównej liczby kwantowej (numer powłoki), litera (, , lub ) jest symbolem podpowłoki i umożliwia dokładne określenie pobocznej liczby kwantowej, natomiast liczba w górnym indeksie oznacza liczbę elektronów na danej podpowłoce.
Porównajmy dwa sposoby zapisu konfiguracji elektronowej dla atomu boru w stanie podstawowym.

Konfiguracje elektronowe atomów będą się przedstawiać następująco:
zapis podpowłokowy: : ; zapis powłokowy: ;
zapis podpowłokowy: : ; zapis powłokowy: ;
zapis podpowłokowy: : ; zapis powłokowy: .
Stosuje się również tzw. zapis skrócony konfiguracji podpowłokowej, który wykorzystuje w zapisie symbol gazu szlachetnego poprzedzającego dany pierwiastek w układzie okresowym. Np. dla litu moglibyśmy zapisać:
: .
Podobnie, bazując na konfiguracji elektronowej poprzedzającego gazu szlachetnego (znajdującego się w okresie powyżej), można podać skrócony zapis konfiguracji elektronowej atomu każdego pierwiastka.
Skrócony zapis konfiguracji elektronowej atomu pierwiastka polega na podaniu symbolu poprzedzającego go helowca oraz dopisaniu elektronów, które nie występują w jego atomie.
Klatkowy zapis konfiguracji elektronowej – tzw. zapis graficzny konfiguracji elektronowej
Najbardziej szczegółowy opis przedstawiania konfiguracji elektronowej prezentuje rozmieszczenie elektronów na poziomach orbitalnych. Opis polega na rysowaniu elektronów w kratkach – każda kratka symbolizuje jeden poziom orbitalny. Podpowłoki , , i obejmują odpowiednio , , , poziomów orbitalnych, więc składają się odpowiednio z jednej, trzech, pięciu lub siedmiu połączonych ze sobą kratek, co przedstawiono na poniższym schemacie.

Zwróć uwagę, że każda „kratka” – poziom orbitalny – może pomieścić maks. dwa elektrony. Sposób przypisania wartości magnetycznej liczby kwantowej do poszczególnych kratek, jaki przedstawiono na powyższym schemacie (a więc od najmniejszej wartości dla lewej kratki do największej wartości dla kratki prawej), jest tylko umowny.
Elektrony będą przedstawiane jako pionowe strzałki o zwrocie w górę lub w dół. Odpowiada to zwrotowi wektora spinu, czyli dodatniej lub ujemnej wartości magnetycznej spinowej liczby kwantowej.
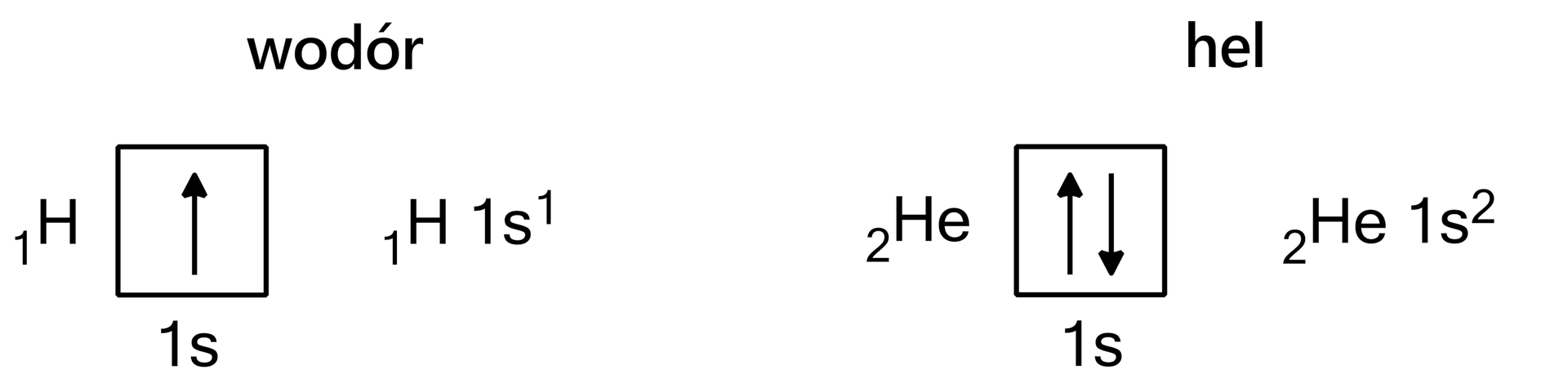
Przypisując elektrony do orbitali, musimy przestrzegać trzech zasad: zasada rozbudowy powłok, zakazu Pauliego i reguły Hunda.
Zakaz Pauliego
Trzy liczby kwantowe (, , ) opisują energię, rozmiar, kształt i orientację przestrzenną orbitalu. Czwarta liczba kwantowa określa dwa stany spinowe. Dowody eksperymentalne sugerują, że elektrony obracają się wokół swoich osi, gdy poruszają się we wnętrzu atomów. Elektron może wirować w jednym z dwóch kierunków, w każdym wytwarzając pole magnetyczne.
Prędkość wirowania elektronów w danym atomie jest taka sama, niezależnie od kierunku, w którym atom obraca się wokół własnej osi. Dlatego właśnie spinowa liczba kwantowa () przyjmuje zawsze wartość . Magnetyczno–spinowa liczba kwantowa () określa kierunek, w którym wiruje elektron. Ma tylko dwie możliwe wartości: lub , bo wirowanie wokół własnej osi może odbywać się tylko w dwóch kierunkach.
W roku szwajcarski fizyk, pochodzenia austriackiego, Wolfgang Pauli zaproponował, że jeden poziom orbitalny mogą zajmować tylko dwa elektrony o przeciwnym kierunku wirowania – a więc o przeciwnej wartości magnetycznej spinowej liczby kwantowej. Ów wniosek stał się znany jako zakaz Pauliego. Polega on na ograniczeniu całkowitej liczby elektronów, które mogą zajmować dowolny orbital. Oznacza to, że orbital może mieć maks. dwa elektrony, a ich spiny muszą być sparowane. A są sparowane, kiedy są ustawione w przeciwnych kierunkach. Orbital może również mieć tylko jeden elektron o dowolnym kierunku wirowania i tak samo może nie mieć żadnych elektronów.
Elektron niesparowany – elektron znajdujący się na poziomie orbitalnym, na którym nie ma innego elektronu.
Elektrony sparowane – dwa elektrony o przeciwnej orientacji spinów, należące do tego samego poziomu orbitalnego.
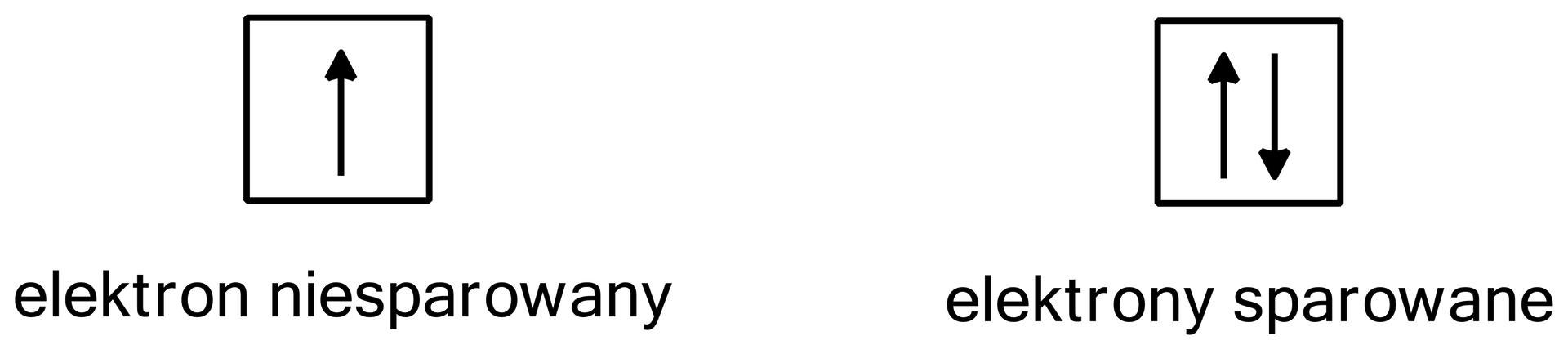
Innym sposobem stwierdzenia zakazu Pauliego jest to, że żadne dwa elektrony w atomie nie mają tych samych wartości wszystkich liczb kwantowych. Ta ważna teza oznacza, że każdy elektron w atomie ma swój unikalny zestaw czterech liczb kwantowych.

Zasada rozbudowy powłok
W ustalaniu kolejności obsadzania powłok, decydującą rolę odgrywa zasada rozbudowy powłok (zasada minimum energii). Elektrony obsadzają powłoki i orbitale, zaczynając od stanu o najniższej energii. Nie pozostawiają żadnych wolnych miejsc. Kolejność jest następująca:

Wyjaśnieniem tego, dość dziwnego na pierwszy rzut oka, sposobu zapełniania podpowłok jest poniższy diagram. Zauważ, że np. energia orbitali jest nieco wyższa niż energia orbitali . Dzięki temu elektrony w pierwszej kolejności obsadzają orbital , a następnie dopiero .

Reguła Hunda
Reguła ta rozwiązuje wiele dylematów podczas rozpisywania konfiguracji elektronowej. Według niej, w danej podpowłoce powinna istnieć możliwie największa liczba niesparowanych elektronów. Te, które obsadzają poziomy orbitalne tej samej podpowłoki, powinny mieć jednakową orientację spinu. Do sparowania elektronów dochodzi dopiero wtedy, gdy elektrony niesparowane zajmą wszystkie poziomy orbitalne danej powłoki.
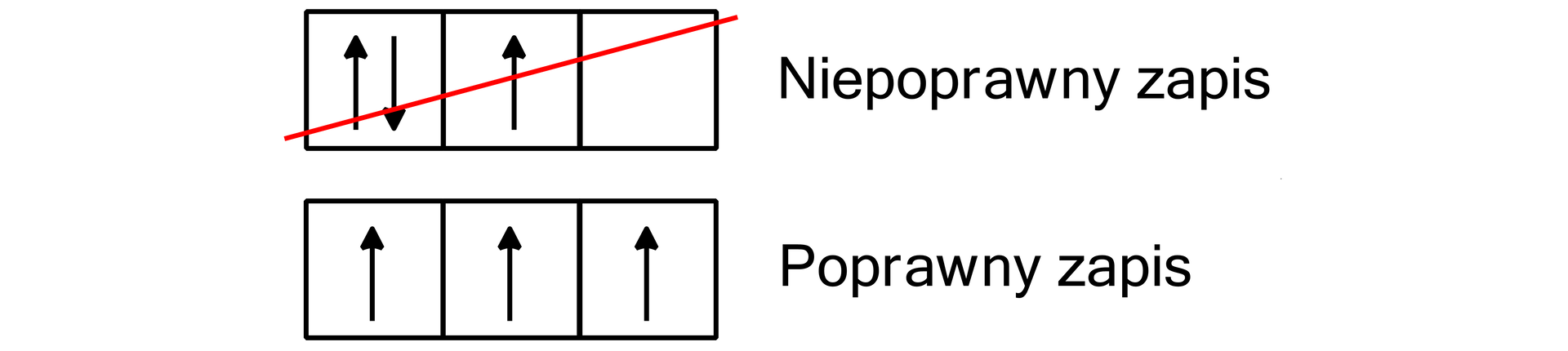
Zapoznaj się z animacją dotyczącą rozmieszczania elektronów na orbitalach i rozwiąż ćwiczenia.

Film dostępny pod adresem /preview/resource/RgTYsHToMZOwa
Film wyjaśnia, na czym polega reguła Hunda i zakaz Pauliego. Zawiera informacje związane z kolejnością zapełniania elektronami podpowłok.
Mając powyższe zasady na uwadze, można przystąpić do rozpisywania konfiguracji elektronowej.
Przedstaw podpowłokową konfigurację elektronową atomu azotu w stanie podstawowym.
Przedstaw pełną podpowłokową konfigurację elektronową oraz skróconą podpowłokową konfigurację elektronową (zawierającą rdzeń gazu szlachetnego) atomu jodu w stanie podstawowym.
Zapisz pełną podpowłokową konfigurację elektronową dla atomu wapnia.
Ćwiczenie zapisu konfiguracji elektronowej
Aplikacja przedstawia zapisywanie konfiguracji elektronowej w różnych formach przy wykorzystaniu układu okresowego.
Pierwszym elementem aplikacji jest konfiguracja elektronowa atomów. Część ta skupia się na zrozumieniu, jak elektrony są rozmieszczone w atomach. Można wybrać typ zapisu konfiguracji elektronowej: zapis pełny podpowłokowy, zapis pełny powłokowy, zapis skrócony (z rdzeniem gazu szlachetnego) lub zapis graficzny (klatkowy).
1. Zapis pełny podpowłokowy.
W pierwszym kroku z układu okresowego pierwiastków chemicznych wybiera się atom, którego konfigurację elektronową chce się zapisać. Do wyboru jest dowolny pierwiastek z pierwszych trzydziestu ośmiu pierwiastków układu okresowego.
Wybrany pierwiastek: Beryl
W drugim kroku należy stworzyć pełny podpowłokowy zapis dla wybranego jonu. Pamiętając o maksymalnej liczbie elektronów na powłokach (s – 2, p – 6, d – 10, f – 14) oraz zgodności liczby elektronów z liczbą atomową jonu.
Poprawny zapis:
Przykłady:
Wybrany pierwiastek: Potas
Poprawny zapis:Wybrany pierwiastek: Żelazo
Poprawny zapis:Wybrany pierwiastek: Chlor
Poprawny zapis:
2. Zapis pełny powłokowy.
W pierwszym kroku z układu okresowego pierwiastków chemicznych wybiera się atom, którego konfigurację elektronową chce się zapisać. Do wyboru jest dowolny pierwiastek z pierwszych 38 pierwiastków układu okresowego.
Wybrany pierwiastek: Beryl
W drugim kroku należy zapisać pełną konfigurację powłokową dla wybranego atomu.
Poprawny zapis:
Przykłady:
Wybrany pierwiastek: Potas
Poprawny zapis:Wybrany pierwiastek: Żelazo
Poprawny zapis:Wybrany pierwiastek: Chlor
Poprawny zapis:
3. Zapis skrócony (z rdzeniem gazu szlachetnego).
W pierwszym kroku z układu okresowego pierwiastków chemicznych wybiera się atom, którego konfigurację elektronową chce się zapisać. Do wyboru jest dowolny pierwiastek z pierwszych 38 pierwiastków układu okresowego.
Wybrany pierwiastek: Beryl
W drugim kroku należy stworzyć poprawny zapis skrócony dla wybranego atomu. Pamiętając, żeby poprawnie ustalić zapis skrócony należy wskazać najbliższy gaz szlachetny poprzedzający analizowany pierwiastek w układzie okresowym.
Zapis należy rozpocząć od wyboru jednego spośród dostępnych gazów szlachetnych, są to: , , , . Wybierając symbol odpowiedniego gazu szlachetnego należy pamiętać, że atom tego gazu powinien mieć liczbę atomową równą lub mniejszą od liczby elektronów zawartych w jonie analizowanego pierwiastka.
Poprawny zapis:
Przykłady:
Wybrany pierwiastek: Potas
Poprawny zapis:Wybrany pierwiastek: Żelazo
Poprawny zapis:Wybrany pierwiastek: Chlor
Poprawny zapis:
4. Zapis graficzny (klatkowy).
W pierwszym kroku z układu okresowego pierwiastków chemicznych wybiera się atom, którego konfigurację elektronową chce się zapisać. Do wyboru jest dowolny pierwiastek z pierwszych 38 pierwiastków układu okresowego.
Wybrany pierwiastek: Beryl
W drugim kroku należy stworzyć zapis graficzny (klatkowy).
Poprawny zapis:
Przykłady:
Wybrany pierwiastek: Potas
Poprawny zapis:Wybrany pierwiastek: Żelazo
Poprawny zapis:Wybrany pierwiastek: Chlor
Poprawny zapis:
Drugim elementem aplikacji jest konfiguracja elektronowa jonów. Temat ten jest bardziej zaawansowany, dotyczy tego jak elektrony są rozmieszczone w jonach. W tym przypadku również można wybrać typ zapisu konfiguracji elektronowej: zapis pełny podpowłokowy, zapis pełny powłokowy, zapis skrócony ( z rdzeniem gazu szlachetnego) lub zapis graficzny (klatkowy).
1. Zapis pełny podpowłokowy.
W pierwszym kroku należy wybrać symbol jonu prostego, którego konfiguracja będzie rozpisywana.
Wybrany jon:
Następnie należy zapisać pełną konfigurację podpowłokową dla wybranego jonu.
Poprawny zapis:
Przykłady:
Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:
2. Zapis pełny powłokowy.
W pierwszym kroku należy wybrać symbol jonu prostego, którego konfiguracja będzie rozpisywana.
Wybrany jon: W drugim kroku należy zapisać pełną konfigurację powłokową dla wybranego jonu.
Poprawny zapis:
Przykłady:
Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:
3. Zapis skrócony (z rdzeniem gazu szlachetnego).
W pierwszym kroku należy wybrać symbol jonu prostego, którego konfiguracja będzie rozpisywana.
Wybrany jon:
W drugim kroku należy stworzyć poprawny zapis skrócony dla wybranego jonu. Pamiętając, żeby poprawnie ustalić zapis skrócony należy wskazać najbliższy gaz szlachetny poprzedzający analizowany pierwiastek w układzie okresowym.
Zapis należy rozpocząć od wyboru jednego spośród dostępnych gazów szlachetnych, są to: , , , . Wybierając symbol odpowiedniego gazu szlachetnego należy pamiętać, że atom tego gazu powinien mieć liczbę atomową równą lub mniejszą od liczby elektronów zawartych w jonie analizowanego pierwiastka.
Poprawny zapis:
Przykłady:
Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:
4. Zapis graficzny (klatkowy).
W pierwszym kroku należy wybrać symbol jonu prostego, którego konfiguracja będzie rozpisywana.
Wybrany jon:
W drugim kroku należy stworzyć zapis graficzny (klatkowy).
Poprawny zapis:
Przykłady:
Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:Wybrany jon:
Poprawny zapis:
Konfiguracja elektronowa dla kationów
Sposób, w jaki wyznaczamy konfiguracje elektroniczne dla kationów, jest zasadniczo podobny do sposobu przeznaczonego dla atomów w ich stanie podstawowym. Oznacza to, że przestrzegamy trzech ważnych zasad: zasady rozbudowy powłok, zakazu Pauliego i reguły Hunda. W celu tworzenia kationów lub podnoszenia ładunku kationów, należy usuwać elektrony z ostatniej powłoki elektronowej, w kolejności . Tak wiec najpierw należy usunąć wszystkie elektrony podpowłoki ostatniej powłoki, następnie wszystkie elektrony podpowłoki ostatniej powłoki i wtedy dopiero możemy usunąć elektrony z podpowłoki ostatniej powłoki.
Przykładowo – konfiguracja elektronowa atomu wapnia w stanie podstawowym () wynosi .
Jon wapniowy () ma jednak dwa elektrony mniej. Stąd konfiguracja elektronów dla wynosi .
Konfiguracja elektronowa atomu żelaza w stanie podstawowym wynosi:
: .
Atom żelaza może oddać dwa elektrony z orbitalu .
Konfiguracja elektronowa : .
Atom żelaza może także oddać trzy elektrony – dwa pochodzące z oraz jeden pochodzący z podpowłoki .
Konfiguracja elektronowa : .
W pierwszej kolejności należy usunąć elektrony z , a dopiero później z , ponieważ ostatnią powłokę stanowią elektrony czwartej powłoki, a z podpowłoki trzeciej możemy usuwać elektrony dopiero po zupełnym usunięciu ich z powłoki ostatniej, czyli czwartej.
Zapoznaj się z poniższymi filmami samouczkami, aby poznać reguły oraz sposoby zapisu konfiguracji elektronowej atomów i jonów na przykładzie różnych pierwiastków.
Czym różnią się atomy od jonów – kationów i anionów?
Ustal, jaki jon () w stanie podstawowym ma konfigurację elektronową : .
Dany jest zestaw indywiduów chemicznych: atom chromu (), kation żelaza() (), anion siarczkowy (). Zapisz konfigurację elektronową dla każdego z wymienionych indywiduów w stanie podstawowym, stosując zapis pełny podpowłokowy i zapis graficzny.
Dane są cztery pierwiastki: pierwiastek , pierwiastek , pierwiastek i pierwiastek . Poniżej podano skrócone konfiguracje elektronowe atomów wymienionych pierwiastków w stanie podstawowym:
pierwiastek : : ;
pierwiastek : : ;
pierwiastek : : ;
pierwiastek : : .
W oparciu o powyższe informacje wykonaj polecenia .
Zakaz Pauliego mówi, że w atomie nie mogą istnieć 1. głównej, 2. elektrony, 3. liczb, 4. elektronów, 5. kwantowych, 6. niesparowanych o takich samych wartościach wszystkich liczb 1. głównej, 2. elektrony, 3. liczb, 4. elektronów, 5. kwantowych, 6. niesparowanych. Muszą się różnić przynajmniej jedną wartością.
Zapoznaj się z konfiguracjami elektronowymi atomów danych pierwiastków, a następnie dopasuj je do odpowiedniego miejsca w układzie okresowym pierwiastków.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5MM81PCV
Niektóre pierwiastki charakteryzują się nietypową konfiguracją elektronową, tzw. promocją elektronową. Wymień je, a następnie zapisz ich konfigurację elektronową.




