Efekt energetyczny reakcji
Czym zajmuje się termochemia?
Dział chemii, który bada efekty cieplne towarzyszące reakcjom chemicznym w oparciu o zasady termodynamiki, to termochemiatermochemia. Opisuje zmiany energii zachodzące podczas reakcji chemicznych. Można wtedy zauważyć, że niektóre z reakcji wydzielają dużą ilość energii (np. reakcja magnezu z kwasem solnym), inne z kolei nie zajdą bez dostarczenia określonej jej ilości. Energia wymieniana jest między układem a otoczeniem.
UkładUkład to wyodrębniona część we wszechświecie, która jest przedmiotem badań i obserwacji. Przykładem układu może być szampon w butelce, woda z lodem, balon z gazem lub kolbka, w której zachodzi reakcja. Otoczeniem jest wszystko to, co nie jest układem. Stan układu można opisać za pomocą wielkości fizycznych (np. ciśnienie, temperatura, objętość). Ze względu na sposób wymiany energii przez układ z otoczeniem, można wyróżnić trzy rodzaje układów, które zostały przedstawione na mapie myśli.
Czym jest efekt energetyczny?
Efekt energetyczny towarzyszy każdej reakcji chemicznej. To wielkość charakterystyczna dla danej reakcji. Efekt energetyczny jest definiowany jako ilość energii przekazanej z otoczenia do układu lub z układu do otoczenia. Ze względu na rodzaj efektu energetycznego, reakcje chemiczne dzielą się na dwa rodzaje:
w reakcjach egzoenergetycznych energia jest uwalniana do otoczenia w dowolnej postaci;
w reakcjach endoenergetycznych energia jest pochłaniana z otoczenia.
Do obliczenia przekazanej energii należy wykorzystać zmianę temperatury. Aby to obliczenie wykonać, potrzebna jest znajomość pojemności cieplnej (). Pojemność cieplna jest to ilość ciepła, jaka jest niezbędna do zmiany temperatury ciała o jednostkę temperatury. Korzystając z poniższego wzoru, można obliczyć wartość pojemności cieplnej.
gdzie:
– pojemność cieplna [];
– ciepło dostarczone [];
– zmiana temperatury [].
Oznaczanie ciepła reakcji chemicznych można wykonać doświadczalnie przy pomocy kalorymetrukalorymetru. Jest to izolowane naczynie, napełnione cieczą o wyznaczonej pojemności cieplnej, np. woda, alkohol, amoniak. Budowa prostego kalorymetru została przedstawiona poniżej.
Zapoznaj się z poniższą symulacją i odpowiedz na pytanie: jakie czynniki wpływają na efekt energetyczny reakcji?

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDZS2PLU3
Zaznacz poprawną odpowiedź.
Zaznacz poprawną odpowiedź.
Zaznacz poprawne odpowiedzi.
Jak zmienia się energia podczas reakcji chemicznych?
Aby reakcja chemiczna mogła zajść, cząsteczki substratów (A i B) muszą się ze sobą zderzyć. Energia kinetyczna, związana z ruchem cząsteczek, zaczyna się przekształcać w energię potencjalną, która wzrasta do maksymalnej wartości i prowadzi do utworzenia nietrwałego, przejściowego kompleksu aktywnego (ABIndeks górny **). Posiada on wyższą energię niż suma energii substratów czy suma energii produktów. Zanim substraty przekształcą się w produkty, muszą mieć energię odpowiadającą kompleksowi aktywnemu, bez względu na to, czy jest to reakcja endo-, czy egzoenergetyczna. Różnica między energią potencjalnej substratów a energią potencjalną kompleksu aktywnego polega na energii aktywacji (EIndeks dolny aa) reakcji. Podczas rozpadu kompleksu aktywnego wydziela się energia, która przekształca się w energię kinetyczną cząsteczek produktów (C i D). Warunkiem zajścia reakcji chemicznej jest pokonanie bariery energetycznej. Jej wysokość jest równa energii aktywacji. Różnica energii potencjalnej substratów i produktów równa jest efektowi energetycznemu reakcji. Przebieg opisanej reakcji chemicznej – reakcji egzoenergetycznej – można przedstawić na wykresie zmian energii reakcji, co zostało przedstawione poniżej:
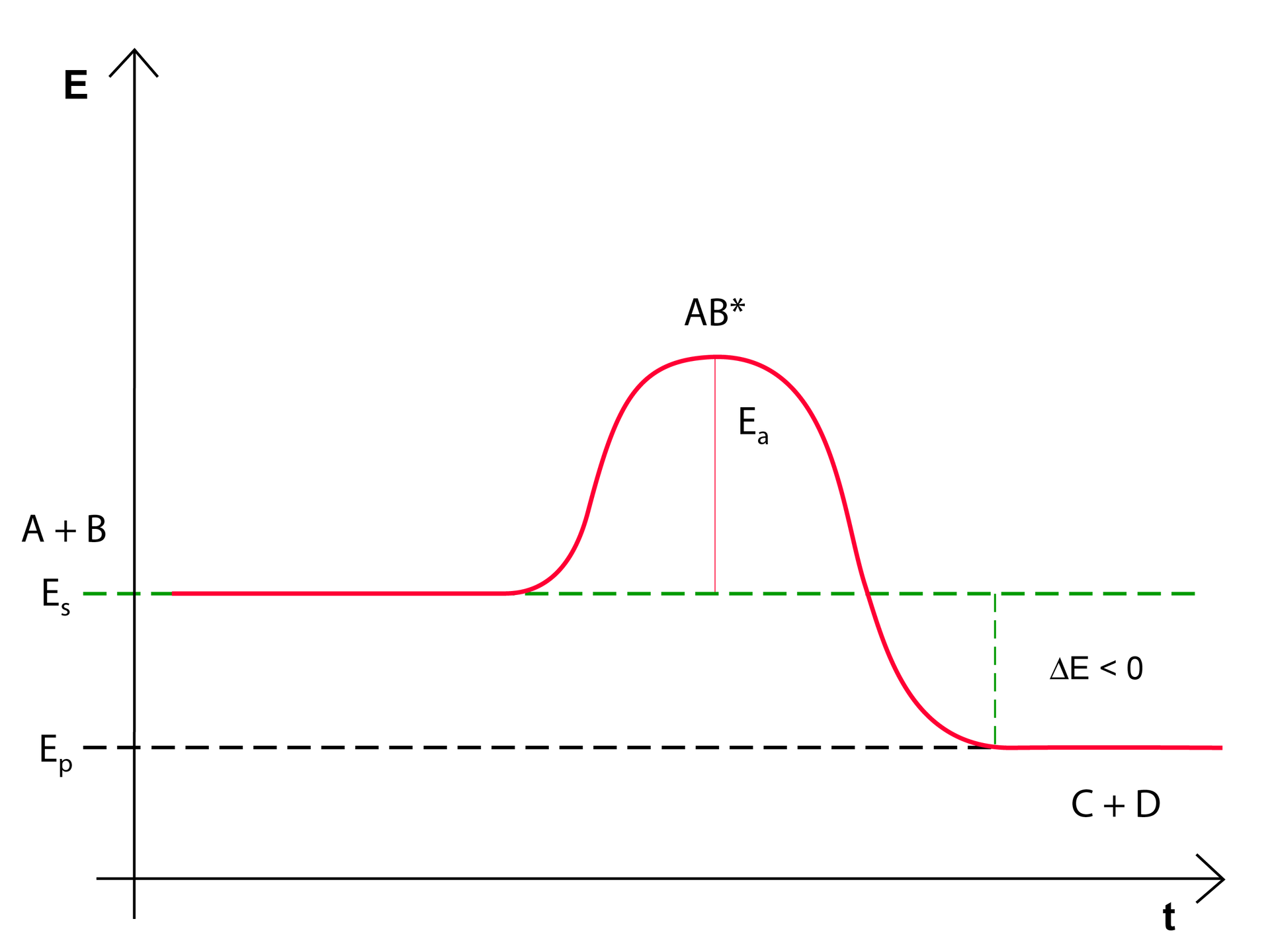
deltaE to energia, która została wydzielona przez układ, zaś EIndeks dolny aa to energia aktywacji, czyli energia potrzebna substratom do przejścia w kompleks aktywny, który jest zdolny do przemiany w produkty. Jeżeli układ wydziela energię do otoczenia, to po reakcji będzie mieć niższą energię niż przed reakcją. Jest to reakcja egzoenergetyczna, czyli reakcja o dodatnim bilansie energetycznym. Energia potencjalna produktów jest mniejsza niż energia potencjalna substratów.
W przypadku reakcji endoenergetycznych, aby reakcja mogła zostać zapoczątkowana, układ pobiera dodatkową energię z otoczenia. Energia aktywacji (EIndeks dolny aa) jest zwykle większa niż całkowita energia reakcji egzoenergetycznej. Poziom energii produktów jest większy niż poziom energii substratów. Poniżej przedstawiono wykres zmian energii układu dla reakcji endoenergetycznej:
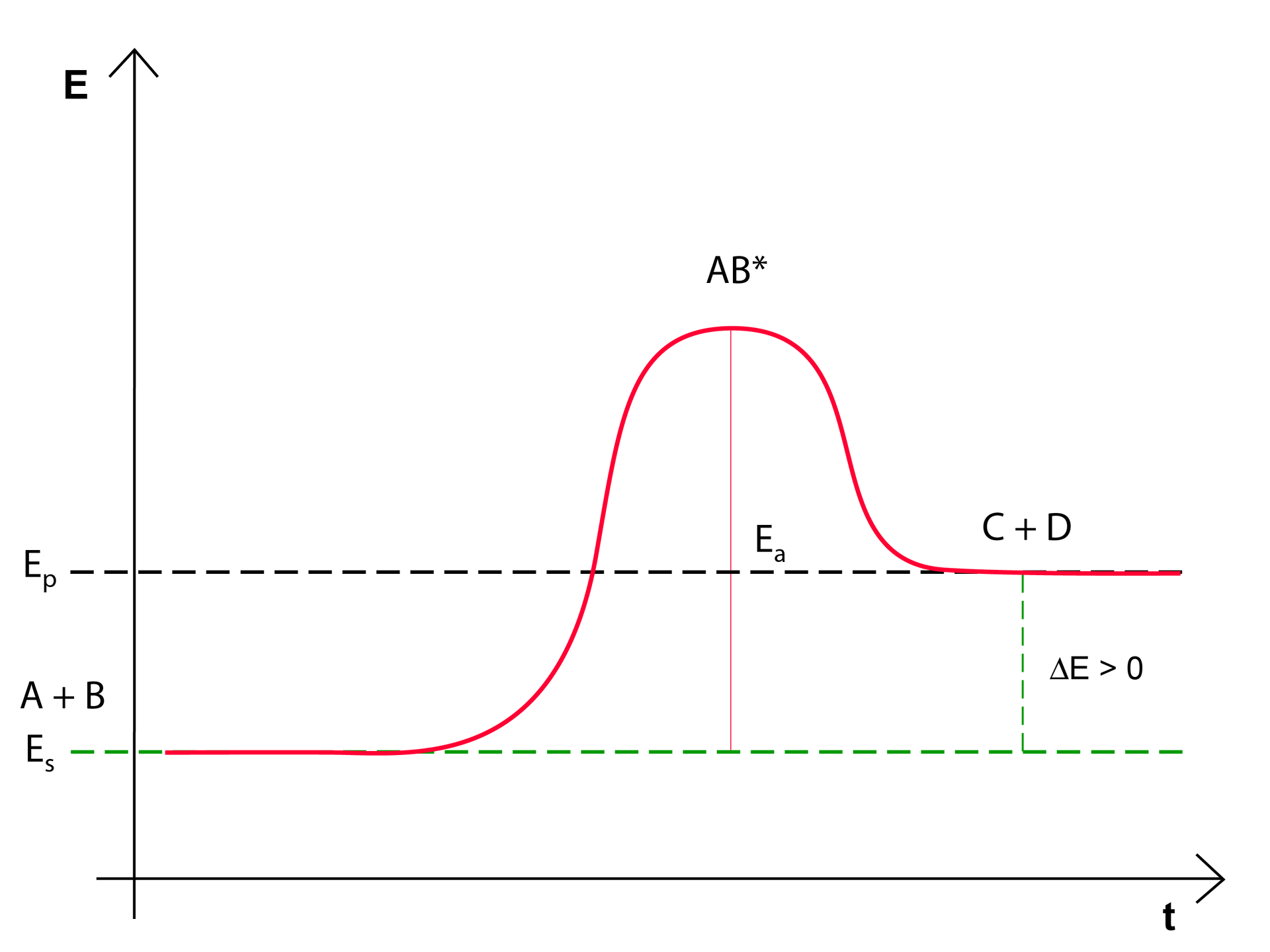
W tym wypadku deltaE jest energią, która została pochłonięta przez układ, a EIndeks dolny aa jest energią aktywacji, potrzebną substratom do przejścia w kompleks aktywny, zdolny do przemiany w produkty. Tym razem, jeśli układ pobierze dodatkową energię z otoczenia, to po reakcji będzie mieć większą energię niż przed nią. Reakcje endoenergetyczne to reakcje o ujemnym bilansie energetycznym. Energia potencjalna produktów jest większa niż energia potencjalna substratów.
Co się zmieni jeśli do reakcji dodamy katalizator?
Katalizator to substancja, która dodana nawet w małych ilościach do reakcji chemicznej zwiększa jej szybkość. Co ważne, katalizator nie jest substratem i nie występuje w równaniu stechiometrycznym. Obniża energię aktywacji, ułatwiając przebieg reakcji. Szybkość zależy od wielkości energii aktywacji. Im wyższa energia aktywacji, tym reakcja zachodzi wolniej. Wykres zmian energii układu przykładowej katalitycznej reakcji egzoenergetycznej został przedstawiony poniżej:
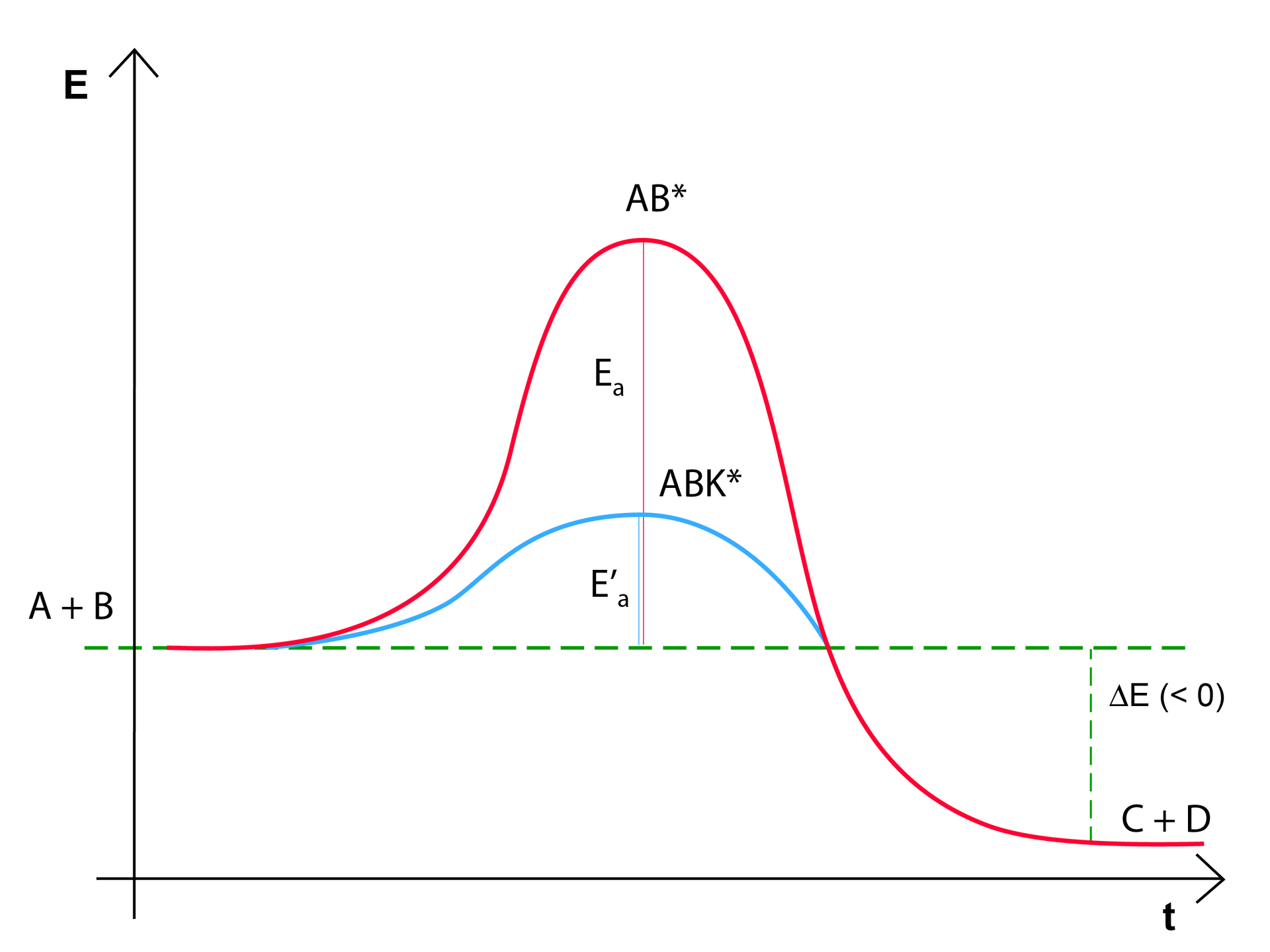
Na wykresie została przedstawiona zmiana energii podczas reakcji chemicznej z udziałem katalizatora. Energia aktywacji reakcji z udziałem katalizatora jest dużo niższa od energii aktywacji reakcji bez udziału katalizatora. Aby zaszła reakcja chemiczna, dwie cząsteczki substratu muszą posiadać sumarycznie większą energię kinetyczną niż wartość energii aktywacji. Im mniejsza energia aktywacji, tym więcej cząsteczek może się ze sobą zderzyć, ponieważ więcej cząsteczek może pokonać barierę energetyczną. Dzięki temu reakcja zachodzi szybciej.
Jakie znasz typy reakcji zmian energii w układzie? Mając do dyspozycji poniższe fotografie, zastanów się, która z nich przedstawia reakcję egzo-, a która endoenergetyczną. Przeglądając grafikę interaktywną poznasz odpowiedzi na te pytania.
Jakie znasz typy reakcji zmian energii w układzie? Mając do dyspozycji opisy fotografii, zastanów się, która z nich dotyczy reakcji egzo-, a która endoenergetycznej.
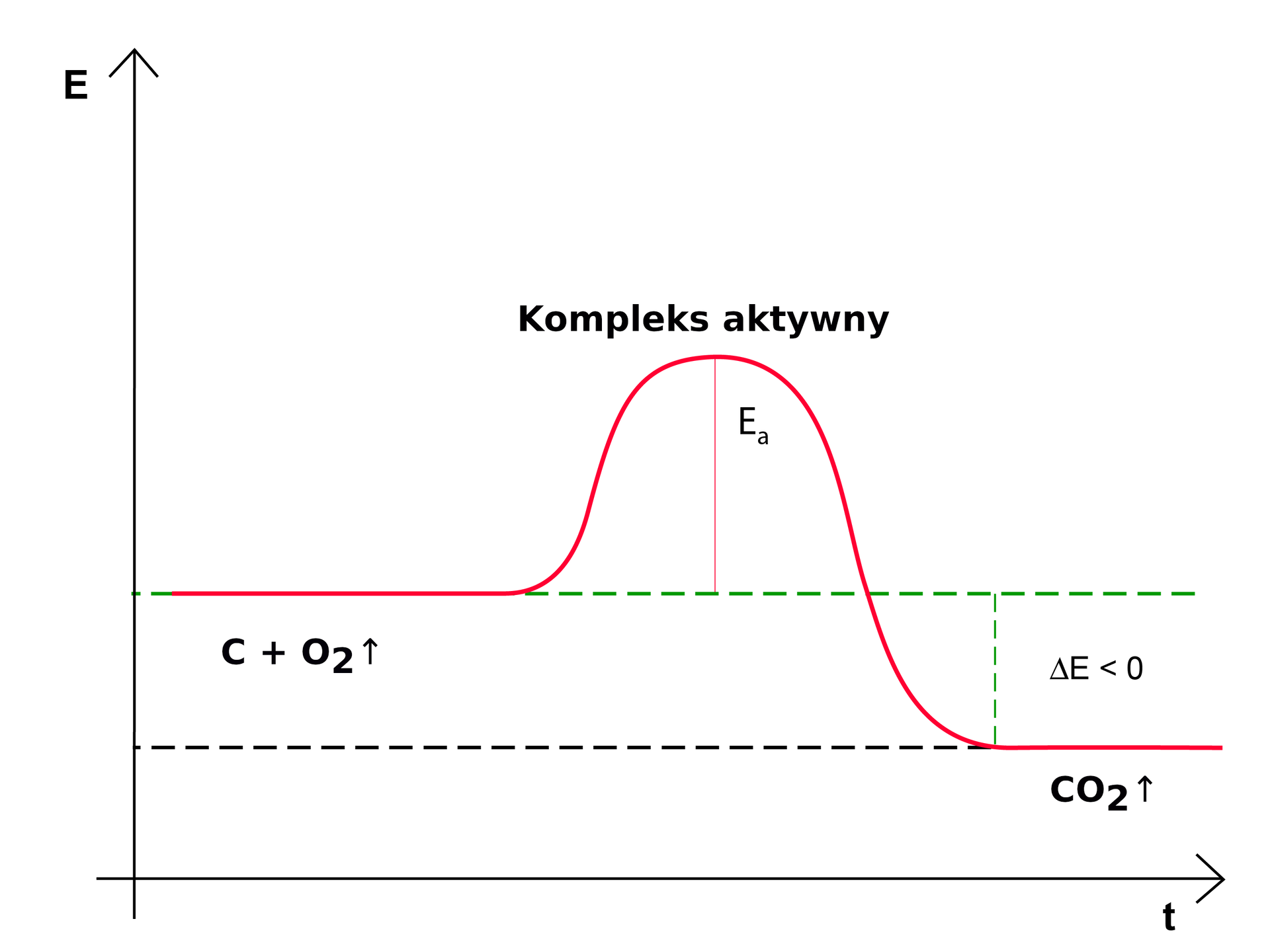
Narysuj wykres energetyczny oraz napisz równanie reakcji chemicznej spalania węgla.
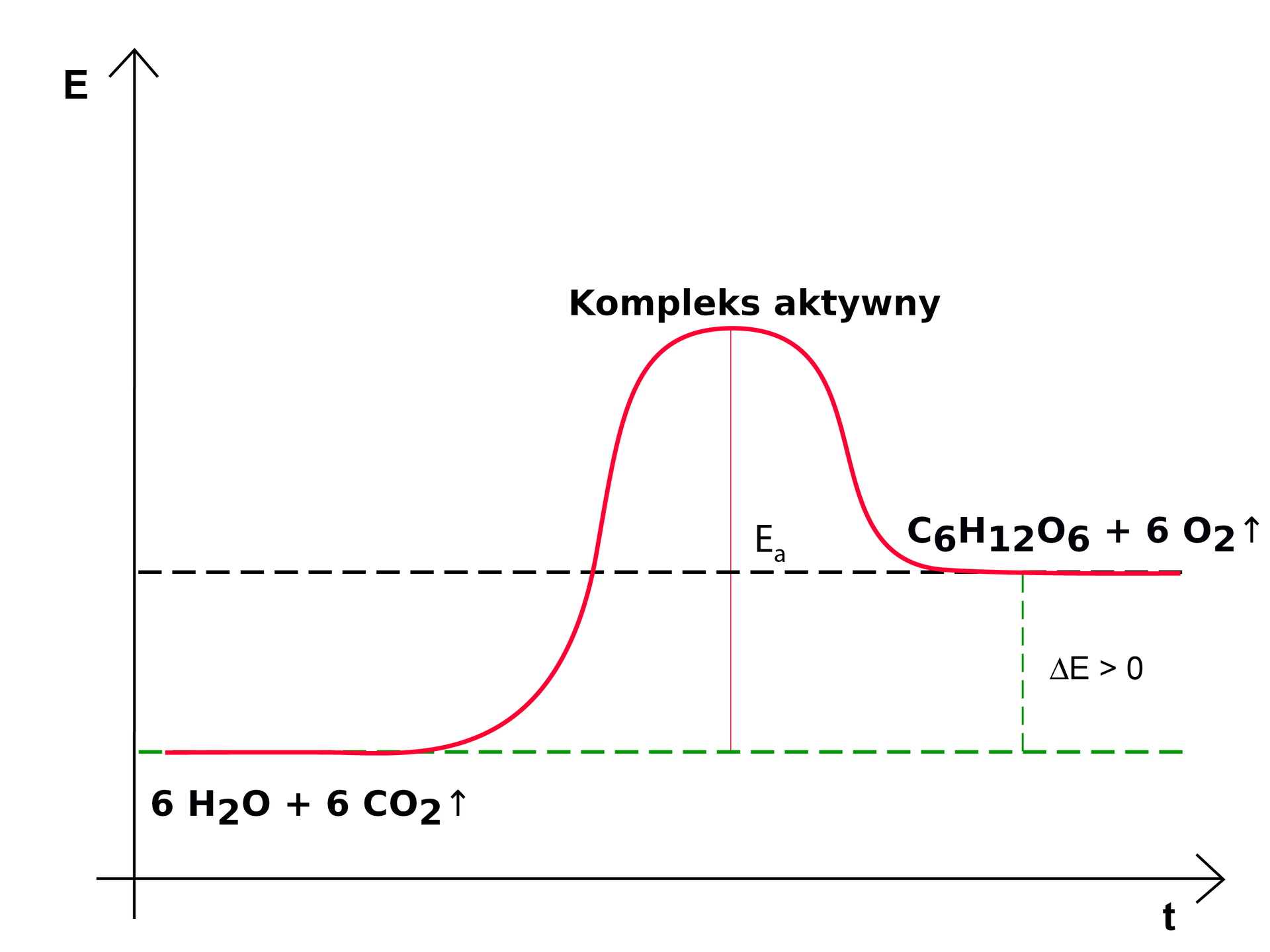
Narysuj wykres energetyczny oraz napisz równanie reakcji chemicznej fotosyntezy.