Jakie oddziaływania występują pomiędzy cząsteczkami?
Cząsteczek nie łączy żadne wiązanie chemiczne, dlatego mogą się przyciągać lub odpychać. Jednak takie oddziaływanie jest dużo słabsze niż wiązania. Oddziaływania między cząsteczkami związku chemicznego, niepołączone wiązaniami chemicznymi, nazywamy oddziaływaniami międzycząsteczkowymi lub siłami van der Waalsa. Siła ta opisuje odpychanie lub przyciąganie między cząsteczkami i jest częściowo odpowiedzialna za stan skupienia związków chemicznych.

Wyróżniamy następujące typy oddziaływań międzycząsteczkowych:
Londona;
dipol–dipol;
wiązania wodorowe.
Oddziaływania te wpływają na:
temperaturę topnienia;
temperaturę wrzenia;
gęstość;
lotność.
Oddziaływania van der Waalsa
Zapoznaj się z poniższym filmem pt. „Siły van der Waalsa”, a następnie rozwiąż zadania.

Film dostępny pod adresem /preview/resource/RxPcxj9aYczSq
Film nawiązujący do treści materiału
Z kolei przyciąganie się dipoli trwałych nazywamy 1. wody, 2. siłami orientacyjnymi Keesoma, 3. sodu, 4. dipol‑dipol, 5. chlorowodoru, 6. ksenonu, 7. chlorkowymi, 8. jon‑dipol, 9. siłami indukcyjnymi Debaya lub po prostu oddziaływaniem typu 1. wody, 2. siłami orientacyjnymi Keesoma, 3. sodu, 4. dipol‑dipol, 5. chlorowodoru, 6. ksenonu, 7. chlorkowymi, 8. jon‑dipol, 9. siłami indukcyjnymi Debaya. Występuje ono m.in. między cząsteczkami ciekłego 1. wody, 2. siłami orientacyjnymi Keesoma, 3. sodu, 4. dipol‑dipol, 5. chlorowodoru, 6. ksenonu, 7. chlorkowymi, 8. jon‑dipol, 9. siłami indukcyjnymi Debaya.
Oddziaływania wodorowe
Zapoznaj się z poniższym filmem samouczkiem, a następnie rozwiąż ćwiczenia.

Film dostępny pod adresem /preview/resource/R1Ow0Uet1LCBp
Film nawiązujący do treści materiału - wyjaśnia, kiedy powstają wiązania wodorowe.
Poniżej przedstawiono wzory sześciu związków chemicznych. Oceń, w przypadku których związków możliwe jest występowanie wiązań wodorowych między cząsteczkami tego związku oraz w przypadku których związków możliwe jest występowanie wiązań wodorowych między cząsteczkami związku a wodą (w roztworze wodnym).
Zapoznaj się z opisami wzorów sześciu związków chemicznych. Oceń, w przypadku których związków możliwe jest występowanie wiązań wodorowych między cząsteczkami tego związku oraz w przypadku których związków możliwe jest występowanie wiązań wodorowych między cząsteczkami związku a wodą (w roztworze wodnym).
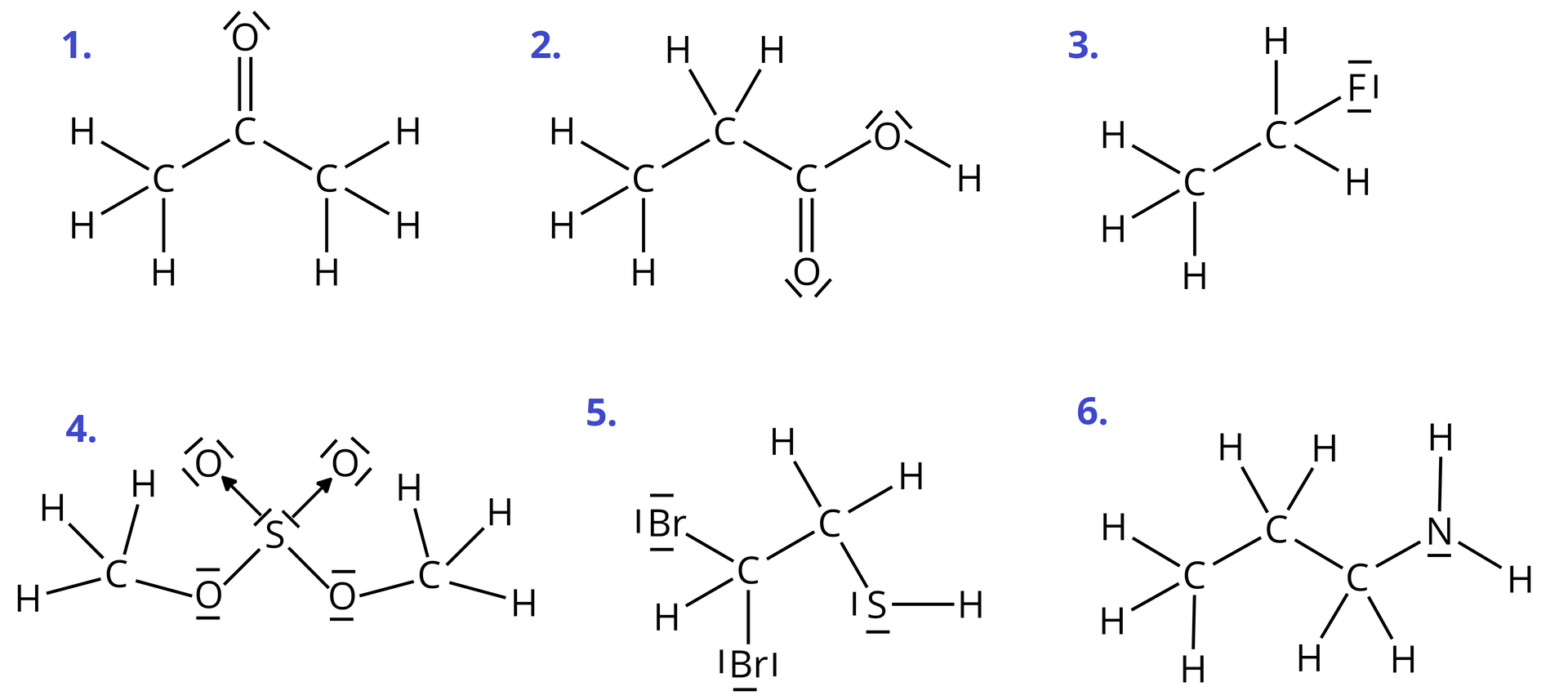
Oddziaływania dipol‑dipol
Czy wiesz, jakie rodzaje oddziaływań występują między dipolami? Zapoznaj się z poniższym filmem, a następnie rozwiąż zadania.

Film dostępny pod adresem /preview/resource/R1AwIU5EX0jLo
Film opisujący oddziaływania między dipolami
Cząsteczki chlorowodoru są dipolami. Próbkę ciekłego chlorowodoru umieszczono pomiędzy nienaładowanymi okładkami kondensatora. Opisaną sytuację możemy przedstawić schematycznie na poniższej grafice.

Następnie do okładek kondensatora przyłożono napięcie, co spowodowało zgromadzenie się ładunków dodatnich na jednej, a ujemnych na drugiej okładce kondensatora. Czy taka sytuacja, w konsekwencji której pojawiło się jednorodne pole elektryczne między okładkami, wpłynie na orientację przestrzenną cząsteczek chlorowodoru? Zaznacz grafikę przedstawiającą ułożenie cząsteczek chlorowodoru między okładkami naładowanego kondensatora.
Zaznacz poprawną odpowiedź.