Ochrona środowiska przed degradacją
17 zasad zrównoważonego rozwoju
W roku ONZ ogłosiło listę zasad zrównoważonego rozwoju:
- Modernizacja przemysłu chemicznego i zakładów produkcyjnych, aby stały się one bardziej zrównoważone poprzez stosowanie czystych i przyjaznych dla środowiska technologii i procesów produkcyjnych.
- Projektowanie, synteza i produkcja zaawansowanych materiałów sprawiających, że infrastruktura jest bardziej zrównoważona.
- Badania pozwalające na zwiększenie innowacyjności w zastosowaniach komercyjnych. Powyższe aspekty są możliwe do zrealizowania tylko dzięki licznym badaniom przeprowadzanym przez grupy chemików na całym świecie.
Chemia odgrywa istotną rolę w dążeniu do lepszego świata, zgodnego z zasadami zrównoważonego rozwoju. Niektóre z powyższych celów postawionych przez ONZ miały być zrealizowane do roku, a pozostałe mają być osiagnięte do roku .
Czy słyszałeś kiedyś o plastiku wytwarzanym z kukurydzy? Aby poznać co nieco informacji na ten temat, wysłuchaj poniższego audiobooka, a następnie rozwiąż załączone do niego ćwiczenia.
Kukurydziany plastik – czyli o polilaktydzie słów kilka
Polilaktyd, poli(kwas mlekowy) czy PLA jest to biodegradowalny polimer otrzymywany z surowców odnawialnych. Jego historia sięga lat 30. XX wieku, kiedy to naukowcy firmy DuPont ogrzewali w próżni kwas mlekowy.
Jednym z głównych źródeł kwasu mlekowego (kwasu 2-hydroksypropanowego) są odpady powstające w wyniku uprawy kukurydzy. Odpady te zawierają znaczne ilości skrobi – polimeru składającego się głównie z merów glukozy. Skrobia poddawana jest procesowi fermentacji w wyniku czego pozyskuje się m.in. kwas mlekowy. W wyniku reakcji odwodnienia kwasu mlekowego pozyskuje się cykliczny diester – laktyd. W wyniku odpowiedniej reakcji chemicznej z użyciem odpowiednich katalizatorów następuje polimeryzacja laktydu wiążąca się z otwarciem pierścienia estru.
Otrzymany w ten sposób polimer topi się w przedziale temperatur od 130 do 180°C, przez co z łatwością może być formowany do odpowiednich kształtów. Z polilaktydu produkuje się między innymi opakowania na żywność czy komponenty stosowane w medycynie.
Kukurydziany plastik ma pewne zalety, które sprawiają, że jest on atrakcyjny pod względem zarówno środowiskowym, jak i ekonomicznym. Obecnie do produkcji plastiku każdego dnia w Stanach Zjednoczonych zużywa się blisko 200 tysięcy baryłek ropy naftowej (1 baryłka to 158,98 dm3). Do produkcji polilaktydu wykorzystuje się głównie odpadki powstające w wyniku uprawy kukurydzy, co znów jest o wiele bardziej korzystne. Ponadto polilaktyd jest w pełni biokompostowalny – oznacza to, że w pewnych warunkach rozpada się na nieszkodliwe substancje pochodzenia naturalnego. Właściwość ta sprawia, że przepełnione już wysypiska śmieci mogą zostać znacznie odciążone. Obecnie szacuje się, że około 25% ich objętości stanowią tworzywa sztuczne.
Produkcja polilaktydu jest znacznie lepsza dla środowiska niż jego konwencjonalnych odpowiedników. W trakcie produkcji zużywa się do 65% mniej energii, a do atmosfery wydostaje się około 70% mniej gazów cieplarnianych, niezawierających toksycznych substancji.
Koniec życia polilaktydu odbywa się w specjalnie przeznaczonych do tego kompostownikach. Polilaktyd oraz resztki roślinne są wprowadzane do odpowiedniego pomieszczenia. Tam odpowiednie drobnoustroje trawią resztki roślinne w określonych warunkach temperatury przez około 10 dni. Polilaktyd rozkładany jest na tlenek węgla(IV) i wodę. Dlatego ważnym elementem recyklingu polilaktydu jest jego odpowiednie magazynowanie po zużyciu w odpowiednio przygotowanych do tego celu pojemnikach.
Jedną z wad polilaktydu jest to, że topi się w stosunkowo niskiej temperaturze. Dlatego też istnieją pewne ograniczenia w jego stosowaniu. Łyżka wykonana z polilaktydu mogłaby rozpuścić się w zjadanej przez nas gorącej zupie, a opakowanie z tego materiału, jeśli pozostawimy je w samochodzie w słoneczny letni dzień, może się odkształcić i nie wróci już do poprzedniej formy.
Blum C., Bunke D., Hungsberg M., Roelofs E., Joas A., Joas R., etc., The concept of sustainable chemistry. Key drivers for the transition towards sustainable development „Chemistry and Pharmacy” 2017, 5, s. 94–104.
Encyklopedia PWN, licencja: CC BY-SA 3.0.
Na powyższym rysunku zaznacz mer polilaktydu.
Jak dużo odpadów produkujemy?
Zgodnie z badaniami przeprowadzonymi w roku przez UNEP (Program Środowiskowy Narodów Zjednoczonych), rokrocznie na świecie produkuje się około milionów ton niebezpiecznych odpadów, co w przybliżeniu stanowi około zanieczyszczeń na osobę. W roku wyprodukowaliśmy około miliardy ton tlenku węgla(). Gdybyśmy go zestalili, otrzymując suchy lód, otrzymalibyśmy sześcian, którego każda z krawędzi ma . Dla porównania, najwyższy polski szczyt, a mianowicie Rysy, ma wysokość około .
Dane na podstawie: United Nations Environment Programme (2019). Emissions Gap Report 2019. UNEP, Nairobi.
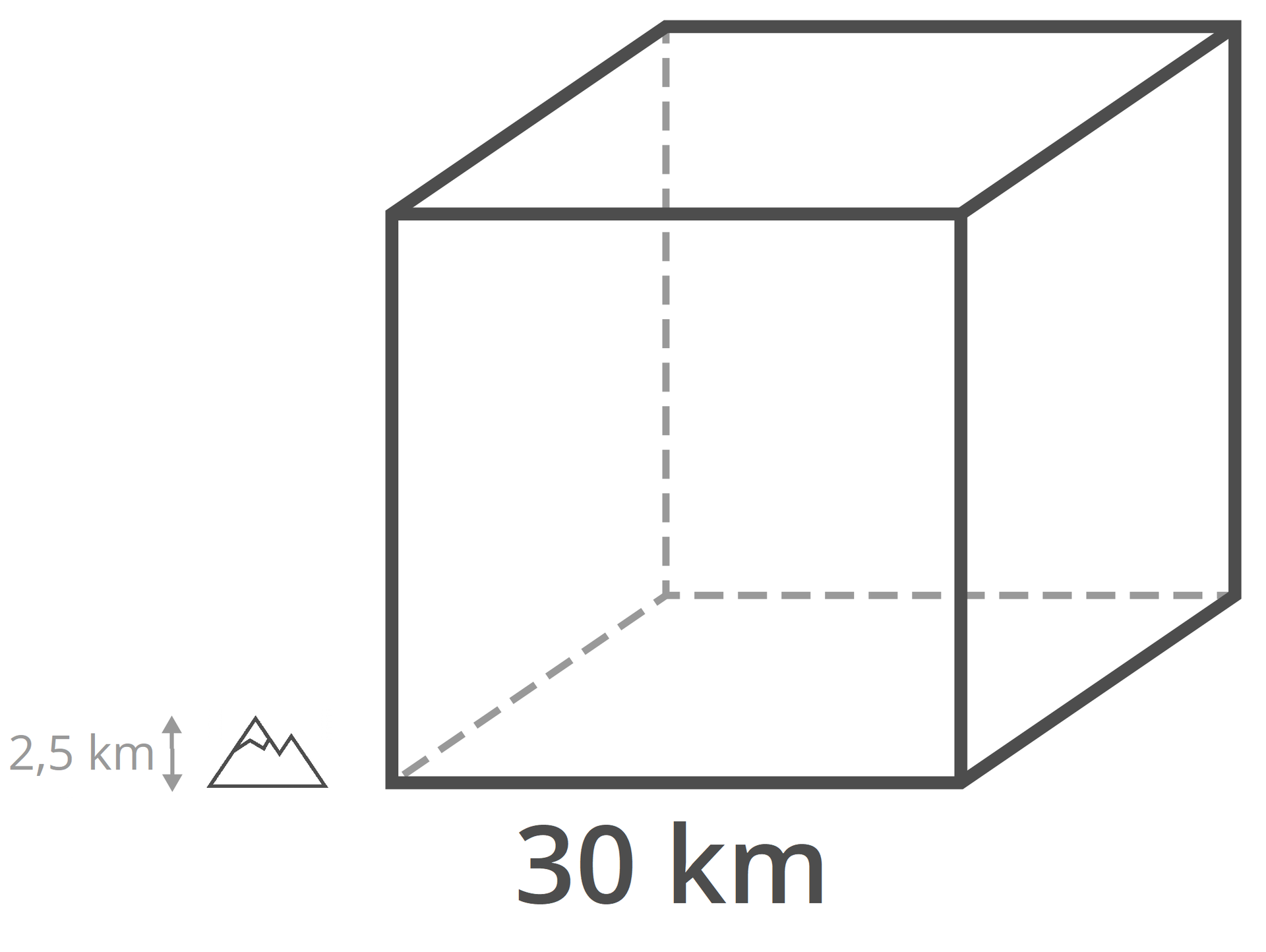
Innym, doskonale obrazującym przykładem na to, jak duża jest to ilość, może być grubość warstwy, jaka powstałaby w wyniku pokrycia całej powierzchni naszego kraju suchym lodem. Wynosiłaby ona aż !
Ciągły wzrost ludności na świecie powoduje zwiększone zapotrzebowanie na żywność, wodę, towary i usługi. Sprawia również, że ludzkość generuje większe ilości zanieczyszczeń i odpadów, które wpływają negatywnie na kondycję planety. Aby zadbać o naszą planetę, oprócz zrównoważonych działań, takich jak choćby recykling odpadów, ograniczenie produkcji tworzyw sztucznych, szkodliwych dla środowiska, oraz zwiększenie efektywności wytwarzania żywności, również chemia i przemysł chemiczny musiałyby wziąć na swoje barki odpowiedzialność za dobro Ziemi. Dlatego też w roku amerykański naukowiec Paul Anastas wprowadził pojęcie Zielona Chemia
.
Zielona chemia
Zielona chemia jest ciągłą próbą rozwiązywania problemów, które są powodowane przez chemikalia i procesy chemiczne. Jest to koncepcja, w której, aby zapobiec powstawaniu szkodliwych dla środowiska i dla człowieka substancji oraz zredukować ich zużycie, odpowiednio optymalizuje się i projektuje procesy chemiczne, w których one powstają. Koncepcja zielonej chemii opiera się na zasadach.
12 zasad zielonej chemii
Czynnik pokazujący wpływ odpadów na efektywność procesu opisuje się literą E. E jest to tzw. czynnik środowiskowy, który możemy opisać wzorem:
Idealną wartością czynnika E jest zero., Ekonomia atomu Ekonomia atomu (A E) jest to miara ilości atomów z materiału wyjściowego, które są obecne w produktach głównych (pożądanych) na końcu procesu chemicznego. Dlatego też ważnym jest, aby tak dobrać substraty, żeby zminimalizować ilość powstałych odpadów. Ilustracja przedstawiająca dwa symboliczne równania reakcji, w pierwszym powstają jedynie pożądane produkty, a w drugim oprócz produktów pożądanych - produkty uboczne. Równanie pierwsze. Czerwona kulka dodać niebieska kulka reprezentujące substraty, strzałka w prawo, czerwona kulka styka się z niebieską kulką, jest to powstały w wyniku reakcji produkt. Równanie drugie. Czerwona kulka stykająca się na górze z zielonym trójkątem, co odpowiada pierwszemu substratowi. Dodać różowy kwadrat stykający się z czterema niebieskimi, małymi kulkami, co reprezentuje drugi substrat. Strzałka w prawo, czerwona kulka stykająca się z niebieską kulką, co odpowiada produktowi. Poniżej znajdują się produkty uboczne, to jest pierwszy reprezentowany przez różowy kwadrat stykający się u góry z zielonym trójkątem, a na dole z małą, niebieską kulką, dodać drugi produkt uboczny, któremu odpowiadają dwie małe stykające się niebieskie kulki. Schematyczne przedstawienie A E. W pierwszej reakcji z dwóch substratów powstaje jeden produkt. W drugiej natomiast z dwóch substratów powstaje jeden produkt główny oraz dwa produkty uboczne.
Źródło: GroMar Sp. z o.o.; Licencja: CC BY‑SA 3.0
Czynnik A E możemy wyrazić poniższym wzorem:
gdzie M – masa molowa.
Np. dla reakcji:
Pożądana wartość A E to jeden., Minimalizacja szkodliwych odczynników podczas syntezy Projektując syntezy chemiczne, należy tak dobierać reagenty, aby nie stanowiły one zagrożenia dla zdrowia i życia ludzi. Ponadto należy pamiętać o tym, aby synteza chemikaliów była jak najbezpieczniejsza, dlatego też należy używać, jako materiałów wyjściowych, substancji nietoksycznych, jeżeli stanowią one alternatywę dla tych niebezpiecznych. Proces produkcyjny należy projektować tak, aby uniknąć powstawania niebezpiecznych odpadów chemicznych, które następnie należy zutylizować.
Istotną rolę pełnią również rozpuszczalniki wykorzystywane w reakcjach. Ilustracja przedstawiająca nazwy oraz wzory rozpuszczalników podzielone na trzy grupy na podstawie zasad zielonej chemii: rekomendowane, nadające się do użytku oraz nierekomendowane. Wymienione grupy zostały oznaczone kolorami, odpowiednio zielonym, żółtym i czerwonym. Wśród rekomendowanych rozpuszczalników znajdują się woda H indeks dolny, dwa, koniec indeksu dolnego, O, alkohole takie jak: metanol C H indeks dolny, trzy, koniec indeksu dolnego, O H, etanol C H indeks dolny, trzy, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, O H czy izopropanol zbudowany z grupy C H połączonej za pomocą wiązań pojedynczych z grupą hydroksylową oraz z dwiema grupami metylowymi C H indeks dolny, trzy, koniec indeksu dolnego. Ostatnim rekomendowanym rozpuszczalnikiem jest aceton, czyli propan-
Źródło: GroMar Sp. z o.o.; Licencja: CC BY‑SA 3.0
W reakcjach prowadzonych na dużą skalę lub w reakcjach, w wyniku których otrzymuje się różnego rodzaju medykamenty, zalecane jest wykorzystywanie rozpuszczalników rekomendowanych. Ze względu na wysoką toksyczność oraz zagrożenie dla środowiska, rozpuszczalników nierekomendowanych nie wykorzystuje się w procesach przemysłowych., Projektowanie chemikaliów w taki sposób, aby były one mniej szkodliwe, ale zachowywały swoje funkcje Powyższa zasada ściśle łączy się z poprzednią zasadą. Pracą chemików jest poszukiwanie nowych materiałów, które mogą zastąpić inne, bardziej szkodliwe. Projektowanie nowych związków i materiałów wymaga odpowiedniej wiedzy na temat ich wpływu na środowisko lub zdrowie i życie ludzi oraz zwierząt., Ograniczenie użycia rozpuszczalników oraz zminimalizowanie ich szkodliwości Wiele procesów i reakcji chemicznych potrzebuje użycia rozpuszczalników. Niektóre rozpuszczalniki charakteryzują się dużą toksycznością oraz niebezpieczeństwami związanymi z ich użytkowaniem, np. są łatwopalne i lotne. W większości przypadków użycie rozpuszczalników jest konieczne, aby zwiększyć wydajność, dlatego też należy odpowiednio dobrać ich ilość. Jednakże należy poszukiwać mniej toksycznych alternatyw lub, jeżeli to możliwe, pozostały po procesie rozpuszczalnik wykorzystać ponownie., Wydajne wykorzystanie energii w procesach chemicznych Energochłonne procesy nie są zgodne z zasadami zielonej chemii. Procesy lub reakcje należy projektować w taki sposób, aby nie było konieczne grzanie lub chłodzenie układu reakcyjnego, a jeżeli to możliwe, proces należy prowadzić w warunkach temperatury pokojowej i ciśnienia atmosferycznego. Przy projektowaniu procesu należy również wziąć pod uwagę procesy usuwania rozpuszczalników lub zanieczyszczeń, które również wymagają nakładów energii., Wykorzystanie surowców pochodzących ze źródeł odnawialnych Zasada ta odnosi się głównie do produktów powstających z nieodnawialnych źródeł energii, takich jak np. ropa naftowa. Z półproduktów powstających z ropy naftowej produkuje się tworzywa sztuczne, takie jak np. plastik. Ropa naftowa jest źródłem nieodnawialnym, o ograniczonym wydobyciu. Dlatego też w projektowaniu nowych materiałów można wykorzystywać substraty pochodzenia naturalnego – takie jak np. substancje pochodzenia roślinnego., Ograniczenie powstawania dodatkowych odpadów wskutek wykorzystania np. grup zabezpieczających Grupy zabezpieczające są często wykorzystywane w chemii organicznej. Niektóre grupy funkcyjne mogą znacząco zmniejszać reaktywność substratów lub wydajność. Wprowadzenie grup zabezpieczających zapobiega powstawaniu produktów ubocznych lub innych niepożądanych reakcji chemicznych. Jednakże wiąże się to z kolejnymi, dodatkowymi etapami reakcji chemicznych, które wymagają użycia dodatkowych reagentów, rozpuszczalników i zużycia energii. Dlatego też, projektując proces chemiczny, należy tak dobrać substraty, aby nie było koniecznym wykonywanie dodatkowych kroków w syntezie. Do przeprowadzenia niektórych procesów chemicznych można wykorzystać enzymy pochodzenia naturalnego – produkowane przez np. bakterie czy grzyby. Ilustracja przedstawiająca schemat reakcji. Od substratu A poprowadzona jest strzałka w prawo do produktu B. Nad strzałką zapis: enzym. Oprócz tego od substratu A poprowadzono strzałkę w dół do C, od C strzałkę w prawo do D, zaś od D strzałkę w górę do produktu B. Co obrazuje dwie drogi prowadzące do produktu B, jednoetapową z udziałem enzymu oraz wieloetapową bez wykorzystania enzymów.
Źródło: GroMar Sp. z o.o.; Licencja: CC BY‑SA 3.0
Aby z substratu A otrzymać produkt B, można obrać dwie ścieżki: Czarną – z wykorzystaniem np. enzymów (jeden etap) Czerwoną – ze związku A otrzymuje się związek C, ze związku C – związek D, ze związku D – finalny produkt B (trzy etapy).
Czerwona ścieżka może reprezentować przeprowadzenie procesu z wykorzystaniem grupy zabezpieczającej. W planowaniu syntezy z wykorzystaniem grup zabezpieczających należy uwzględnić przynajmniej dwa dodatkowe etapy – etap "zabezpieczania" (blokowania) danej grupy funkcyjnej w określonym reagencie i etap jej "odbezpieczania"., Kataliza Kataliza jest to zjawisko, w którym następuje przyspieszenie reakcji chemicznej po dodaniu niewielkiej ilości katalizatora. Katalizator nie jest zużywany w trakcie reakcji, dlatego też może być ponownie wykorzystany. W niektórych przypadkach użycie katalizatora umożliwia przebieg reakcji, która nie zachodziłaby w danych warunkach, lub powoduje zmniejszenie ilości produktów ubocznych. Wykres zależności energii od przebiegu reakcji. Oś pionowa opisana jako energia, z kolei oś pozioma jako przebieg reakcji, czyli jej postęp w czasie. W pierwszym przypadku krzywa reprezentuje funkcję dla reakcji prowadzonej bez udziału katalizatora. Poziomy fragment prostopadły do osi pionowej odpowiada energii substratów, następnie funkcja gwałtownie rośnie w miarę postępu reakcji, osiągając maksimum, a następnie maleje, osiągając energię produktów reakcji, która w tym przypadku jest mniejsza od energii substratów. W drugim przypadku reakcja prowadzona jest z udziałem katalizatora, co obrazuje druga krzywa, energie substratów i produktów są jednakowe jak dla reakcji bez udziału katalizatora, jednakże maksymalna energia osiągnięta w trakcie jej przebiegu jest znacząco niższa, zatem katalizator wpłyną na zmniejszenie energii aktywacji reakcji.
Źródło: GroMar Sp. z o.o.; Licencja: CC BY‑SA 3.0
Użycie katalizatora zmniejsza energię potrzebną do zajścia reakcji chemicznej, dzięki czemu zużywa się mniej energii do jej przeprowadzenia, a to jest korzystne dla środowiska. Co więcej, warto stosować katalizatory naturalnego pochodzenia – enzymy – zamiast katalizatorów zawierających w centrach aktywnych metale ciężkie, np. pallad, platynę czy nikiel., Projektowanie produktów w taki sposób, aby po okresie ich użytkowania rozkładały się do substancji nieszkodliwych Idealne produkty reakcji chemicznych powinny być zaprojektowane tak, aby po okresie ich zużycia rozpadały się na substancje nieszkodliwe dla środowiska. Niektóre zanieczyszczenia organiczne mogą wykazywać wysoką trwałość oraz utrzymywać się w środowisku przez wiele lat. Jednym z przykładów trwałych i szkodliwych dla środowiska związków chemicznych może być związek DDT (dichlorodifenylotrichloroetan). Rozkłada się on do związków DDD i DDE, które są równie trwałe oraz równie szkodliwe. Schemat reakcji przedstawiających produkty, do jakich przekształcany jest DDT w wyniku metabolizmu. D D T zbudowany jest z grupy C H połączonej za pomocą wiązań pojedynczych z dwoma podstawnikami cztery-chlorofenylowymi, a także z atomem węgla podstawionym trzema atomami chloru. Może on ulegać dwóm przemianom. W wyniku pierwszej od D D T odłącza się jedna cząsteczka chlorowodoru, co prowadzi do powstania D D E zbudowanego z atomu węgla połączonego za pomocą wiązań pojedynczych z dwiema grupami cztery-chlorofenylowymi, a także za pomocą wiązania podwójnego z atomem węgla podstawionym dwoma atomami chloru. Na drodze drugiej możliwej przemiany, która polega na redukcji z uwolnieniem cząsteczki chlorowodoru, powstaje D D D zbudowany z grupy C H połączonej za pomocą wiązań pojedynczych z dwoma podstawnikami cztery-chlorofenylowymi, a także z atomem węgla podstawionym dwoma atomami chloru i jednym wodoru.
Źródło: www.wikipedia.org; Licencja: domena publiczna
Dlatego ważnym jest, aby projektować produkty w taki sposób, aby ulegały degradacji do nieszkodliwych substancji pod wpływem promieniowania UV, wilgoci lub organizmów żywych, głównie saprobiontów (tzw. biodegradacja)., Kontrolowanie w czasie rzeczywistym procesów chemicznych, aby uniknąć powstawania szkodliwych zanieczyszczeń Monitorowanie reakcji w czasie rzeczywistym może odbywać się przy pomocy odpowiednich technik analitycznych. Monitoring procesu pozwala na uniknięcie powstawania niebezpiecznych i szkodliwych substancji, mogących stanowić zagrożenie dla zdrowia lub życia osób pracujących przy procesie. Odpowiednia kontrola pozwala na odpowiednio wczesne zatrzymanie procesu, a co za tym idzie uniknięcie niebezpiecznych wypadków., Stosowanie substancji ograniczających możliwość powstawania wypadków Nieodłącznym elementem pracy z chemikaliami jest ryzyko. Odpowiednie zarządzanie zagrożeniami może je zminimalizować. Zasada dwunasta ściśle łączy się z innymi zasadami omawiającymi niebezpieczne reagenty. Tam, gdzie jest to możliwe, należy wyeliminować narażenie na zagrożenie, a w przypadku, gdy eliminacja jest niemożliwa, proces powinien być zaprojektowany w taki sposób, aby je zminimalizować.
Zagraj w grę dotyczącą zasad zielonej chemii. Gra składa się z dwóch etapów następujących po sobie, a przejście do drugiego jest możliwe dopiero po zaliczeniu pierwszego. W pierwszym etapie sprawdzisz swoją znajomość oraz rozumienie zasad zielonej chemii, a w drugim ich zastosowanie w praktyce. Powodzenia!

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DCTKS1T3S
Zagraj w grę dotyczącą zasad zielonej chemii. Po udzieleniu odpowiedzi dowiesz się, czy rozumiesz znaczenie zasad zielonej chemii i czy będziesz w stanie wykorzystać je w praktyce. Powodzenia!
