Jak otrzymać sole?
Metody otrzymywania soli
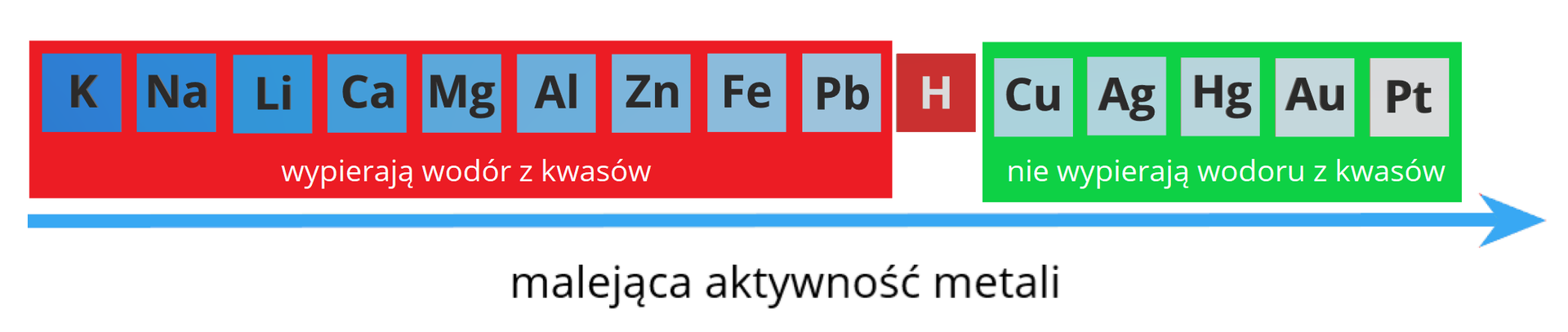
Reakcje metali z kwasami
Reakcji z wydzieleniem wodoru będą ulegały tylko metale o ujemnych wartościach potencjału. Pozostałe metale nie wypierają wodoru z kwasów. , , i mogą jednak reagować ze stężonym, gorącym kwasem siarkowym(VI) oraz z rozcieńczonym i stężonym kwasem azotowym(V). W reakcjach tych nie powstaje jednak wodór, ale odpowiednie tlenki
Inne metale, takie jak np. żelazo, również mogą reagować z kwasami silnie utleniającymi bez wydzielenia wodoru, np.:
Reakcje te przebiegają w dwóch etapach:
Etap 1: metal utlenia się do swojego tlenku;
Etap 2: tlenek metalu reaguje z kwasem, dając odpowiednią sól. Dlatego też metale ulegające pasywacji, nie roztwarzają się w stężonym kwasie azotowym. Do takich przypadków należą: glin, chrom, żelazo oraz kobalt, nikiel i molibden. W rozcieńczonym roztworze pasywacja zachodzi w dużo mniejszym stopniu i roztworzenie metalu staje się bardziej prawdopodobne.

Reakcja tlenku zasadowego z kwasem bądź tlenku amfoteryczneg z mocnym kwasem
W wyniku reakcji powstaje sól i woda. Przykładowe równania reakcji:
Skutecznym produktem usuwającym rdzę jest... Cola! Wystarczy zanurzyć w niej przedmiot ze śladami rdzy na kilka minut, a następnie dokładnie wyszorować, umyć i osuszyć. Dzieje się tak za sprawą obecnego w niej kwasu ortofosforowego, który reaguje z rdzą (tlenkami żelaza).
Reakcja wodorotlenku z kwasem
W jej wyniku powstaje sól i woda. Jest to najbardziej uniwersalna metoda otrzymywania soli. Przykładowe równania reakcji:
Reakcja wodorotlenku z tlenkiem kwasowym
W reakcji tej otrzymać można tylko sole kwasów tlenowych. Przykładowe równania reakcji:
Reakcja tlenku kwasowego z tlenkiem zasadowym
W wyniku reakcji powstaje sól – tylko otrzymywanie soli kwasów tlenowych. Przykładowe równania reakcji
Reakcja metalu z niemetalem
Powstaje sól – tylko otrzymywanie soli kwasów beztlenowych. Przykładowe równania reakcji:
Reakcja metalu i rozpuszczalnej w wodzie soli mniej aktywnego metalu
Powstaje inna sól i inny metal (mówimy wtedy o wypieraniu metalu z roztworu jego soli). Przykładowe równania reakcji:
Reakcja soli z kwasem
Powstaje inna sól i inny kwas. Zachodzi, gdy powstała sól jest solą trudno rozpuszczalną w wodzie lub gdy sól biorąca udział w reakcji jest solą słabego kwasu i reaguje z mocnym kwasem. Przykładowe równania reakcji:
Reakcja wodorotlenku i soli
Powstają inna sól i inny wodorotlenek. Reakcja zachodzi w przypadku, gdy wszystkie substraty są rozpuszczalne, natomiast jeden z produktów – sól lub wodorotlenek – jest trudno rozpuszczalny. Przykładowe równania reakcji:
Reakcje między dwiema solami
Zachodzą one wówczas, gdy powstają sole trudniej rozpuszczalne od soli stanowiących substraty tych reakcji. Ponadto, substratami mogą być jedynie dobrze rozpuszczalne sole. Przykładowe równania reakcji:
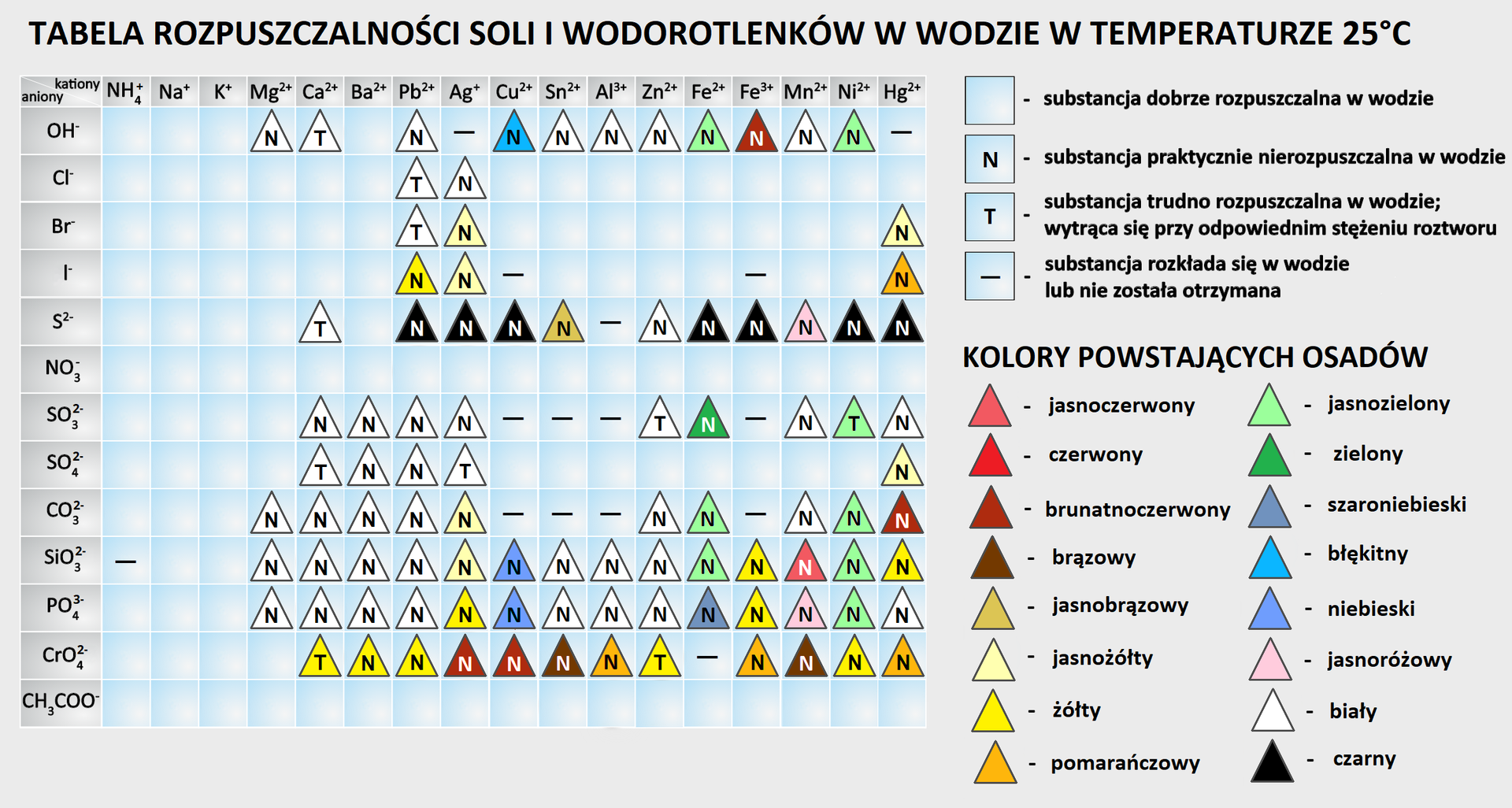
Otrzymując sole, warto korzystać z tabeli rozpuszczalności
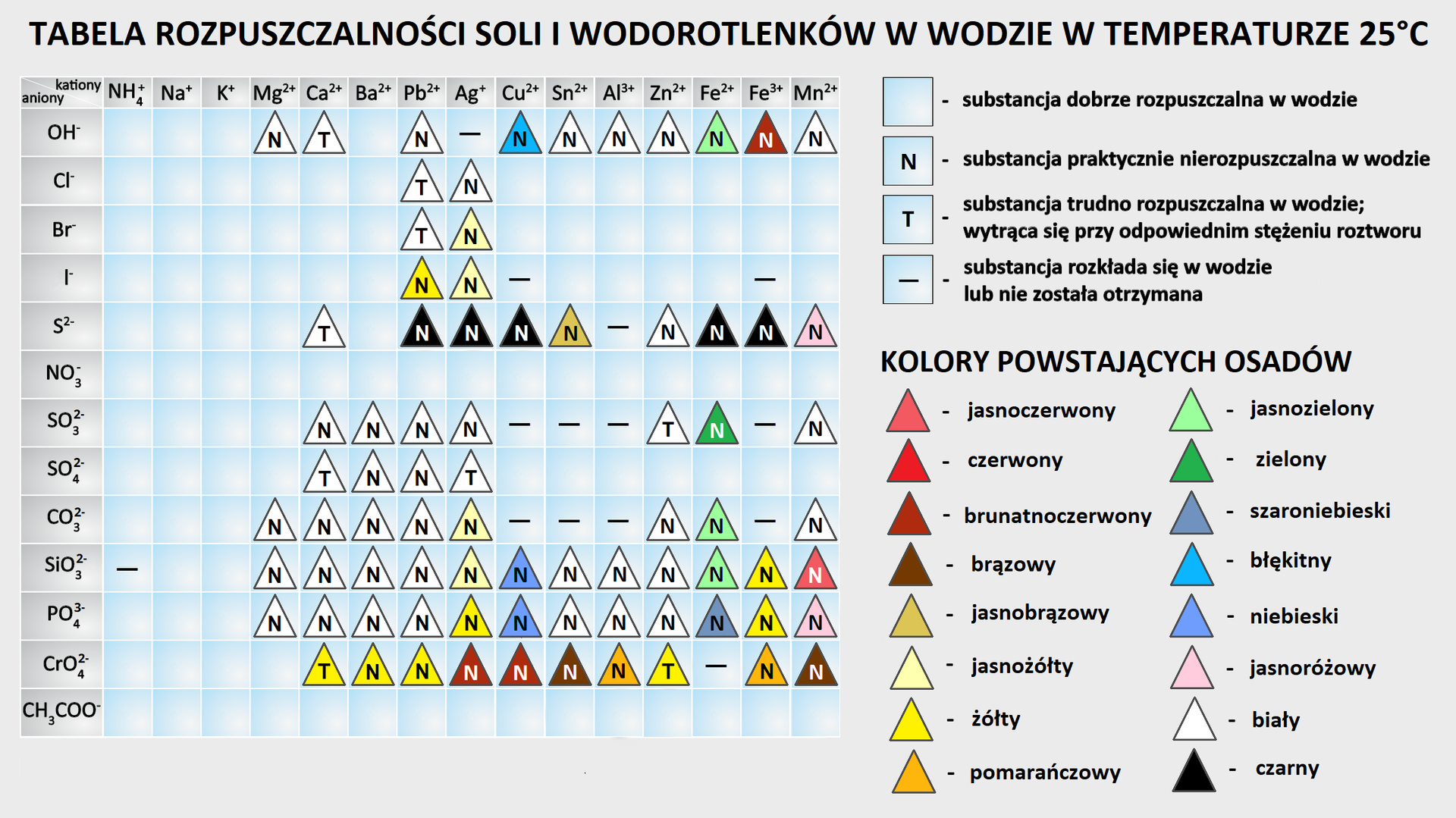
lub zapamiętać wynikające z niej reguły dla popularnych soli:
dobrze rozpuszczalne są sole litowców (sodu, potasu) i amonu;
dobrze rozpuszczalne są azotany, etaniany (octany) i chlorany;
większość siarczanów należy do dobrze rozpuszczalnych (wyjątkami są: , , );
do trudno rozpuszczalnych należą i ;
większość chlorków, bromków i jodków jest dobrze rozpuszczalna z wyjątkiem soli , i ;
większość siarczków metali jest trudno rozpuszczalna (dobrze rozpuszczalne są siarczki litowców, berylowców i amonu);
większość węglanów i ortofosforanów jest trudno rozpuszczalna, dobrze rozpuszczalne są węglany i ortofosforany litowców i amonu.
Umiejętność pisania i uzgadniania równań reakcji jest niezbędna w tzw. analizie chemicznej.
Zapoznaj się z możliwościami poniższego laboratorium chemicznego i zaproponuj doświadczenia, w wyniku przeprowadzenia których możesz otrzymać sole. Następnie zapoznaj się z problemem badawczym, sformułuj i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje, wyniki oraz zapisz wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D8L9X61LQ
Zapoznaj się z opisem serii eksperymentów przeprowadzanych w laboratorium chemicznym. Następnie zapoznaj się z problemem badawczym, sformułuj i zweryfikuj własną hipotezę. Na koniec rozwiąż krótkie zadania sprawdzające.
Analiza eksperymentu: Otrzymywanie siarczanu magnezu różnymi metodami.
Problem badawczy: Czy siarczan magnezu można otrzymać za pomocą sześciu różnych metod?
Hipoteza: Siarczan magnezu można otrzymać za pomocą sześciu różnych metod.
Sprzęt laboratoryjny:
probówki (6 sztuk) – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
pipety jednorazowe – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki chemiczne:
roztwór kwasu siarkowego, siarczan miedzi – roztwór wodny, siarczek magnezu – roztwór wodny, wodorotlenek magnezu, tlenek magnezu, magnez.
Przebieg eksperymentu:
Probówka 1 – Umieszczono w probówce za pomocą pipety jednorazowej roztworu kwasu siarkowego, a następnie dodano magnezu.
Probówka 2 – Umieszczono w probówce za pomocą pipety jednorazowej roztworu kwasu siarkowego, a następnie dodano tlenku magnezu.
Probówka 3 – Umieszczono w probówce za pomocą pipety jednorazowej roztworu kwasu siarkowego, a następnie dodano wodorotlenku magnezu.
Probówka 4 – Umieszczono w probówce za pomocą pipety jednorazowej siarczanu miedzi, a następnie dodano magnezu.
Probówka 5 – Umieszczono w probówce za pomocą pipety jednorazowej siarczanu miedzi, a następnie dodano siarczku magnezu.
Probówka 6 – Umieszczono w probówce za pomocą pipety jednorazowej siarczku magnezu i dodano do niej roztworu kwasu siarkowego. Następnie ustaw nad probówkę uniwersalny papierek wskaźnikowy.
Obserwacje:
Probówka 1 . Magnez po wprowadzeniu do kwasu roztwarza się. Wydziela się bezbarwny gaz.
Probówka 2. Tlenek magnezu po wprowadzeniu do kwasu roztwarza się.
Probówka 3. Wodorotlenek magnezu po wprowadzeniu do kwasu roztwarza się.
Probówka 4. Magnez roztwarza się. Niebieski roztwór odbarwia się. Wytrąca się brunatnoczerwony (różowoczerwony) osad.
Probówka 5. Wytrąca się czarny osad. Niebieski roztwór odbarwia się.
Probówka 6. Wydziela się bezbarwny gaz o zapachu zgniłych jaj. Zwilżony wodą uniwersalny papierek wskaźnikowy zmienia zabarwienie na czerwone.
Wyniki:
Gazem wydzielającym się w probówce pierwszej jest wodór. W probówce czwartej roztwór zmienia kolor na jasnozielony, ze względu na powstającą w reakcji chemicznej miedź. Czarnym osadem pojawiającym się w probówce piątej jest siarczek miedzi. Wydzielającym się gazem w probówce szóstej, o charakterystycznym zapachu, jest kwas siarkowodorowy.
Wnioski:
Siarczan magnezu jest solą, którą można otrzymać za pomocą sześciu różnych metod. Hipoteza została potwierdzona.
Właściwości fizykochemiczne soli
Poniżej przedstawiono schemat pewnego doświadczenia.
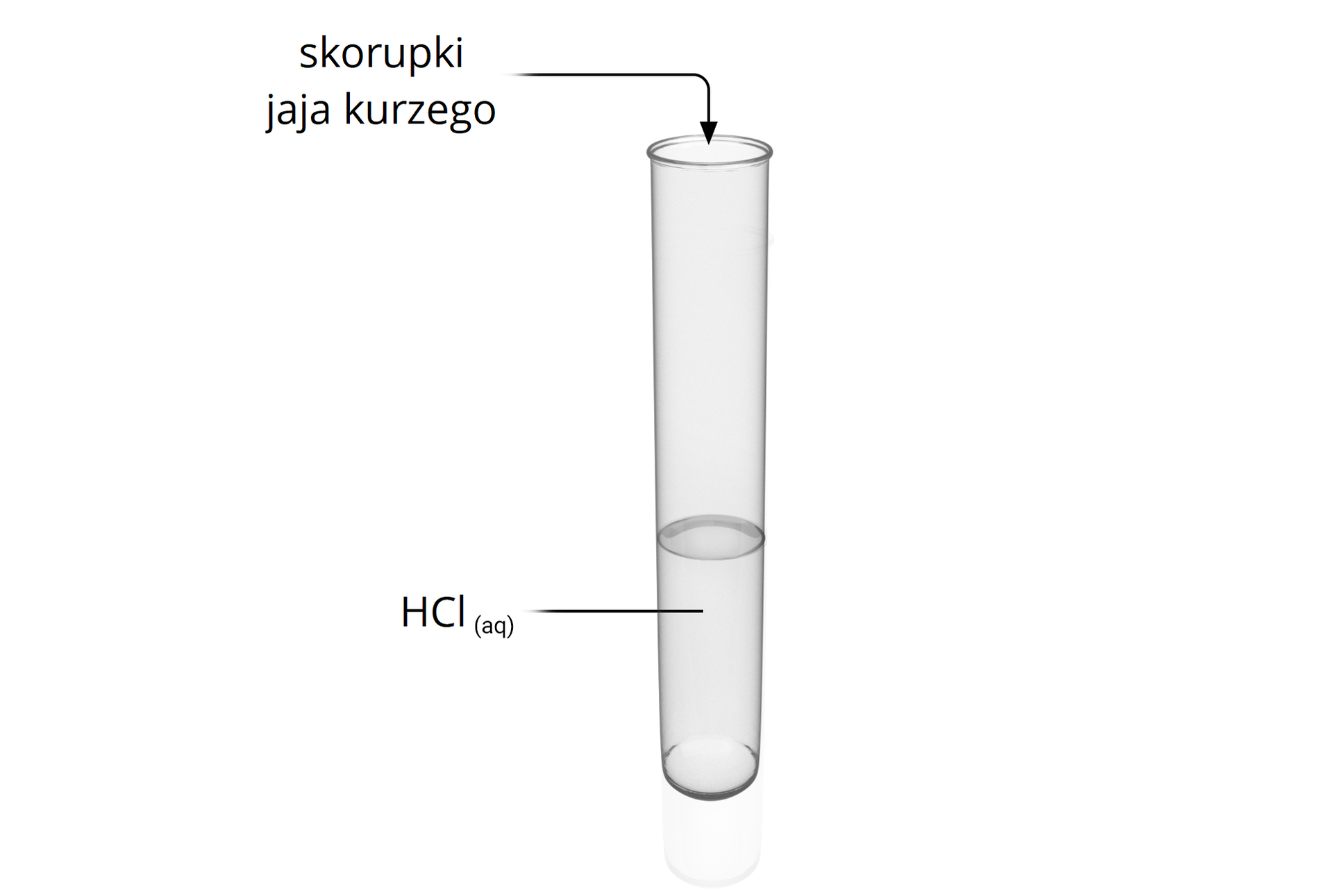
Pewien uczeń zapisał swoje obserwacje po wykonaniu doświadczenia:
Pewien uczeń przeprowadził doświadczenie chemiczne polegające na dodaniu skorupek jaja kurzego do kwasu chlorowodorowego. Następnie zapisał on swoje obserwacje:
„Skorupki jaja kurzego roztworzyły się. Zaczął wydzielać się bezbarwny, bezwonny gaz. Po pewnym czasie w zlewce pozostała jedynie ciecz.”
Do najważniejszych reakcji, jakim ulegają sole, należą reakcje ich rozkładu. Najczęściej mamy do czynienia z rozkładem termicznym. Powstaje wówczas tlenek metalu i tlenek niemetalu.
Możliwy jest również rozpad soli pod wpływem promieni świetlnych. Na przykład bromek srebra() ulega takiemu rozkładowi. Dzięki temu znalazł zastosowanie w fotografii, będąc składnikiem między innymi światłoczułych emulsji fotograficznych.
Sole znalazły liczne zastosowania w: gospodarstwie domowym, rolnictwie, przemyśle chemicznym, budownictwie i medycynie. Stanowią między innymi środki konserwujące, składniki nawozów sztucznych, zaprawy murarskie czy opatrunki gipsowe.
Mapa pojęć
Mapa pojęć ukazuje budowę, właściowości, otrzymywanie i zastosowania soli. Zielony węzeł opisuje budowę. Sole to substancje krystaliczne o budowie jonowej. Składają się z kationów metali (lub np. kationu amonu) oraz anionów reszt kwasowych. Przedstawiono następujący wzór sumaryczny: kolorem zielonym , opisane jako kation metalu , a dalej kolorem czerwonym , opisane jako anion reszty kwasowej kwasu .
Pomarańczowy węzeł opisuje otrzymywanie. Przedstawiono różne równania reakcji.
Reakcja tlenku kwasowego z wodorotlenkiem:
tlenek węgla cztery plus wodorotlenek sodu strzałka w prawo węglan sodu plus woda
Reakcja kwasu z wodorotlenkiem:
kwas bromowodorowy plus wodorotlenek potasu strzałka w prawo bromek potasu plus woda
Reakcja tlenku zasadowego z kwasem:
tlenek żelaza dwa plus kwas chlorowodorowy strzałka w prawo chlorek żelaza dwa plus woda
Reakcja soli z wodorotlenkami pierwszej i drugiej grupy układu okresowego pierwiastków (tak zwanymi mocnymi zasadami):
chlorek żelaza trzy plus wodorotlenek sodu strzałka w prawo wodorotlenek żelaza trzy plus chlorek sodu
Reakcja tlenku kwasowego z tlenkiem zasadowym:
tlenek potasu plus tlenek siarki cztery strzałka w prawo siarczan cztery potasu
W reakcji otrzymywania, w której bierze udział tlenek niemetalu, powstają sole kwasów tlenowych.
Reakcja metalu z kwasem:
magnez plus kwas siarkowy sześć strzałka w prawo siarczan cztery magnezu plus wodór
Nie wszystkie metale reagują w ten sposób z kwasami. Te metale, które leżą w szeregu aktywności metali za atomem wodoru, nie wypierają go z kwasów, np. czy .
Reakcja metalu z niemetalem:
glin plus siarka strzałka w prawo siarczek glinu
Powstają jedynie sole kwasów beztlenowych.
Reakcja mocnych kwasów z siarczanami() lub węglanami:
kwas bromowodorowy plus siarczan cztery wapnia strzałka w prawo bromek wapnia tlenek siarki cztery plus woda
Reakcja soli z solami:
chlorek wapnia plus fosforany pięć sodu strzałka w prawo fosforany pięć wapnia plus chlorek sodu
Należy pamiętać, że jedną z otrzymywanych soli musi być sól słabo lub trudno rozpuszczalna w wodzie.
Kremowy węzeł opisuje zastosowania. Sole wykorzystywane są w budownictwie, do gipsowania ścian stosuje się między innymi siarczan() wapnia. Zamieszczono ilustrację ukazującą fragment sufitu z kwadratowym wgłębieniem. Ręka ubrana w czerwono–zieloną, ubrudzoną na biało bluzkę, nakłada szpachelką gips na brzegi wgłębienia. W medycynie sole wykorzystuje się sól fizjologiczną, czyli –procentowy roztwór chlorku sodu () stosowana w medycynie do uzupełniania niedoborów kationów sodu i anionów chlorkowych. Zamieszczono ilustrację przedstawiającą metalowy stojak, na którym zawieszone są trzy torebki z kroplówką, W lewym dolnym rogu zdjęcia znajduje się dłoń sięgająca po jedną z torebek. Składnikiem proszku do pieczenia, wykorzystywanego w gospodarstwach domowych, jest między innymi wodorowęglan amonu (). W procesie jego rozkładu termicznego powstaje między innymi tlenek węgla(), który spulchnia ciasto. Zamieszczono ilustrację przedstawiającą leżący bokiem, na białym, porcelanowym talerzu, kawałek czekoladowego tortu. Obok ciasta leży biały widelec. W rolnictwie stosuje się nawozy, aby uzupełnić niedobory składników odżywczych dla roślin. W większości są to sole, między innymi , , , czy .
Czerwony węzeł opisuje właściwości chemiczne i fizyczne soli. Opis właściwości chemicznych podzielono na: dysocjację elektrolityczną, reakcje strąceniowe i reakcje rozkładu. Dysocjacja elektrolityczna to rozpad elektrolitu na jony pod wpływem wody. W jego wyniku do roztworu uwalniane są kationy metali (lub kation amonu) i aniony reszty kwasowej. Zamieszczono następujące równania reakcji:
chlorek amonu strzałka w prawo nad strzałką woda za strzałką kation amonowy plus anion chlorkowy
azotan pięć baru strzałka w prawo nad strzałką woda za strzałką kation baru plus anion azotanowy pięć
Sole ulegają między innymi reakcjom strąceniowym. W ich wyniku wyniku otrzymujemy osady, czyli substancje stałe wydzielone z roztworu. Reakcje strąceniowe, którym ulegają sole należą do typu reakcji wymiany podwójnej, w której substratami są sole i zasady, sole i kwasy lub dwie sole. Zamieszczono przykładowe równania reakcji (w równaniach reakcji strzałką skierowaną w dół zaznaczamy substancję powstającą w postaci osadu (strąconą)):
sól pierwsza plus wodorotlenek pierwszy strzałka w prawo sól druga plus wodorotlenek drugi strzałka w dół
sól pierwsza plus sól druga strzałka w prawo sól trzecia strzałka w dół plus sól czwarta lub sól pierwsza plus sól druga strzałka w prawo sól trzecia plus sól czwarta strzałka w dół
sól pierwsza plus wodorotlenek pierwszy strzałka w prawo sól druga strzałka w dół plus wodorotlenek drugi
sól pierwsza plus kwas pierwszy strzałka w prawo sól druga strzałka w dół plus kwas drugi
Rozkład termiczny soli kwasów tlenowych często prowadzi do powstania tlenków.
węglan cynku strzałka w prawo tlenek cynku plus tlenek węgla cztery
Niektóre sole ulegają rozkładowi pod wpływem światła. Na przykład rozkład soli beztlenowej może prowadzić do otrzymania metalu i niemetalu.
chlorek srebra strzałka w prawo nad strzałką światło za strzałką srebro plus chlor
Właściwości fizyczne podzielono na: stan skupienia, barwy, rozpuszczalność w wodzie i temperaturę topnienia. Sole w temperaturze pokojowej to ciała stałe najczęściej o budowie krystalicznej. Większość soli ma barwę białą. Jednak występują również sole bezbarwne lub charakteryzujące się różnymi barwami. Węglan wapnia ma barwę białą. Zamieszczono ilustrację przedstawiającą szaro–białe kostki węglanu wapnia. tworzy ciemnofioletowe kryształy. Zamieszczono ilustrację przedstawiającą szalkę, na której znajduje się stosik drobnych, ciemnych kryształków. Wytrącony w roztworze. Zamieszczono ilustrację przedstawiającą zlewkę, w której znajduje się sto dwadzieścia pięć mililitrów żółto–pomarańczowej, przezroczystej, błyszczącej w świetle substancji. Pod względem rozpuszczalności w wodzie, sole są bardzo zróżnicowane. Na rozpuszczalność w wodzie wpływa zarówno kation, jak i anion soli. Wszystkie azotany() oraz sole sodowe, potasowe i amonowe są dobrze rozpuszczalne w wodzie. Natomiast do najbardziej znanych soli trudno rozpuszczalnych w wodzie należą między innymi , , , , , , . Do sprawdzenia rozpuszczalności różnych soli w wodzie służy tabela rozpuszczalności. Pod wpływem temperatury niektóre sole topnieją. Rozerwana zostaje wówczas struktura krystaliczna i uwalniają się kationy i aniony. Na przykład sól (chlorek potasu) topi się w temperaturze równej i w trakcie tego procesu uwalniane są kationy potasu i aniony chlorkowe ze struktury krystalicznej.
Azotan() strontu to sól, która znalazła zastosowanie pirotechnice jako składnik między innymi sztucznych ogni. Zapisz równanie reakcji otrzymywania tej soli za pomocą metody zobojętniania.
Korzystając z tabeli rozpuszczalności zamieszczonej poniżej, dopasuj wymienione sole do odpowiedniej grupy.