Jak są zbudowane i jak otrzymać kwasy?
Co to są kwasy?
Kwasy to związki chemiczne, które definiowane są na wiele sposobów. Klasyfikacji dokonuje się na podstawie danej teorii. Na przykład wg teorii Arrheniusa kwasy to substancje, które w roztworze wodnym dysocjują na kation wodoru i anion reszty kwasowej. Z kolei wg teorii Brønsteda–Lowry’ego są donorami (dawcami) protonów, a według teorii Lewisa kwasy przyjmują parę elektronową. Jednak wszystkie znane kwasy nieorganiczne oznaczane są następującym wzorem ogólnym:
Gdzie oznacza resztę kwasową, a – indeks stechiometryczny, oznaczający ilość atomów wodoru w cząsteczce kwasu.
Jeżeli pod literą kryje się grupa atomów zawierająca – poza innymi pierwiastkami – atom tlenu, wówczas kwas określa się jako tlenowy, tzw. oksokwas. Natomiast jeżeli stanowi atom niemetalu, kwas jest beztlenowy.
- Nazwa kategorii: Reszta kwasowa [italic]R[/]
- Nazwa kategorii: atom niemetalu
- Nazwa kategorii: kwas beztlenowy Koniec elementów należących do kategorii atom niemetalu
- Nazwa kategorii: grupa atomów zawierająca tlen oraz przynajmniej jeden inny pierwiastek chemiczny
- Nazwa kategorii: kwas tlenowy Koniec elementów należących do kategorii grupa atomów zawierająca tlen oraz przynajmniej jeden inny pierwiastek chemiczny
- Elementy należące do kategorii Reszta kwasowa [italic]R[/]
- Elementy należące do kategorii atom niemetalu
- Elementy należące do kategorii grupa atomów zawierająca tlen oraz przynajmniej jeden inny pierwiastek chemiczny
Kwasy beztlenowe
Kwasy beztlenowe to wodne roztwory wodorków niemetali, należących do 16. oraz 17. grupy układu okresowego.
Wzór kwasu | Nazwa kwasu |
|---|---|
kwas siarkowodorowy | |
kwas selenowodorowy | |
kwas tellurowodorowy | |
kwas fluorowodorowy | |
kwas chlorowodorowy (zwyczajowa nazwa: kwas solny) | |
kwas bromowodorowy | |
kwas jodowodorowy |
Wzory elektronowe kreskowe wodorków tworzących kwasy beztlenowe przedstawia się w następujący sposób:

Niektóre z kwasów beztlenowych są zbudowane z innych niemetali i mają bardziej złożoną budowę, np. kwas cyjanowodorowy () oraz kwas tiocyjanowy (inaczej kwas rodanowodorowy ), w związku z tym posiadają następujące wzory elektronowe kreskowe:

Ze względu na różnicę elektroujemności pomiędzy atomami, w wodorkach, tworzaących kwasy beztlenowe, pomiędzy atomem (atomami) wodoru a atomem niemetalu występują wiązania kowalencyjne spolaryzowane:
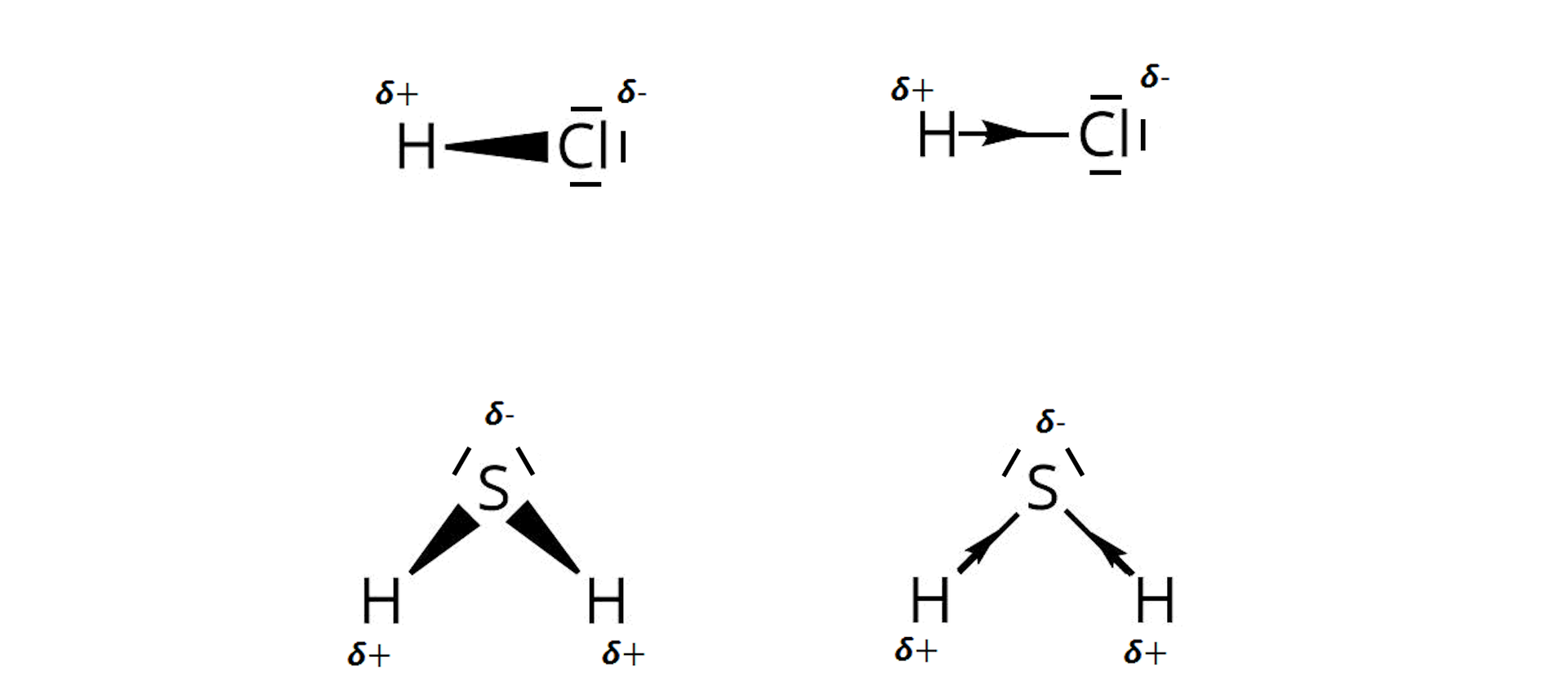
Kwasy tlenowe
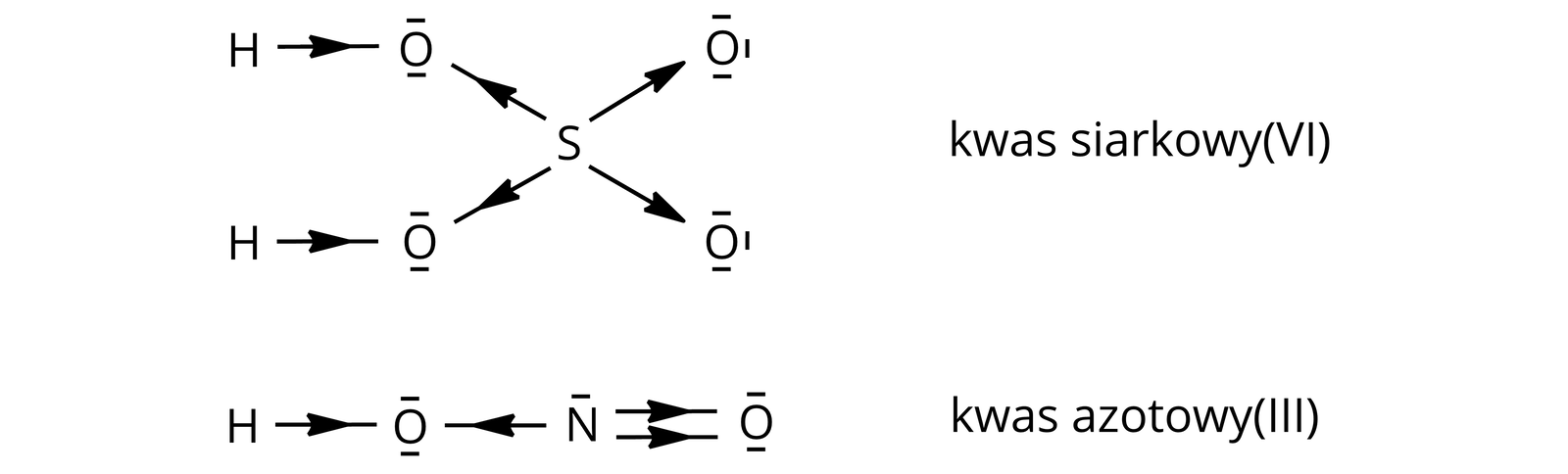
Kwasy tlenowe (oksokwasy) zawierają przynajmniej jeden atom wodoru, związany z atomem tlenu, oraz atom (atomy) innego pierwiastka chemicznego. Pierwiastkami chemicznymi w kwasach tlenowych są zazwyczaj niemetale, ale również metale na wysokich stopniach utlenienia, np. lub , które stanowią atomy centralne w cząsteczkach kwasów.
Wzór kwasu | Nazwa kwasu |
|---|---|
| kwas siarkowy() |
kwas azotowy() | |
kwas azotowy() | |
kwas chlorowy() | |
kwas chlorowy() | |
kwas chlorowy() | |
kwas chlorowy() | |
kwas jodowy() | |
kwas fosforowy() | |
kwas arsenowy() | |
| kwas węglowy |
kwas ortokrzemowy | |
kwas metakrzemowy | |
kwas ortoborowy | |
kwas chromowy() | |
kwas dichromowy() | |
kwas manganowy() |
Zapoznaj się z filmem i odpowiedz na pytania.

Film dostępny pod adresem /preview/resource/RLmv5mzXNqPXe
Film nawiązujący do treści materiału - dotyczy podziału kwasów nieorganicznych.
Jaki stopień utlenienia ma atom siarki w cząsteczce ?
Podaj nazwę wg systemu Stocka dla wodnego roztworu siarkowodoru.
Jak wg Systemu Stocka brzmi nazwa kwasu ?
Jak otrzymać kwasy?
Czy zastanawiasz się czasem, skąd biorą się kwasy spotykane w chemii i codziennym życiu? Poznanie metod ich otrzymywania to nie tylko sposób na zrozumienie wielu reakcji chemicznych, ale także okazja do uporządkowania wiedzy o właściwościach różnych substancji. Dzięki temu łatwiej jest pojąć, dlaczego jedne kwasy powstają z gazów, inne z tlenków, a jeszcze inne z soli. To fascynujący temat, który warto poznać bliżej!
Reakcja wodorków niemetali z wodą
Metoda ta pozwala na otrzymanie wodnych roztworów kwasów beztlenowych. Dobrze działa w przypadku wodorków, które są rozpuszczalnymi w wodzie gazami, a w cząteczkach których występuje silna polaryzacja wiązań umożliwiająca łatwe oderwanie jonu wodoru.
wodorek niemetalu + H₂O → kwas beztlenowy
HCl Indeks dolny (g)(g) + HIndeks dolny 22O → HCl Indeks dolny (aq)(aq) (kwas chlorowodorowy)
HIndeks dolny 22S Indeks dolny (g)(g) + HIndeks dolny 22O → HIndeks dolny 22S Indeks dolny (aq)(aq) (kwas siarkowodorowy)
Reakcja tlenków kwasotwórczych z wodą
W kontekście otrzymywania kwasów, można wyróżnić tlenki, które mają charakter kwasowy i jednocześnie reagują z wodą. To właśnie te tlenki, w wyniku reakcji z wodą tworzą kwasy.
Potrafisz podać przykład reakcji tlenku z wodą, w wyniku której otrzymasz kwas tlenowy? Umiesz zaplanować takie doświadczenie? W jaki sposób potwierdzisz, że otrzymanym produktem jest kwas? Przeprowadź eksperyment w wirtualnym laboratorium, a na pewno udzielisz odpowiedzi na powyższe pytania. Zapoznaj się z problemem badawczym, zaproponuj hipotezę, zanotuj obserwacje i wyniki oraz sformułuj wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBMAS4FTQ
Potrafisz podać przykład reakcji tlenku z wodą w wyniku której otrzymasz kwas tlenowy? Umiesz zaplanować takie doświadczenie? W jaki sposób potwierdzisz, że otrzymanym produktem jest kwas? Zapoznaj się z opisem doświadczenia, a na pewno będziesz znał odpowiedź na powyższe pytania. Zapoznaj się z problemem badawczym, hipotezą, obserwacjami i wynikami oraz sformułowanymi wnioski.
Analiza eksperymentu:
Otrzymywanie kwasów tlenowych w wyniku reakcji odpowiednich tlenków z wodą.
Problem badawczy:
Czy w wyniku reakcji tlenku z wodą można otrzymać kwas tlenowy?
Hipoteza:
W wyniku reakcji tlenku z wodą można otrzymać kwas tlenowy.
Sprzęt laboratoryjny:
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
pipety – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczki – długie trzonki wykonane ze szkła, porcelany lub metalu zakończone z jednej strony łyżeczką.
Odczynniki chemiczne:
wskaźnik uniwersalny; tlenek siarki(); suchy lód; tlenek fosforu(); tlenek krzemu().
Przebieg eksperymentu:
1. Umieszczenie w probówce trzech centymetrów sześciennych wody ze wskaźnikiem uniwersalnym.
2. Przez roztwór w probówce przepuszczono gazowy tlenek siarki().
3. Doświadczenie powtórzono dla pozostałych trzech tlenków wsypując je do roztworu wody ze wskaźnikiem uniwersalnym
Obserwacje:
W probówkach do których dodano: tlenek siarki(), suchy lód oraz tlenek fosforu() roztwór zmienił barwę z zielonego na czerwone. Natomiast w probówce z tlenkiem krzemu() brak zmian.
Wyniki:
W probówkach, w których znalazły się tlenki: siarki(), węgla() oraz fosforu() doszło do spadku pH. W przypadku probówki z tlenkiem krzemu() nie doszło do zmian pH.
Wnioski:
W probówkach, w których nastąpiła zmiana koloru z zielonej na czerwoną jako produkt powstał kwas. Za zmianę zabarwienia odpowiada wskaźnik uniwersalny, który w środowisku kwasowym przyjmuje czerwone zabarwienie. Tlenek krzemu() nie reaguje z wodą, brak widocznych objawów reakcji. Tlenek siarki(), zestalony tlenek węgla() oraz tlenek fosforu() reagują z wodą w wyniku czego powstają odpowiednie kwasy tlenowe. Hipoteza została potwierdzona.
Dlaczego w powyższym doświadczeniu wykorzystujemy wskaźnik kwasowo‑zasadowy?
Reakcje tlenków kwasotwórczych z wodą biegną według następującego schematu:
W wyniku reakcji chemicznej tlenku kwasotwórczego z wodą powstaje odpowiedni kwas tlenowy.
Zapisz równanie reakcji tlenku siarki() z wodą w formie cząsteczkowej.
Wzór tlenku:
Równanie reakcji z wodą:
W wyniku reakcji tlenku siarki() z wodą powstaje kwas siarkowy().
Jak łatwo zauważyć, stopień utlenienia atomu siarki w wyniku reakcji nie zmienia się.
Zapisz równanie reakcji otrzymywania kwasu fosforowego() z odpowiedniego tlenku i wody w formie cząsteczkowej. Zapisz wzór tlenku.
Wzór kwasu:
Stopień utlenienia atomu fosforu:
Wzór tlenku:
Równanie reakcji:
Tlenek węgla() jest bezwodnikiem kwasu węglowego. Kwas węglowy jest kwasem nietrwałym, dlatego też reakcja ta jest odwracalna. Zapisz równanie reakcji tlenku węgla() z wodą.
Równanie reakcji:
Ze względu na nietrwałość kwasu węglowego równanie reakcji zapisywane jest z dwiema strzałkami (reakcja odwracalna).
Otrzymywanie kwasu przez wypieranie go z jego soli
Kwasy, których nie da się otrzymać w wyniku reakcji odpowiedniego tlenku z wodą, otrzymuje się zazwyczaj z ich soli. Na taką sól działa się innym mocnym kwasem (mocniejszym, niż ten wypierany), w wyniku czego interesujący nas kwas zostaje wyparty z soli.
W wirtualnym laboratorium otrzymaj wybrany przez siebie kwas metodą wypierania go ze swojej soli. Zapoznaj się z problemem badawczym oraz postaw hipotezę badawczą. Sporządź notatkę, w której zapiszesz własne obserwacje, wyniki i wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBMAS4FTQ
Zadanie: jak otrzymać kwas poprzez wypieranie go z soli.
Analiza eksperymentu: Otrzymywanie kwasu poprzez wypieranie go z jego soli.
Problem badawczy: Czy w reakcji soli z mocnym kwasem zawsze dochodzi do powstania innego kwasu?
Hipoteza: Powstanie kwasu następuje jedynie w wyniku reakcji soli słabego kwasu z mocnym kwasem.
Sprzęt laboratoryjny: probówki - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych; pipety - wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki; statyw na probówki - prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki.
Odczynniki chemiczne: kwas chlorowodorowy; siarczek sodu (ciało stałe); siarczan(IV) potasu (ciało stałe); węglan wapnia (ciało stałe); siarczan(VI) baru (ciało stałe).
Przebieg eksperymentu: Do każdej z probówek dodano małą ilość soli zgodnie z kolejnością położenia na półce. Następnie dodano kwas chlorowodorowy. Probówkę z siarczkiem sodu oraz siarczanem(IV) potasu dodatkowo podgrzewano.
Obserwacje: W probówkach z siarczan(IV) potasu, siarczkiem sodu i węglanem wapnia ciała stałe uległy roztworzeniu, wydzieliły się bezbarwne gazy. Gaz wydzielający się z probówki z węglanem był bezwonny, z probówki z siarczkiem sodu - miał charakterystyczny zapach zgniłych jaj, a z probówki z siarczanem(IV) potasu - charakterystyczny drażniący zapach. W probówce z siarczanem(VI) baru nie zaobserwowano zmian.
Wyniki: W przypadku węglanu wapnia, siarczku sodu i siarczanu(IV) potasu doszło do reakcji z kwasami, czego efektem było wydzielanie się gazów. W przypadku siarczanu(VI) baru nie zaobserwowano żadnej reakcji z kwasami.
Wnioski: Kwas chlorowodorowy jest kwasem mocniejszym od kwasu siarkowego(IV), węglowego i siarkowodorowego dlatego wypiera je z ich soli oraz roztworów ich soli. Nie wypiera jednak kwasu siarkowego(VI), który to jest kwasem mocnym. Hipoteza została potwierdzona.
Równania reakcji chemicznej: 1. Węglan wapnia z kwasem chlorowodorowym: jedna cząsteczka węglanu wapnia + dwie cząsteczki chlorowodoru dają jedną cząsteczkę chlorku wapnia + jedną cząsteczkę wody + jedną cząsteczkę dwutlenku węgla. 2. Siarczek sodu z kwasem chlorowodorowym: jedna cząsteczka siarczku sodu + dwie cząsteczki chlorowodoru daje dwie cząsteczki chlorku sodu + jedna cząsteczka siarkowodoru. 3. Siarczan(IV) potasu z kwasem chlorowodorowym: jedna cząsteczka siarczanu(IV) potasu + dwie cząsteczki chlorowodoru daje dwie cząsteczki chlorku potasu + jedna cząsteczka wody + jedna cząsteczka dwutlenku siarki. 4. Siarczan(VI) baru z kwasem chlorowodorowym: reakcja nie zachodzi.
Wypierany kwas jest słabszy niż kwas działający na sól. Reakcja przebiega według schematu:
sól słabego kwasu + mocny kwas → słaby kwas + sól mocnego kwasu
Gdy do roztworu octanu sodu () doda się kwas solny (np. ), to równanie omawianej reakcji chemicznej wygląda następująco:
Jak widać, w wyniku powyższej reakcji otrzymano chlorek sodu oraz kwas octowy (etanowy). Octan (etanian) sodu jest solą złożoną z kationu metalu oraz anionu reszty kwasu octowego, który jest słabym kwasem ( = 1,8 · 10Indeks górny -5-5). Natomiast kwas solny jest kwasem mocnym ( = 1,0 · 10Indeks górny 77; ) , który wyparł kwas słabszy (kwas octowy) z roztworu jego soli.