Dlaczego woda ma niezwykłe właściwości?
Woda w czasach greckich filozofów była traktowana jako niepodzielna cząstka. Stanowiła jeden z czterech pierwiastków, które tworzyły otaczający nas świat.

Tak mijały lata aż do 1784 r., w którym to brytyjski chemik i fizyk, Henry Cavendish, odkrył, że woda jest związkiem chemicznym, a nie pierwiastkiem.

W 1886 r. August Wilhelm von Hofmann skonstruował aparat Hofmanna, dzięki któremu dowiódł, że woda ulega rozkładowi na dwie cząsteczki wodoru oraz jedną cząsteczkę tlenu.

Woda jako związek chemiczny

Woda zajmuje 2/3 powierzchni naszej planety. Poza ocenami i morzami jest ona również składnikiem atmosfery i środowiska lądowego. Całość wody na naszej planecie określamy mianem hydrosfery.
Woda, która nadaje się do picia, nazywana jest wodą słodką – niestety stanowi ona zaledwie 3% całkowitej ilości wody na Ziemi, z czego tylko ¼ to wody dostępne dla ludzi. Reszta znajduje się w postaci lodu. Dlatego tak ważne jest jej oszczędzanie.
Kąt między wiązaniami wynosi 104,5°, co oznacza, że orbitale walencyjne atomu tlenu w cząsteczce wody wykazują hybrydyzację . Atom tlenu posiada dodatkowo dwie wolne pary elektronowe.
Elektroujemność tlenu wg skali Paulina wynosi 3,44, a atomu wodoru 2,20. Zatem różnica wartości elektroujemności atomów, które tworzą wiązanie, wynosi 1,24 – a zatem w cząsteczce wody występuje wiązanie kowalencyjne spolaryzowane. Moment dipolowy cząsteczki wody wynosi 1,86 D. Jest więc ona cząsteczką polarną.
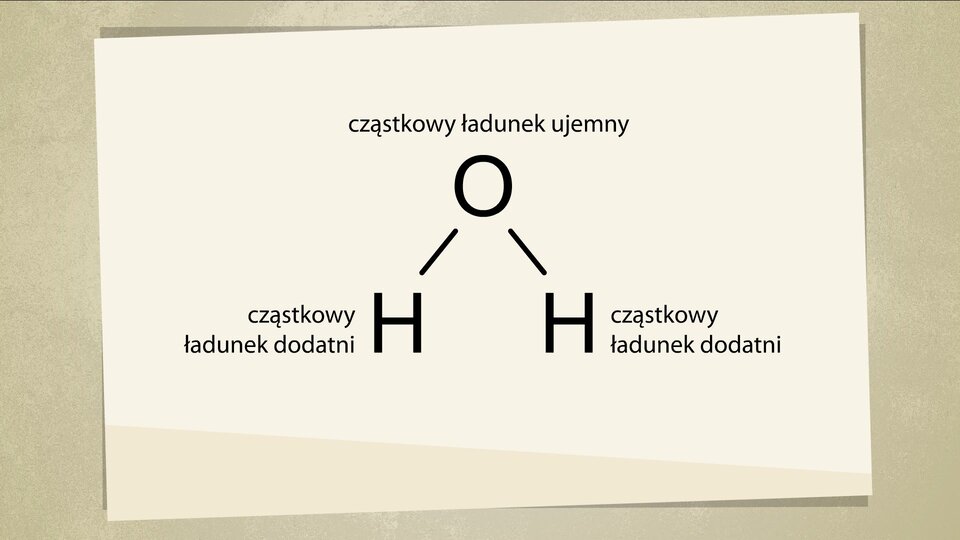
Na grafice został przedstawiony rozkład ładunków w cząsteczce wody. Kolorami ciepłymi (pomarańczowy, czerwony) został zaznaczony obszar z ładunkiem ujemnym, a kolorami zimnymi (niebieski) obszar z ładunkiem dodatnim.

W cząsteczkach, w których występuje polaryzacja wiązania X‑H, atom X jest atomem bardziej elektroujemnym niż atom wodoru, w związku z czym zyskuje cząstkowy ładunek ujemny. Skutkiem tego jest możliwość oddziaływania atomu wodoru z atomem innej cząsteczki, w której następuje nagromadzenie się ładunku ujemnego Y. Schematycznie można to zapisać:
Zaznaczone kropkami oddziaływanie pomiędzy atomem wodoru a atomem Y oznacza wiązanie wodorowe.
To właśnie dzięki występowaniu wiązań wodorowych w cząsteczce wody wykazuje ona dużo większą temperaturę wrzenia i topnienia niż inne wodorki należące do 16. grupy układu okresowego.
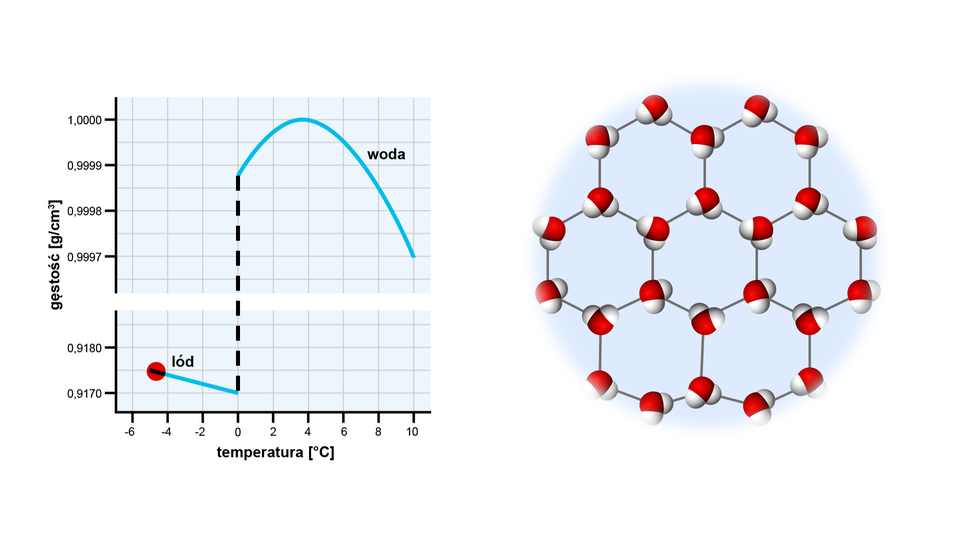
![Sieć wiązań wodorowych między cząsteczkami wody. [https://ep2019.contentplus.io/!/project/design/P1AI0Kmmp/comment/DBqNCeZSz lekcja 0084]. Na ilustracji są liczne cząsteczki zbudowane z jednej czerwonej kulki i dwóch białych. Pomiędzy czerwonymi kulkami jednych cząsteczek a białymi kolejnych poprowadzono linie przerywane.](https://static.zpe.gov.pl/portal/f/res-minimized/RN6SoiJY0rlss/1618580911/1r4OzDualdNYdsItC2zznFj0t3peMkJh.png)
Woda w stanie stałym, nazywanym lodem, może w zależności od warunków występować w aż dziewięciu odmianach. Lód, który powstaje pod ciśnieniem 1 atmosfery i w temperaturze 0°C, nazywamy lodem Ih. Długość wiązań wodorowych w ciekłej wodzie wynosi ok. 1,89 Å. Ciekła woda charakteryzuje się dość dużą ruchliwością cząsteczek – mogą się one do siebie przybliżać bądź oddalać. W przypadku fazy stałej lodu, ten ruch jest zahamowany.
Wynika z tego kolejna właściwość wody – podczas krzepnięcia zwiększa swoją objętość. Gęstość lodu wynosi 0,917 , dlatego unosi się on na wodzie. Jest to cecha bardzo ważna dla organizmów żyjących w zbiornikach wody. Największą gęstość woda posiada w temperaturze 4°C i wynosi 1 . Opadając na dno zbiornika, dostarcza tlenu organizmom wodnym.
Kolejną charakterystyczną cechą wody jest wysokie ciepło parowania, które wynosi 40,66 . Ciepło parowania to ilość energii, jaką trzeba dostarczyć, aby określona substancja przeszła ze stanu ciekłego w stan pary. Jest określona w jednostkach energii J na jednostkę masy bądź na mol substancji.
Woda zawdzięcza swoje niezwykłe (anomalne) właściwości dzięki występowaniu wiązań wodorowych.
Dlaczego woda wykazuje niezwykłe właściwości?
Zapoznaj się z poniższym filmem, a następnie rozwiąż zadania.
Uwaga! Doświadczenia omówione w filmie samouczku mają tylko charakter pokazowy i były wykonywane przez doświadczone osoby – nie próbuj wykonywać ich samodzielnie.
Film dostępny pod adresem /preview/resource/R1Am1M5mxPp9E
Film nawiązujący do treści materiału - dotyczy wody - podstawy życia, co decyduje o jej niezwykłości.
Co sprawia, że wodę cechuje duże ciepło właściwe?
Wyjaśnij, dlaczego zimą woda nie zamarza na dnie większych zbiorników? Jakie to ma znaczenie dla żyjących tam organizmów wodnych?
Obejrzyj poniższy film, a następnie narysuj lub zbuduj, przy użyciu modeli pręcikowo‑kulkowych lub plasteliny, model cząsteczki wody (ze wskazaniem cząstkowych ładunków delta+ oraz delta-).
Wpływ polarnej budowy cząsteczek wody na jej gęstość
Polarna budowa cząsteczek wody ma swoje konsekwencje – są nimi właściwości fizyczne wody. Zazwyczaj jest tak, że w ciele stałym drobiny znajdują się bliżej siebie niż w cieczy i substancja w stanie stałym ma większą gęstość niż w stanie ciekłym. W przypadku wody, cząsteczki w fazie stałej tworzą struktury, które pozostawiają dużo wolnej przestrzeni, przez co odległości między cząsteczkami są większe w lodzie niż w wodzie ciekłej. Z tego powodu lód ma mniejszą gęstość niż woda ciekła.

Lód ma mniejszą gęstość niż woda ciekła i dlatego unosi się na jej powierzchni
Film dostępny pod adresem /preview/resource/Rcxttq8WnzY0s
W animacji przedstawiono cząsteczkę wody i omówiono, czym spowodowana jest jej polarność.
Stan skupienia | Gęstość |
woda w stanie stałym w temperaturze 0 °C | |
woda w stanie ciekłym w temperaturze około 4 °C |
Niska, w stosunku do gęstości ciekłej wody, gęstość lodu ma bardzo ważne znaczenie dla istnienia życia wodnego na Ziemi. Lód, który tworzy się na powierzchni wody, izoluje jej głębsze warstwy i chroni przed zamarzaniem. Umożliwia w ten sposób egzystencję organizmom wodnym w czasie mrozów.

W mroźne dni lód chroni życie wodne w zbiorniku. Pod nim temperatura wody wynosi zawsze około 0 °C, a na dnie zaś sięga około 4 °C
Woda występuje w trzech stanach skupienia. Jest to 1. jonowych, 2. 100, 3. niespolaryzowanych, 4. ciecz i ciało stałe, 5. spolaryzowanych, 6. dwóch, 7. ciecz, gaz i ciało stałe, 8. 0, 9. 4. Woda ma największą gęstość w temperaturze 1. jonowych, 2. 100, 3. niespolaryzowanych, 4. ciecz i ciało stałe, 5. spolaryzowanych, 6. dwóch, 7. ciecz, gaz i ciało stałe, 8. 0, 9. 4°C.
