Rozpuszczalność
Rozpuszczanie
Substancje stałe, ciekłe lub gazowe różnią się zdolnościami do tworzenia z innymi substancjami układów homogenicznychukładów homogenicznych. Rozpuszczanie to fizyczny proces mieszania się dwóch substancji, prowadzący do otrzymania roztworu.
Efekty towarzyszące procesowi rozpuszczania to np. zmiana temperatury i zmiana objętości roztworu (zjawisko dylatacji dylatacji lub kontrakcjikontrakcji). W czasie rozpuszczania następuje solwatacja, czyli otaczanie cząsteczek (lub jonów) substancji rozpuszczonej przez cząsteczki rozpuszczalnika. Solwatację w roztworach wodnych nazywamy hydratacją.
Rozpuszczalność
Rozpuszczalność jest cechą danej pary substancji rozpuszczanej i rozpuszczalnika w określonej temperaturze. Na ogół ilość substancji, którą można rozpuścić w danej ilości rozpuszczalnika i w określonej temperaturze, jest ograniczona i prowadzi do uzyskania tzw. roztworu nasyconegoroztworu nasyconego. Ilość substancji niezbędnej do uzyskania roztworu nasyconego określa wielkość fizyczna zwana rozpuszczalnością.
Rozpuszczalność substancji zależy od:
rodzaju substancji rozpuszczonej;
rodzaju rozpuszczalnika;
temperatury (rozpuszczalność większości ciał stałych i cieczy rośnie wraz ze wzrostem temperatury, a rozpuszczalność gazów maleje);
ciśnienia – tylko dla gazów (ich rozpuszczalność rośnie wraz ze wzrostem ciśnienia oraz od wpływu wspólnego jonu);
Rozpuszczalność to liczba gramów danej substancji niezbędna do nasycenia 100 g rozpuszczalnika w danej temperaturze.
Poniższa tabela przedstawia rozpuszczalność wybranych substancji w 100 g wody i w temperaturze 25ºC.
Sól | Rozpuszczalność |
|---|---|
Rozpuszczalność gazów
Przeanalizuj poniższą symulację. Zwróć uwagę, jak zmiana temperatury oraz ciśnienia wpływa na rozpuszczalność tlenku węgla() w wodzie. Następnie rozwiąż ćwiczenia sprawdzające.
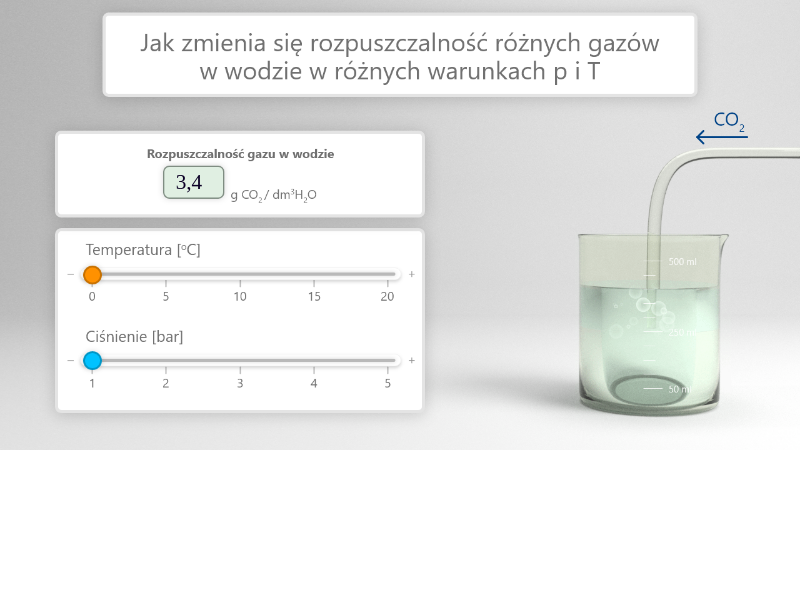
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DCXR45UPP
Rozpuszczalność gazów zależy od ciśnienia i rośnie wraz z jego wzrostem. Podobnie jak różny wpływ wywiera temperatura na rozpuszczalność, tak wzrost ciśnienia może powodować znaczne zwiększenie rozpuszczalności, tak jak dla dwutlenku węgla, bądź nie powodować tak dużych zmian, jak w przypadku tlenu.

Czym jest krzywa rozpuszczalności i jak odczytać z niej rozpuszczalność substancji?
Wykres przedstawiający zależność rozpuszczalności danej substancji od temperatury nazywa się krzywą rozpuszczalności.
Odczytaj z wykresu rozpuszczalność chlorku sodu () w temperaturze 90°C przy stałym ciśnieniu.
Zapoznaj się z opisem wykresu. Dowiesz się, jaka jest rozpuszczalność chlorku sodu (NaCl) w temperaturze 90°C przy stałym ciśnieniu.
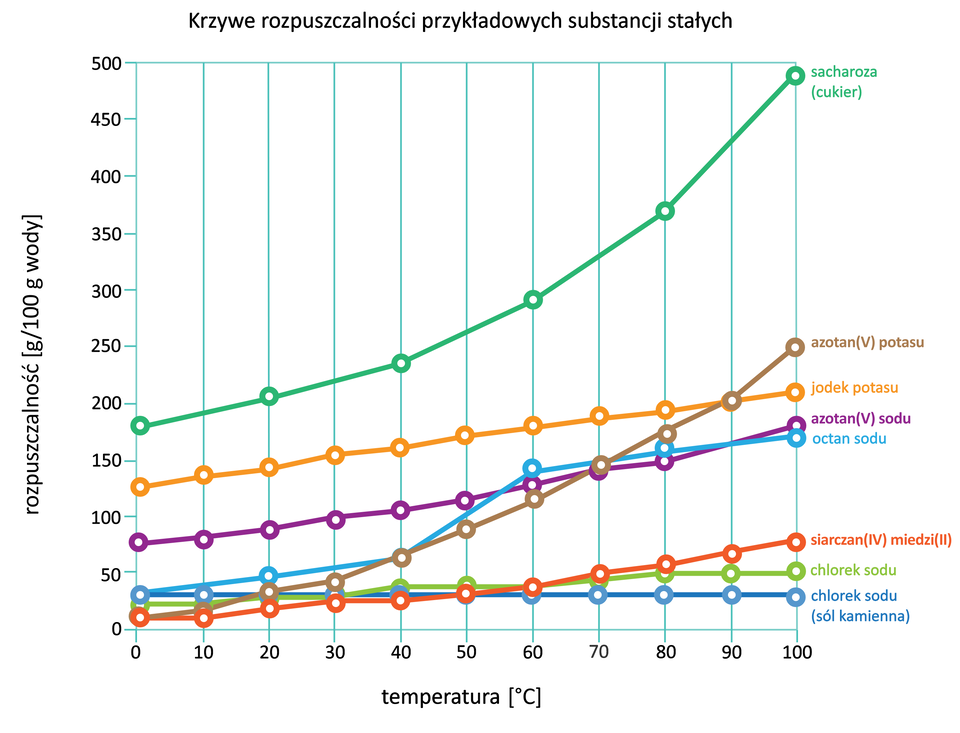
Interpretacja danych z wykresu rozpuszczalności
Ile gramów azotanu(V) sodu należy rozpuścić w 100 g wody, aby w temperaturze 40°C otrzymać roztwór nasycony?

Czynniki wpływające na szybkość rozpuszczania
Zmierzono czas rozpuszczania cukru w zimnej i gorącej wodzie. W tym celu do dwóch jednakowych naczyń wlano identyczną objętość wody. Do jednego – zimną wodę z kranu, a do drugiego – gorącą wodę. Do każdego z nich wrzucono łyżeczkę cukru. Zamieszano zawartość każdego naczynia. Porównano szybkość rozpuszczania cukru w obu naczyniach.
W naczyniu z gorącą wodą kryształy cukru rozpuszczały się szybciej.
Przedstawiona symulacja prezentuje wpływ różnych czynników na szybkość rozpuszczania substancji. Przeanalizuj, jaki wpływ na ten proces mają temperatura, mieszanie i rozdrobnienie, a następnie rozwiąż zadania.
Zapoznaj się z opisem symulacji, która prezentuje wpływ różnych czynników na szybkość rozpuszczania substancji. Następnie rozwiąż zadania.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DCXR45UPP
Symulacja interaktywna przedstawia laboratorium, w którym przedstawiony został wpływ temperatury, mieszania oraz rozdrobnienia na szybkość rozpuszczania substancji w wodzie. W laboratorium do wykorzystania możliwe są trzy substancje: sacharoza (), chlorek sodu () oraz uwodniony siarczan miedzi ().
Sacharoza ():
Temperatura:
Na stole w laboratorium znajdują się dwie zlewki z wodą. W pierwszej zlewce znajduje się woda w temperaturze , a w drugiej zlewce znajduje się woda w temperaturze . Obok każdej ze zlewek znajduje się szalka, na której przygotowano po sacharozy.
Sacharoza zostaje wsypana do zlewek jednocześnie.
Obserwacje: W zlewce z wyższą temperaturą sacharoza rozpuszcza się już po minutach, a w zlewce z niższą temperaturą dopiero po upływie godziny.Mieszanie:
Na stole w laboratorium znajdują się dwie zlewki z wodą o temperaturze , obok każdej z nich znajduje się szalka z pięcioma gramami sacharozy.
Substancja zostaje umieszczona w wodzie jednocześnie. W jednej ze zlewek wymieszano substancję przy użyciu szklanej bagietki.
Obserwacje: W zlewce, w której wymieszano substancje, sacharoza rozpuszcza się po minutach, a zlewce drugiej po około godzinie.Rozdrobnienie:
Na stole w laboratorium znajdują się dwie zlewki z wodą o temperaturze , obok każdej z nich znajduje się szalka z pięcioma gramami sacharozy. Na jednej szalce znajduje się rozdrobiona sacharoza, a na drugiej substancja w postaci większych kryształów.
Substancja zostaje umieszczona w wodzie jednocześnie.
Obserwacje: W zlewce, w której umieszczono rozdrobnioną sacharozę substancja rozpuszcza się po około minutach, podczas gdy rozpuszczenie się większych kryształów zajmuje około godziny.
Chlorek sodu ():
Temperatura:
Na stole w laboratorium znajdują się dwie zlewki z wodą. W pierwszej zlewce znajduje się woda w temperaturze , a w drugiej zlewce znajduje się woda w temperaturze . Obok każdej ze zlewek znajduje się szalka, na której przygotowano po chlorku sodu.
Substancja zostaje wsypana do zlewek jednocześnie.
Obserwacje: W zlewce z wyższą temperaturą chlorek sodu rozpuszcza się już po minutach, a w zlewce z niższą temperaturą dopiero po upływie godziny.Mieszanie:
Na stole w laboratorium znajdują się dwie zlewki z wodą o temperaturze , obok każdej z nich znajduje się szalka z pięcioma gramami chlorku sodu.
Substancja została umieszczona w wodzie jednocześnie. W jednej ze zlewek wymieszano substancję przy użyciu szklanej bagietki.
Obserwacje: W zlewce, w której wymieszano substancje, chlorek sodu rozpuszcza się po minutach, a zlewce drugiej po około godzinie.Rozdrobnienie:
Na stole w laboratorium znajdują się dwie zlewki z wodą o temperaturze , obok każdej z nich znajduje się szalka z pięcioma gramami chlorku sodu. Na jednej szalce znajduje się rozdrobiona substancja, a na drugiej substancja w postaci większych kryształów. Chlorek sodu zostaje umieszczony w wodzie jednocześnie.
Obserwacje: W zlewce, w której umieszczono rozdrobnioną substancję, rozpuszcza się ona po około minutach, podczas gdy rozpuszczenie się większych kryształów zajmuje około godziny..
Uwodniony siarczan miedzi ():
Temperatura:
Na stole w laboratorium znajdują się dwie zlewki z wodą. W pierwszej zlewce znajduje się woda w temperaturze , a w drugiej zlewce znajduje się woda w temperaturze . Obok każdej ze zlewek znajduje się szalka, na której przygotowano po uwodnionego siarczanu miedzi.
Substancja zostaje wsypana do zlewek jednocześnie.
Obserwacje: W zlewce z wyższą temperaturą uwodniony siarczan miedzi rozpuszcza się już po minutach zabarwiając roztwór na kolor niebieski, a w zlewce z niższą temperaturą dopiero po upływie godziny.Mieszanie:
Na stole w laboratorium znajdują się dwie zlewki z wodą o temperaturze , obok każdej z nich znajduje się szalka z pięcioma gramami uwodnionego siarczanu miedzi.
Substancja została umieszczona w wodzie jednocześnie. W jednej ze zlewek wymieszano substancję przy użyciu szklanej bagietki.
W zlewce, w której wymieszano substancje, uwodniony siarczan miedzi rozpuszcza się po minutach, a zlewce drugiej po około godzinie.Rozdrobnienie:
Na stole w laboratorium znajdują się dwie zlewki z wodą o temperaturze , obok każdej z nich znajduje się szalka z pięcioma gramami uwodnionego siarczanu miedzi. Na jednej szalce znajduje się rozdrobiona substancja, a na drugiej substancja w postaci większych kryształów. Uwodniony siarczan miedzi zostaje umieszczony w wodzie jednocześnie.
Obserwacje: W zlewce, w której umieszczono rozdrobnioną substancję, rozpuszcza się ona po około minutach barwiąc roztwór na kolor niebieski, podczas gdy rozpuszczenie się większych kryształów zajmuje około godziny.

