Podsumowanie wątku 2
Wejdź na wyższy poziom
Wykrywanie cukrów prostych
Redukujące właściwości aldoz (np. glukozy, galaktozy, rybozy) oraz ketoz (np. fruktozy, rybulozy) wykorzystuje się do wykrywania tych cukrów w reakcjach charakterystycznych:
ze świeżo strąconym wodorotlenkiem miedzi(II) – z odczynnikami Fehlinga, Trommera;
z siarczanem(VI) miedzi(II) (solą) – z odczynnikiem Benedicta;
z amoniakalnym roztworem tlenku srebra(I) – z odczynnikiem Tollensa.
Próba Fehlinga

Próba ta służy do wykrywania związków o właściwościach redukujących, mających grupę aldehydową, m.in. cukrów – aldoz. Fruktoza, mimo że jest ketozą, w roztworze zasadowym łatwo przechodzi w glukozę lub mannozę, dlatego jej obecność również może być wykryta za pomocą tej reakcji. Z odczynnikiem Fehlinga reagują niektóre dwucukry, np. maltoza i laktoza.
Do wykonania reakcji potrzebne są dwa odczynniki, łączone dopiero podczas wykonywania próby. Odczynnik Fehling I to roztwór kwasu siarkowego i siarczanu(VI) miedzi(II). Fehling II zawiera roztwór wodorotlenku sodu i winianu sodowo‑potasowego. Kiedy oba płyny zmiesza się w równej objętości, powstaje klarowny roztwór o szafirowej barwie. W następnym kroku do płynu dodaje się badaną substancję i całość ogrzewa – krótko nad palnikiem lub kilka minut w łaźni wodnej. Jeśli pojawi się ceglastopomarańczowy osad, świadczy to o obecności cukrów redukujących. W próbie Fehlinga jony miedzi(II) są redukowane przez glukozę do nierozpuszczalnych tlenków miedzi(I), a glukoza utlenia się do kwasu glukonowego (glukonianu).
Próba Trommera
Próba Trommera także polega na wykrywaniu związków z grupą aldehydową, dzięki ich właściwościom redukującym. Pod wpływem wodorotlenku miedzi(II) zachodzi reakcja redoks, prowadząca do utlenienia aldehydów do kwasów karboksylowych i zredukowania miedzi z II stopnia utlenienia do I. Wykonanie próby polega na ogrzewaniu wodorotlenku miedzi(II) z próbką. W przypadku obecności aldehydów niebieski osad (Cu(OH)Indeks dolny 22) zmienia zabarwienie na ceglastoczerwone (CuIndeks dolny 22O).
Próba Tollensa

W próbie Tollensa czynnikiem powodującym utlenienie glukozy jest amoniakalny roztwór tlenku srebra(I). W wyniku szeregu reakcji następuje wytrącenie metalicznego srebra (powstanie lustra srebrowego) na ściankach probówki. W ten sposób wytwarza się lustra do użytku domowego, a także srebrzy się wnętrze bombek choinkowych i termosów.
Próba Benedicta

W specyficznej dla cukrów redukujących i bardzo czułej reakcji Benedicta (pozwalającej wykryć glukozę w stężeniu nawet 0,1%) jako odczynnik stosuje się siarczan(VI) miedzi(II) z węglanem sodu i cytrynianem sodu. Tak jak w próbie Fehlinga tworzy się rozpuszczalny kompleks miedziowy, który ulega rozpadowi z wytworzeniem nierozpuszczalnego tlenku miedzi(I). Jego zabarwienie (od zielonego przez żółtawe do czerwonego) zależy od ilości cząstek cukru w roztworze i na tej podstawie można ocenić procentowe stężenie glukozy w badanej próbce. Barwa zielona jest wynikiem nakładania się pomarańczowej barwy tlenku miedzi(I) na szafirową barwę odczynnika.
Przeprowadź doświadczenie w laboratorium biologicznym w celu wykrycia cukrów prostych. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Temat: Wykrywanie cukrów prostych
Problem badawczy: Czy w soku z cytryny, cebuli i winogron znajdują się cukry proste (o właściwościach redukujących)?
Hipoteza 1: W soku z cytryny, cebuli i winogron znajdują się cukry proste (redukujące).
Hipoteza 2: W sokach z cytryny, cebuli i winogron nie występują cukry proste (redukujące).
Materiał biologiczny:
sok z cytryny;
sok z cebuli;
sok z białych winogron.
Odczynniki:
odczynnik Fehlinga;
1‑procentowy roztwór glukozy;
roztwór skrobi.
Sprzęt laboratoryjny:
probówki;
stojak na probówki;
pipety;
łaźnia wodna.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D17GAGH34
Laboratorium 1
Przeprowadzono doświadczenie w laboratorium biologicznym w celu wykrycia cukrów prostych. Rozwiązano problem badawczy i zweryfikowano hipotezę.
Temat: wykrywanie cukrów prostych.
Problem badawczy: Czy w soku z cytryny, cebuli i winogron znajdują się cukry proste (o właściwościach redukujących)?
Hipoteza 1. W soku z cytryny, cebuli i winogron znajdują się cukry proste (redukujące).
Hipoteza 2. W sokach z cytryny, cebuli i winogron nie występują cukry proste (redukujące).
Materiał biologiczny: sok z cytryny, z białych winogron, z cebuli.
Odczynniki: odczynnik Fehlinga, 1‑procentowy roztwór glukozy, roztwór skrobi.
Sprzęt laboratoryjny: probówki, stojak na probówki, pipety, łaźnia wodna.
Szczegóły doświadczenia 1. Przeprowadzone doświadczenie to tzw. próba Fehlinga, która jest reakcją redoks.
Szczegóły doświadczenia 2. Aldehydy ulegają utlenieniu do kwasów karboksylowych, miedź ze stopnia utlenienia II redukuje się do I.
Szczegóły doświadczenia 3. Wytrącający się tlenek miedzi(I) CuIndeks dolny 22O jest produktem szybkiej reakcji powstających jonów CuIndeks górny ++ z jonami hydroksylowymi.
Instrukcja wykonania doświadczenia:
1. Podpisano probówki.
2. Do probówek z kontrolą pozytywną i negatywną wlano odpowiednie roztwory.
3. Do kolejnych probówek wlano: sok z cebuli oraz sok z winogron.
4. Do wszystkich probówek dodano po kilka kropli odczynnika Fehlinga.
5. Umieszczono probówki w łaźni wodnej i ogrzewano przez 5 minut w temperaturze 100 stopni Celsjusza.
6. Obserwowano zachodzące zmiany w probówkach.
Obserwacje. Pod wpływem odczynnika Fehlinga i ogrzania:
- roztwór skrobi (kontrola negatywna) nie zmienił się;
- w roztworze glukozy (kontrola pozytywna) wytrącił się ceglastoczerwony osad;
- w soku z cytryny, cebuli i białych winogron wytrącił się ceglastoczerwony osad.
Wnioski: W soku z cytryny, cebuli i winogron znajdują się cukry proste, wykazujące właściwości redukujące. Hipoteza 1 jest prawdziwa, a hipoteza 2 nieprawdziwa.
Podsumowanie: Próba Fehlinga pozwala wykryć obecność cukrów prostych dzięki ich właściwościom redukującym.
Próba Barfoeda pozwala na odróżnienie cukrów prostych od wielocukrów. Po dodaniu odczynnika i krótkim ogrzaniu (do 5 min) roztwór zmienia zabarwienie z lekko niebieskiego na pomarańczowe i wytrąca się ceglastoczerwony osad CuIndeks dolny 22O, jeśli w badanej próbce są monosacharydy. W przypadku oligo- i polisacharydów niebieskie zabarwienie nie zmienia się w tym czasie (przedłużenie ogrzewania prowadzi do rozkładu wielocukrów na cukry proste i może zaburzyć wyniki).
Do 5 probówek dodano kolejno: 1 – glukozę, 2 – fruktozę, 3 – laktozę, 4 – sacharozę i 5 – skrobię.
Banany są bogatym źródłem składników mineralnych, witamin z grupy B, witaminy C oraz kwasu foliowego. Zawierają również dużo białka oraz węglowodanów, których zawartość jest znacznie wyższa niż w innych owocach. W niedojrzałych, zielonych owocach banana cukry występują głównie pod postacią skrobi, która w miarę dojrzewania owoców prawie w całości ulega rozkładowi na cukry proste.
Wadą tych owoców jest to, że wykazują one stosunkowo krótką trwałość i dlatego przywozi się owoce niedojrzałe, które dojrzewają dopiero na miejscu ich przeznaczenia.
Wykrywanie lipidów
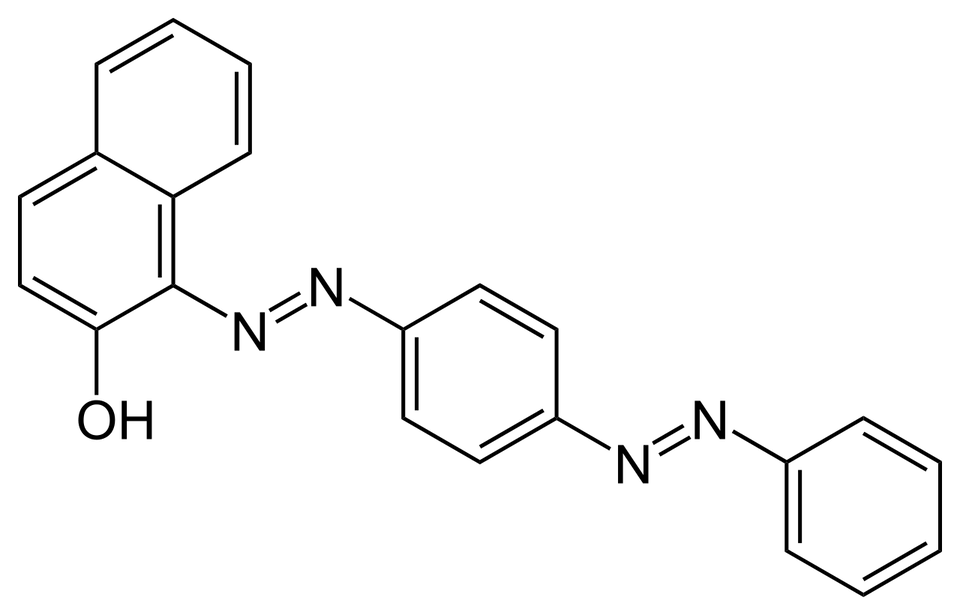
W celu wykrycia lipidów w komórkach należy użyć Sudanu III.
Jest to czerwony barwnik azowy, rozpuszczalny w rozpuszczalnikach organicznych – benzenie, acetonie oraz etanolu.
Barwnik bardzo dobrze rozpuszcza się w tłuszczach, dlatego gdy Sudan III łączy się z lipidami, przybierają one czerwony kolor.
Przeprowadź doświadczenie w laboratorium biologicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje, a następnie sformułuj wnioski.
Temat: Wykrywanie lipidów w materiale roślinnym.
Problem badawczy: Czy olej roślinny i nasiona rzepaku zawierają lipidy?
Hipoteza: Olej roślinny i nasiona rzepaku zawierają lipidy.
Sprzęt laboratoryjny:
probówki;
stojak na probówki;
pipeta;
palnik;
drewniana łapa;
moździerz z tłuczkiem;
szkiełko zegarkowe;
bagietka szklana;
szkiełko podstawowe;
szkiełko nakrywkowe;
mikroskop.
Materiały:
roztwór alkoholowy Sudanu III;
woda destylowana;
oliwa/olej;
nasiona rzepaku.
Instrukcja:
Próba kontrolna negatywna
Załóż fartuch, rękawiczki jednorazowe oraz okulary ochronne.
Do probówki wlej 2 ml wody destylowanej i dodaj 2 krople roztworu alkoholowego Sudanu III.
Umieść probówkę w drewnianej łapie. Zachowując ostrożność, ogrzewaj probówkę nad palnikiem.
Obserwuj i zapisz wynik obserwacji.
Próba kontrolna pozytywna
Do probówki wlej 2 ml oliwy/oleju i dodaj 2 krople roztworu alkoholowego Sudanu III.
Umieść probówkę w drewnianej łapie i zachowując ostrożność, ogrzewaj probówkę nad palnikiem.
Obserwuj i zapisz wynik obserwacji.
Próba badawcza
Kilka nasion rzepaku rozetrzyj w moździerzu.
Niewielką ilość zmiażdżonych nasion przełóż na szkiełko zegarkowe. Dodaj 2–3 krople roztworu alkoholowego Sudanu III i zamieszaj bagietką szklaną.
Ogrzej szkiełko zegarkowe nad płomieniem palnika.
Z ogrzanego materiału roślinnego przygotuj preparat i obserwuj pod mikroskopem.
Zapisz wyniki obserwacji.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D17GAGH34
Zaproponuj metodę badania właściwości fizycznych tłuszczów roślinnych i zwierzęcych. W dzienniczku zapisz instrukcję wykonania doświadczenia oraz spodziewane obserwacje i wnioski.
Wykrywanie wiązań peptydowych

Reakcja biuretowa to charakterystyczna reakcja chemiczna umożliwiająca wykrywanie wiązań peptydowych (-CO‑NH-) w związkach chemicznych, w których znajdują się blisko siebie co najmniej dwa takie wiązania. Do związków tych należą peptydy i białka. Białka w środowisku zasadowym tworzą z jonami miedzi (CuIndeks górny 2+2+) fioletowoczerwone kompleksy, natomiast polipeptydy — purpurowoczerwone. Intensywność zabarwienia zależy od liczby wiązań peptydowych i dlatego reakcja biuretowa może być wykorzystywana do kolorymetrycznego oznaczania stężenia białek w roztworach.
Przeprowadź doświadczenie w laboratorium biologicznym w celu wykrycia białek w produktach spożywczych przy pomocy reakcji biuretowej. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje, a następnie sformułuj wnioski.
Temat: Wykrywanie białek w produktach spożywczych przy pomocy reakcji biuretowej
Problem badawczy:
Które produkty spożywcze zawierają białka?
Hipoteza:
Wszystkie produkty spożywcze zawierają białka.
Analizowane produkty spożywcze:
skrobia ziemniaczana;
białko jaja kurzego;
ser biały;
olej roślinny;
cukier.
Sprzęt laboratoryjny:
Odczynniki:
50% roztwór sody kaustycznej (NaOH);
10% roztwór siarczanu(VI) miedzi(II);
woda.
Instrukcja wykonania doświadczenia:
Włóż każdy produkt (cukier, skrobię, białko jaja kurzego, odrobinę sera białego oraz olej roślinny) do osobnej zlewki – w przypadku cieczy ok. 2 ml, w przypadku ciał stałych ok. 0,2 g.
Przygotuj próbę kontrolną – do zlewki nalej 1 ml 50% roztworu sody kaustycznej oraz 1 ml 10% roztworu siarczanu(VI) miedzi(II). Całość wymieszaj szklaną bagietką.
Do zlewek zawierających produkty spożywcze dodaj 1 ml 50% roztworu sody kaustycznej i 1 ml 10% roztworu siarczanu(VI) miedzi(II). Wymieszaj bagietką.
Obserwuj zmiany barwy w zlewkach. Porównaj zlewki zawierające produkty z próbą kontrolną.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D17GAGH34
Problem badawczy: Które produkty spożywcze zawierają białka?
Hipoteza: Wszystkie produkty spożywcze zawierają białka.
Analizowane produkty spożywcze:
skrobia ziemniaczana;
białko jaja kurzego;
ser biały;
olej roślinny;
cukier.
Sprzęt laboratoryjny:
6 zlewek;
5 szalek Petriego;
tryskawka z wodą;
szklane bagietki;
pipety.
Odczynniki:
50% roztwór sody kaustycznej (NaOH);
10% roztwór siarczanu(VI) miedzi(II); woda.
Doświadczenie polega na włożeniu próbki każdego produktu na osobnej zlewki – w przypadku cieczy ok. 2 ml, w przypadku ciał stałych ok. 0,2 g. Następnie należy przygotować próbę kontrolną - do zlewki nalano 1 ml 50% roztworu sody kaustycznej oraz 1 ml 10% roztworu siarczanu(VI) miedzi(II). Całość wymieszano szklaną bagietką.
Do zlewek zawierających produkty spożywcze dodano 1 ml 50% roztworu sody kaustycznej i 1 ml 10% roztworu siarczanu(VI) miedzi(II). Wymieszano bagietką. Zaobserwowano zmiany barwy w zlewkach. Porównano zlewki zawierające produkty z próbą kontrolną.
Obserwacje
W których probówkach doszło do zmiany barwy z jasnoniebieskiej na fioletową?
Próba kontrolna jest jasnoniebieska. Natomiast w probówce z białkiem jaja kurzego i serem białym mieszanina zabarwiła się na fioletowo. W pozostałych probówkach kolor pozostał jasnoniebieski.
Wnioski
Które z produktów spożywczych zawierają białka? Ser biały i białko jaja kurzego zawierają białka.
Zaproponuj inną metodę wykrywania białek. W dzienniczku zapisz instrukcję wykonania doświadczenia oraz spodziewane obserwacje i wnioski.
Film przedstawiający wykrywanie wiązań peptydowych za pomocą reakcji biuretowej

Film dostępny pod adresem /preview/resource/Rj3VV1b19TRxh
Doświadczenie dotyczy wykrywania wiązań peptydowych. W stojaku są umieszczone probówki. W pierwszej jest niebieski siarczan sześć miedzi dwa roztwór ce u es o cztery, w drugiej – bezbarwny wodorotlenek sodu roztwór en a o ha. W trzeciej probówce jest białko jaja kurzego. Osoba wykonująca doświadczenie do pustej probówki nabiera pipetą pewną ilość siarczanu sześć miedzi dwa oraz wodorotlenku sodu. Wodorotlenek miedzi dwa ce u o ha wytrąca się w postaci niebieskiego osadu. Następnie na szalkę Petriego eksperymentator wylewa białko jaja kurzego i dodaje wodorotlenek miedzi dwa. Miesza. Białko wybarwia się na fioletowo.
Film przedstawiający przebieg reakcji ksantoproteinowej
Reakcja ksantoproteinowa – reakcji tej ulegają białka zawierające aminokwasy aromatyczne, których podstawnik (R) jest pierścieniem aromatycznym. Pierścień ten w obecności stężonego kwasu azotowego(V) może ulec reakcji „nitrowania”, dając w efekcie żółte zabarwienie roztworu. Reakcja ksantoproteinowa umożliwia wykrywanie białka, np. w produktach spożywczych.