Litowce - występowanie i zastosowanie
Znaczenie związków litowców
Związki litowców mają duże znaczenie praktyczne, ponieważ na ogół są rozpuszczalne w wodzie, a w przypadku związków sodu i potasu, stosunkowo łatwo dostępne i tanie. Lit różni się od innych pierwiastków 1. grupy bardzo małymi rozmiarami kationu litu oraz małą masą atomową. On i jego związki zaczęły być wykorzystywane od połowy XX w. m.in. do produkcji ogniw galwanicznych, leków oraz mydeł litowych.
Zastosowania związków litu
Preparaty, zawierające sole litu, stosowane są w leczeniu niektórych chorób psychicznych i neurologicznych. Innym przykładem ich wykorzystania są baterie jonowo‑litowe, które zasilają nasze telefony komórkowe, tablety, laptopy, a nawet samochody. Z kolei akumulatory litowo‑jonowe służą do zasilania domów i samolotów.
Litowce w kosmosie
W trakcie odbywania lotów kosmicznych, największym i zarazem najważniejszym wyzwaniem jest podtrzymywanie życia astronautów. Na stacjach i w pojazdach kosmicznych potrzeba nie tylko zmagazynowanego tlenu, ale również sprawnego usuwania z powietrza, którym oddychają astronauci, , czyli tlenku węgla(IV). Podczas krótkich lotów, jednym ze sposobów było zastosowanie wodorotlenku litu, który chętnie reaguje właśnie z tlenkiem węgla(IV), czego produktem ubocznym jest woda. Wodorotlenek litu nadaje się do tego zadania najlepiej spośród wszystkich wodorotlenków litowców, ponieważ ma małą masę molową, co pozwala optymalizować obciążenie pojazdu kosmicznego. Podczas dłuższych lotów kosmicznych, na pokładzie wahadłowca lub stacji kosmicznej, poza eliminowaniem , jest konieczne także odzyskiwanie tlenu. Na przykład w jednej z rosyjskich stacji wykorzystywano reakcję ponadtlenku potasu z tlenkiem węgla(IV). Produktem ubocznym tej reakcji był węglan potasu. Ale oczywiście technologie stosowane podczas lotów kosmicznych są stale rozwijane, a ich celem jest dążenie m.in. do odzyskiwania całej ilości tlenu, aby pojazdy/stacje mogły odbywać jak najdłuższe loty. Do tych nowoczesnych rozwiązań litowce już nie są potrzebne.
Zastosowanie związków sodu
Chlorek sodu
Chlorek sodu () – sól kuchenna jest oczywiście przyprawą, ale jednocześnie dostarcza jonów , które pełnią ważne funkcje w naszym organizmie. Są głównym kationem zewnątrzkomórkowym i są konieczne do utrzymania potencjału czynnościowego błon komórkowych. Sól fizjologiczna jest bardzo rozcieńczonym roztworem chlorku sodu. Sól kuchenną stosujemy również do konserwacji żywności, ale to nie wszystko. Jest też istotnym surowcem w przemyśle chemicznym – jako produkt wyjściowy do tworzenia chloru, wodorotlenku sodu oraz węglanu i wodorowęglanu sodu. Z kolei węglan sodu służy do produkcji m.in. szkła, mydła, środków piorących i barwników.

Chlebem i solą
Witanie chlebem i solą jest tradycyjną ceremonią w kilku słowiańskich kulturach, ale też w wielu innych. Chlorek sodu, czyli sól kuchenna, jest jednym z najważniejszych związków litowców, znanym i stosowanym od stuleci. Występuje jako kopalina – sól kamienna – oraz w dużych ilościach w wodzie morskiej. W Polsce złoża soli kamiennej znajdują się na terenie obecnego województwa małopolskiego w okolicach Wieliczki i Bochni, a także w okolicach Inowrocławia i Ciechocinka. W wielu krajach odzyskuje się chlorek sodu z wody morskiej. To przede wszystkim ważny dla człowieka składnik pokarmowy.

Wodorotlenek sodu
Wodorotlenek sodu jest powszechnie stosowany w procesach technologicznych, w których niezbędne jest użycie mocnej zasady:
przy produkcji paliw, m.in. do usuwania zanieczyszczeń siarkowych, obecnych w niskogatunkowej ropie naftowej, oraz przy produkcji biopaliw;
w przemyśle papierniczym (wybielanie włókien drzewnych);
jako przemysłowy, używany w gospodarstwie domowym, środek czyszczący (odtykacz do rur).

Wodorowęglan sodu
Soda do pieczenia to wodorowęglan sodu (). Stosuje się go jako składnik proszku do pieczenia, w lecznictwie (przy nadkwasocie) oraz w gaśnicach.
Węglan sodu
Węglan sodu , czyli soda kalcynowana, to z kolei składnik proszków do prania, środków do zmiękczania wody, surowiec do produkcji szkła.

Zastosowanie związków potasu
Związki potasu, ze względu na wysoką cenę oraz reaktywność, mają ograniczone zastosowanie. Do najważniejszych związków potasu należy tlenek potasu (), wodorotlenek potasu (), który znalazł zastosowanie jako środek suszący lub przy wyrobie mydeł potasowych, oraz azotan(V) potasu (), stosowany w przemyśle jako konserwant mięsa.
Potoczne nazwy związków litowców, które znalazły swoje zastosowanie.
Wzór | Nazwa systematyczna | Nazwa potoczna |
wodorotlenek sodu | soda żrąca/soda kaustyczna | |
wodorowęglan sodu | soda oczyszczona | |
węglan sodu | soda kalcynowana | |
chlorek sodu | sól kuchenna | |
azotan(V) sodu | saletra chilijska | |
wodorotlenek potasu | potaż | |
azotan(V) potasu | saletra indyjska |
luka do uzupełnienia luka do uzupełnienia plus luka do uzupełnienia luka do uzupełnienia strzałka w prawo, dwa K indeks dolny, dwa, koniec indeksu dolnego, C O indeks dolny, trzy nawias g zamknięcie nawiasu, koniec indeksu dolnego, plus luka do uzupełnienia luka do uzupełnienia
Zapoznaj się z treścią audiobooka i wykonaj ćwiczenia.
Wodorowęglan sodu, stosowany m.in. jako składnik proszku do pieczenia, ulega rozkładowi w podwyższonej temperaturze. W wyniku zachodzącej reakcji powstaje inna sól kwasu węglowego i wydziela się tlenek węgla(IV).
1. Napisz, za pomocą wzorów sumarycznych, równanie opisanej reakcji chemicznej.
2. Oblicz objętość tlenku węgla(IV) (w przeliczeniu na warunki normalne), jaka wydzieli się w wyniku termicznego rozkładu 2 g wodorowęglanu sodu. Załóż, że wydajność opisanej reakcji wynosi 90%. Wynik podaj w z dokładnością do jedności.
Przeprowadzono doświadczenie, zilustrowane na poniższym schemacie:
Przeprowadzono doświadczenie. Zapoznaj się z jego schematem.
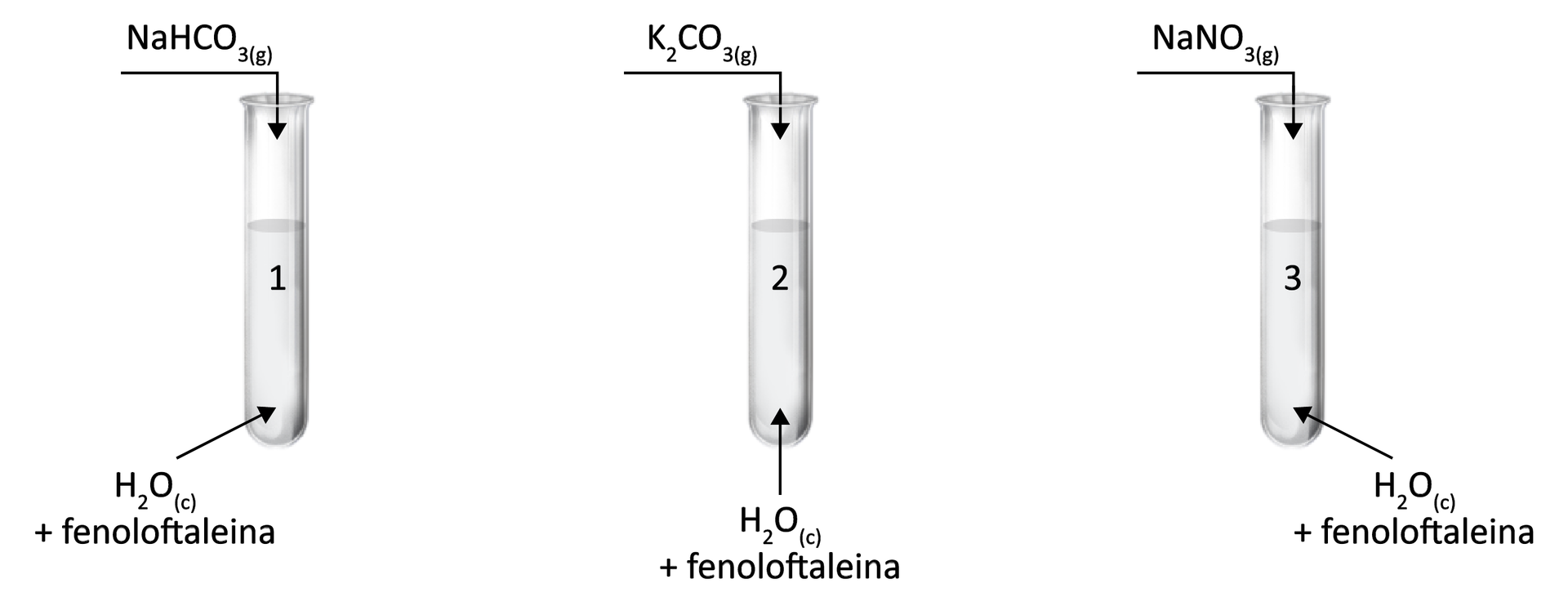
Przeanalizuj schemat doświadczenia, a następnie wykonaj polecenia.
1. Określ, w której probówce/w których probówkach otrzymano roztwór/roztwory o malinowym zabarwieniu.
2. Napisz, za pomocą wzorów sumarycznych, równanie reakcji odpowiedzialnej za odczyn roztworu, uzyskanego w probówce numer 2.
Sporządź mapę pojęciową, która zobrazuje zastosowania litowców jako pierwiastków. Odszukaj niezbędne informacje w dostępnych źródłach.